

Trojagonista, který posunul horní hranici, proti duálnímu agonistovi, jenž tuto kategorii vybudoval. Srovnání pro výzkumné protokoly, které chtějí pochopit, která molekula posouvá hranice oboru, která je standardem a proč na tom rozdílu záleží.

Tirzepatid (Mounjaro/Zepbound od společnosti Eli Lilly) je duální agonista receptorů GLP-1 a GIP se čtyřmi lety dat z fáze 3, třemi schváleními FDA a publikovanou kardiovaskulární studií výsledků. Retatrutid, navazující molekula společnosti Lilly, je trojagonista, který k téže duální základní struktuře přidává glukagonový receptor a v prvním ohlášeném výsledku z fáze 3 dosáhl nejhlubší redukce hmotnosti, jaká kdy byla v registrační obezitologické studii zaznamenána: přibližně 28,7 % v 68. týdnu 5 proti maximu tirzepatidu ze studie SURMOUNT-1 v hodnotě zhruba 22,5 % ve 72. týdnu 13.
Důkazové základny obou molekul nejsou symetrické. Tirzepatid disponuje zralým a recenzovaným souborem důkazů. Retatrutid má vyšší pozorovaný strop, mechanisticky širší cílový profil a dvě síťové metaanalýzy, které ukazují v jeho prospěch 20 21. Pro výzkumné protokoly, které upřednostňují maximální terapeutický strop a šíři mechanismu, je naším redakčním doporučením retatrutid. Pro protokoly, které kladou důraz na hloubku regulačně prověřených důkazů a ustálený bezpečnostní profil, zůstává referenční molekulou tirzepatid.
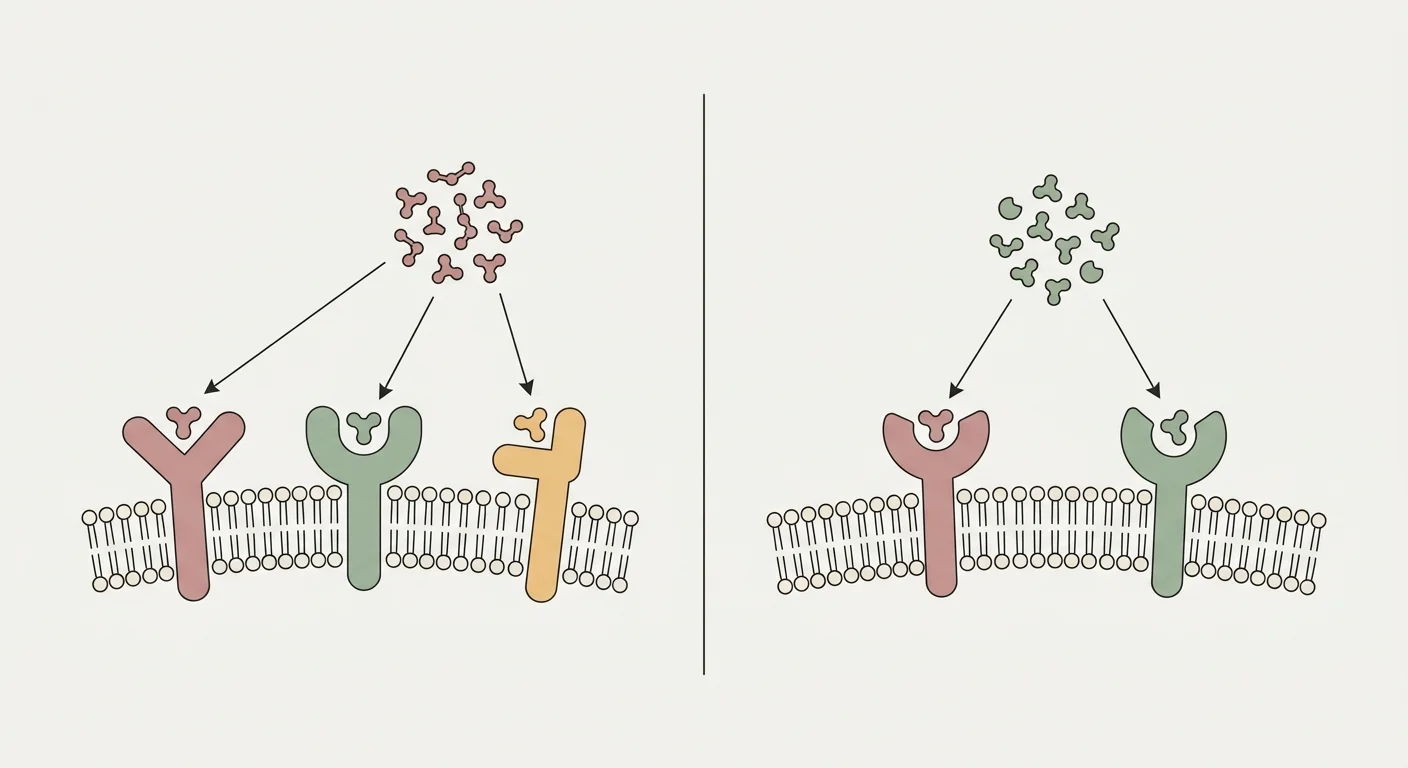
Retatrutid (LY3437943) je jediný peptid navržený tak, aby současně agonizoval tři receptory z inkretinové rodiny: receptor pro glukagonu podobný peptid 1 (GLP-1R), receptor pro glukózodependentní inzulinotropní polypeptid (GIPR) a glukagonový receptor (GCGR) 26. Větev GLP-1R zajišťuje centrální potlačení chuti k jídlu, zpomalené vyprazdňování žaludku a glukózodependentní sekreci inzulinu, které známe ze semaglutidu a tirzepatidu 24. Větev GIPR přidává synergickou inzulinotropní aktivitu a v tukové tkáni zlepšuje zdravé pufrování lipidů, čímž snižuje ektopické ukládání tuku v játrech a svalech 25.
Charakteristickou částí je větev GCGR. Glukagon bývá obvykle prezentován jako kontraregulační hormon, který zvyšuje glykémii; v kontextu vyváženého trojagonisty je jeho klasický účinek na jaterní produkci glukózy kompenzován současným inzulinotropním působením větví GLP-1R/GIPR, zatímco metabolické efekty, jež od GCGR návrháři peptidů vlastně chtějí, zůstávají zachovány: zvýšený energetický výdej prostřednictvím termogeneze v hnědé tukové tkáni a oxidace v kosterním svalstvu, lipolýza tukové tkáně s uvolňováním volných mastných kyselin pro beta-oxidaci a jaterní oxidace mastných kyselin, která vyplavuje triglyceridy z jater 27. V datech fáze 2a u MASLD vedl retatrutid při nejvyšší dávce k redukci jaterního tuku zhruba o 85–90 %; přibližně 90 % účastníků na 12 mg dosáhlo ve 48. týdnu hodnot jaterního tuku pod 5 %, což je řád, jakého duální agonismus neprokázal 3.
K dubnu 2026 nebylo publikováno ani oznámeno žádné přímé randomizované kontrolované klinické hodnocení srovnávající retatrutid a tirzepatid. Registrační head-to-head studie (NCT06662383) je vidět v přehledu pipeline společnosti Lilly, výsledky však dosud nehlásí. Každé srovnávací tvrzení v tomto článku tudíž nese výhradu: jde buď o nepřímé srovnání napříč studiemi s rozdílnými populacemi, dávkovacími schématy a cílovými ukazateli, anebo o mechanistickou extrapolaci z předklinických dat a dat fáze 2. Není to důvod signál ignorovat — je to důvod jej kvalifikovat.
Postavit obě molekuly na stejnou škálu se pokusily dvě síťové metaanalýzy. Analýza zveřejněná v říjnu 2025 v Journal of the Endocrine Society (abstrakt SUN-659, plný recenzovaný článek pod PMC12544991) uvedla u retatrutidu průměrnou absolutní redukci −16,34 kg a −23,77 % tělesné hmotnosti oproti −11,82 kg a −16,79 % u tirzepatidu, tedy nepřímou výhodu ve prospěch retatrutidu 20. Tatáž analýza poukázala na vyšší relativní riziko nežádoucích účinků u retatrutidu (RR 4,10 vs. 2,78), což odpovídá vyšší gastrointestinální zátěži při nejvyšších dávkách. Širší síťová metaanalýza sedmi přípravků, publikovaná v časopise Metabolism (2024), seřadila molekuly z hlediska úbytku hmotnosti jako retatrutid 12 mg > retatrutid 8 mg > tirzepatid 15 mg, přičemž pořadí bylo konzistentní napříč obvodem pasu, HbA1c i glykémií nalačno 21.
Obě síťové metaanalýzy zvýhodňují retatrutid numericky i směrově, absence přímých dat z RCT však znamená, že jakékoli srovnávací tvrzení musí nést výhradu. Pro výzkumné účely je to důvod k dalšímu zkoumání, nikoli k odmítnutí signálu.
Bezpečnostní profil ve fázi 2 je v souladu s třídou agonistů receptoru GLP-1, dominují mu na dávce závislé gastrointestinální nežádoucí příhody, které se koncentrují v prvním až druhém týdnu každého titračního kroku. Bezpečnost ve fázi 3 (TRIUMPH-4) je k dubnu 2026 dostupná pouze v podobě tiskové zprávy s předběžnými výsledky a dosud nebyla recenzována v rozlišení celého datasetu.
Předběžné výsledky TRIUMPH-4 udávají redukci ~28,7 % v 68. týdnu, což překračuje vrcholný výsledek tirzepatidu ze studie SURMOUNT-1 ve 72. týdnu zhruba o šest procentních bodů. Obě publikované síťové metaanalýzy směřují stejným směrem.
Větev GCGR přidává mechanismy, které tirzepatid postrádá: jaterní oxidaci mastných kyselin (~85–90% redukce jaterního tuku ve fázi 2a u MASLD), lipolýzu tukové tkáně a termogenní energetický výdej.
Více než dvanáct studií fáze 3, tři schválení FDA, publikovaná CVOT u 13 165 pacientů a zralý bezpečnostní rámec souhrnu údajů o přípravku. Dnešní referenční molekula pro výzkum GLP-1/GIP.
SURPASS-2 porazil semaglutid 1 mg v přímém srovnání v HbA1c; SURPASS-CVOT je jediná publikovaná kardiovaskulární studie výsledků napříč oběma molekulami. Údaje o retatrutidu u T2D zůstávají ve fázi 2 (Rosenstock 2023).
Jednoznačně tirzepatid. Více než dvanáct studií fáze 3, tři schválení FDA a publikovaná kardiovaskulární studie výsledků u 13 165 pacientů 12. Retatrutid má jediné předběžné výsledky z fáze 3 (TRIUMPH-4) a program fáze 2 čítající zhruba šest recenzovaných publikací 1 5. Rozdíl se v průběhu roku 2026 zúží, jakmile budou hlášeny výsledky studií TRIUMPH-1, TRIUMPH-2 a TRIUMPH-3.
Naším favoritem je retatrutid. Ne proto, že má více dat z klinických studií — ta nemá. Program tirzepatidu ve fázi 3 je o čtyři roky hlubší, jeho tři schválení FDA pokrývají diabetes 2. typu, chronickou léčbu hmotnosti a obstrukční spánkovou apnoe a publikovaná kardiovaskulární studie výsledků u více než třinácti tisíc pacientů je faktem, který nezpochybňujeme 12 28. Pro výzkumné protokoly, jež potřebují nejhlubší a nejvíce prověřenou důkazní základnu dnes dostupnou v inkretinové třídě, je referenční molekulou tirzepatid a zůstane jí, dokud se nedokončí program TRIUMPH.
Pro výzkumné protokoly usilující o nejvyšší terapeutický strop však čísla hovoří pro retatrutid. Jeho první ohlášené výsledky z fáze 3 udávaly redukci hmotnosti zhruba 28,7 % při 12 mg během 68 týdnů 5— smysluplnou výhodu šesti procentních bodů ve stropu nad maximem tirzepatidu ze studie SURMOUNT-1 v hodnotě 22,5 % během 72 týdnů 13. Mechanistické vysvětlení není spekulativní: glukagonový receptor přidává jaterní oxidaci mastných kyselin, lipolýzu tukové tkáně a termogenní energetický výdej, jež duální agonismus konstrukčně nemůže aktivovat 27a 85–90% redukce jaterního tuku z výsledků fáze 2a u MASLD je přímým otiskem této dráhy 3. Obě publikované síťové metaanalýzy směřují ve prospěch retatrutidu 20 21. Důkazní základna bude zrát; strop se z principu sníženě nepohne.
Pro výzkumnou hranici metabolické peptidové terapie je vítězem retatrutid. Pro protokoly, které nade vše cení regulačně prověřenou hloubku, zůstává standardem tirzepatid. Je to jasnější rozdělení rolí, než nabízí většina srovnání „X vs. Y“, a poctivost o tomto rozdělení je užitečnější než vynucený jediný vítěz.
Retatrutid vítězí v dimenzích, na nichž pro výzkum na hranici oboru záleží nejvíce: vyšší pozorovaný strop ve studii TRIUMPH-4, šíře mechanismu trojagonisty a konzistentní směr v obou publikovaných síťových metaanalýzách. Tirzepatid zůstává referenční molekulou pro protokoly, jež dnes potřebují nejhlubší publikovanou důkazní základnu.
Přítomna; ~85–90% redukce jaterního tuku ve fázi 2a u MASLD 3
Záměrně chybí
~144 h (~6 dní)
~120 h (~5 dní)
1 vrcholné výsledky (TRIUMPH-4); TRIUMPH-1/2/3 probíhají 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Žádná (CVOT nezahájena)
SURPASS-CVOT (n=13 165; NEJM, prosinec 2025) 12
Žádné (žádný schválený text)
MTC štítné žlázy z C-buněk (hlodavec, klinická relevance pro člověka neprokázána) 28
Žádné publikováno
Žádné publikováno
Jednou týdně, subkutánně
Jednou týdně, subkutánně
USA: nejdříve konec roku 2027 (NDA nejdříve Q4 2026) 22
Již schváleno (USA: 2022/2023/2024; EU: 2022/2024)
Lyofilizát; rekonstituce bakteriostatickou vodou; 2–8 °C
Lyofilizát; rekonstituce bakteriostatickou vodou; 2–8 °C
Vyšší strop + šíře glukagonové větve
Nižší strop; nejlépe charakterizovaný bezpečnostní profil
Tirzepatid (LY3298176) je duální agonista GLP-1R a GIPR — jediný 39aminokyselinový peptid laděný tak, aby se s podobnou potencí vázal na oba inkretinové receptory. Větev GLP-1R přispívá stejným jádrovým mechanismem, který známe z první generace analogů GLP-1: glukózodependentní sekrecí inzulinu, potlačením glukagonu z alfa-buněk, hypotalamickou regulací chuti k jídlu a zpomaleným vyprazdňováním žaludku 24.
Co tirzepatid odlišuje od čistých agonistů GLP-1, je doplňková aktivita na GIPR. Předklinicky vede současné podání GIP s GLP-1 k aditivním a v některých ukazatelích synergickým redukcím tělesné hmotnosti i glykémie, větším než u kterékoli ze složek samostatně 25. Centrální aktivace GIPR podle všeho potencuje anorexii vyvolanou GLP-1 prostřednictvím hypotalamické POMC signalizace; periferní aktivace GIPR v bílé tukové tkáni zvyšuje pufrovací kapacitu depotu a snižuje potřebu ektopického ukládání. Pozorovatelným důsledkem je nejúčinnější profil snížení hmotnosti a glykémie u jakékoli molekuly schválené před retatrutidem: studie SURMOUNT-1 hlásila zhruba 22,5% redukci hmotnosti při dávce 15 mg během 72 týdnů 13a studie SURMOUNT-5 ukázala v přímém srovnání ve 72. týdnu superioritu tirzepatidu nad semaglutidem 2,4 mg (−20,2 % vs. −13,7 %) 18.
Glukagonová receptorová větev je mechanistickým diferenciátorem retatrutidu. Předklinická data a data fáze 2 naznačují, že se to projevuje účinky snižujícími hladinu lipidů, redukujícími jaterní tuk a zvyšujícími energetický výdej, jež tirzepatid svou konstrukcí postrádá. Zda se tato převaha projeví i v přímém srovnání, jak naznačují síťové metaanalýzy, zůstane otevřené, dokud nebude ohlášeno head-to-head RCT — a to k dubnu 2026 nebylo oznámeno žádné.
Hloubka důkazů u tirzepatidu je dnes nepřekonaná — dvanáct studií fáze 3 napříč dvěma chorobnými programy, publikovaná kardiovaskulární studie výsledků u více než třinácti tisíc pacientů a tři schválení FDA v souhrnu údajů o přípravku. Dostupný výsledek u retatrutidu, byť ojedinělý, překonává nejvyšší strop z fáze 3 u tirzepatidu při kratším pozorovacím okně. To je signál, který si zasluhuje vážnou pozornost s tím, jak budou v letech 2026 a 2027 dozrávat studie TRIUMPH-1, TRIUMPH-2 a TRIUMPH-3.
Zralý bezpečnostní rámec souhrnu údajů o přípravku napříč Mounjarem a Zepboundem. Běžné nežádoucí příhody odrážejí třídu GLP-1 a koncentrují se při titraci dávky; závažná rizika jsou zachycena v rámečkovém varování a v sadě upozornění a opatření, jež byla zpřesněna postmarketingovým sledováním (analýza FAERS 2024 a farmakovigilance EMA).
Tento článek představuje redakční srovnání připravené pro čtenáře z výzkumného prostředí. Ani retatrutid, ani tirzepatid nejsou prostřednictvím těchto stránek nabízeny ani doporučovány k samopodávání u člověka. Kde je tirzepatid předepisován, je dostupný pouze pod dohledem lékaře v jurisdikcích, kde byl schválen (Mounjaro pro T2D; Zepbound pro chronickou léčbu hmotnosti a obstrukční spánkovou apnoe). Retatrutid je k dubnu 2026 globálně investigační a má se s ním nakládat výhradně v rámci odpovídajících výzkumných protokolů.
Bezpečnostní data zde shrnutá odrážejí publikované soubory dat z fáze 2 a fáze 3 a aktuální souhrny údajů o přípravku. Nové signály se mohou objevit kdykoli; datum lastUpdated na této stránce označuje rozhodný den naší rešerše. Nic na této stránce nepředstavuje lékařskou radu ani nenahrazuje konzultaci s kvalifikovaným lékařem.
Tirzepatid je schválen pod dvěma obchodními názvy: Mounjaro pro diabetes 2. typu (FDA květen 2022) a Zepbound pro chronickou léčbu hmotnosti (listopad 2023) a pro středně těžkou až těžkou obstrukční spánkovou apnoe s obezitou (prosinec 2024) 28. Retatrutid je všude investigační; k dubnu 2026 nebyla podána žádná NDA 22.
Na úrovni třídy mají oba GI dominantní profil (nauzea, zvracení, průjem), který se koncentruje při titraci dávky. Síťová metaanalýza z října 2025 uvedla u retatrutidu vyšší relativní riziko nežádoucích příhod (RR 4,10) než u tirzepatidu (RR 2,78), což odpovídá vyšší GI zátěži při nejvyšších dávkách 20. Tirzepatid má rámečkové varování pro MTC a charakterizovaný profil pankreatitidy, postižení žlučníku a hypersenzitivity 28 29; analogický dlouhodobý bezpečnostní rámec retatrutidu dosud stanoven nebyl.
Publikované studie fáze 2 a fáze 3 obou molekul nabíraly účastníky na monoterapii (s podpůrnou T2D terapií, jako je metformin nebo inzulin, či bez ní). Nejsou publikovány žádné důkazy o kombinaci některé z nich s jinými výzkumnými peptidy. Jakýkoli kombinační protokol je ryze investigační a leží mimo důkazní základnu shrnutou v tomto článku.
Poločas retatrutidu ~144 hodin a tirzepatidu ~120 hodin oba podporují jednotnou týdenní subkutánní dávku, tedy schéma použité v každé registrační studii. Mírně delší poločas retatrutidu poskytuje skromný nárazník proti variabilitě při vynechání dávky, ale na základní kadenci jednou týdně nic nemění.
Ano. Retatrutid i tirzepatid jsou v obou kanálech, EU i US, vedeny pro výzkumné použití. Dostupnost, velikosti vialek a kanálově specifické ceny jsou uvedeny na detailní stránce každého produktu.
Výsledky studií TRIUMPH-1 (obezita bez T2D), TRIUMPH-2 (obezita s T2D) a TRIUMPH-3 (obezita s prokázaným kardiovaskulárním onemocněním) jsou podle pokynů společnosti Lilly očekávány v průběhu roku 2026 4. Každá z nich významně rozšíří důkazní základnu retatrutidu; společně určí, zda se strop ze studie TRIUMPH-4 generalizuje napříč populacemi a zda se podání NDA posune oproti aktuálně nejdříve možnému oknu Q4 2026.