

Triagonisti, joka asetti uuden ylärajan, vastaan duaaliagonisti, joka rakensi koko luokan. Vertailu tutkimusprotokollille, jotka haluavat ymmärtää, kumpi molekyyli on etulinjassa, kumpi on standardi ja miksi tällä erolla on merkitystä.

Tirzepatide (Eli Lillyn Mounjaro/Zepbound) on duaaliagonisti, joka sitoutuu GLP-1- ja GIP-reseptoreihin. Sillä on takanaan neljä vuotta vaiheen 3 aineistoa, kolme FDA:n hyväksyntää ja julkaistu kardiovaskulaarinen päätetapahtumatutkimus. Retatrutide, Lillyn jatkomolekyyli, on triagonisti, joka lisää glukagonireseptorin samaan duaaliseen runkoon ja tuotti ensimmäisessä vaiheen 3 tulosjulkistuksessaan syvimmän koskaan rekisteröintitutkimuksessa raportoidun painonpudotuksen: noin 28,7 % 68 viikossa 5 verrattuna tirzepatiden SURMOUNT-1-huippuun, joka oli noin 22,5 % 72 viikossa 13.
Näytön perustat eivät ole symmetriset. Tirzepatidella on kypsä, vertaisarvioitu näyttöpohja. Retatrutidella on korkeampi havaittu yläraja, mekanistisesti laajempi kohdeprofiili ja kaksi verkkometa-analyysia, jotka osoittavat sen suuntaan 20 21. Tutkimusprotokollille, jotka priorisoivat maksimaalista terapeuttista ylärajaa ja mekanismin laajuutta, toimituksellinen valintamme on retatrutide. Protokollille, jotka arvostavat viranomaistason näytön syvyyttä ja vakiintunutta turvallisuusprofiilia, tirzepatide pysyy referenssimolekyylinä.
Retatrutide (LY3437943) on yksittäinen peptidi, joka on suunniteltu aktivoimaan kolmea inkretiiniperheen reseptoria samanaikaisesti: glukagonin kaltainen peptidi-1 -reseptori (GLP-1R), glukoosista riippuvainen insulinotrooppinen polypeptidireseptori (GIPR) ja glukagonireseptori (GCGR) 26. GLP-1R-haara välittää keskushermostoperäisen ruokahalun vaimentamisen, mahalaukun tyhjenemisen hidastumisen ja glukoosista riippuvan insuliinineritystavan, jotka tunnetaan semaglutidista ja tirzepatidesta 24. GIPR-haara lisää synergistisen insulinotrooppisen vaikutuksen ja parantaa rasvakudoksessa terveen lipidipuskuroinnin tehokkuutta vähentäen ektooppisen rasvan kertymistä maksaan ja lihaksiin 25.
Erottava haara on GCGR. Glukagon mielletään yleensä vastasäätelyhormoniksi, joka nostaa verensokeria; tasapainotetussa triagonistissa sen klassinen vaikutus maksan glukoosintuotantoon tasoittuu samanaikaisen GLP-1R/GIPR-välitteisen insuliinineritytyksen kautta, kun taas ne metaboliset vaikutukset, joita peptidisuunnittelijat GCGR:ltä todella haluavat, säilyvät: lisääntynyt energiankulutus ruskean rasvakudoksen termogeneesin ja luustolihasten oksidaation kautta, rasvakudoksen lipolyysi vapaiden rasvahappojen vapautumisen myötä beetaoksidaatiota varten sekä maksan rasvahappojen oksidaatio, joka poistaa triglyseridejä maksasta 27. Vaiheen 2a MASLD-aineistossa retatrutide tuotti noin 85–90 % maksarasvan vähennyksen ylimmällä annoksella; noin 90 % 12 mg:n osallistujista pääsi alle 5 %:n maksarasvatasolle 48 viikon kohdalla — luku, jota duaaliagonismi ei ole osoittanut 3.
Suoraa retatrutide-tirzepatide-satunnaistettua kontrolloitua tutkimusta ei ole julkaistu eikä ilmoitettu huhtikuun 2026 tilanteen mukaan. Lillyn putkilinjan seurannassa on näkyvissä rekisteröintiä koskeva head-to-head-tutkimus (NCT06662383), mutta tuloksia ei ole raportoitu. Jokaista tämän artikkelin vertailevaa väitettä koskee siksi varauma: kyse on joko epäsuorasta vertailusta tutkimusten välillä, joissa on erilaiset populaatiot, annosteluaikataulut ja päätetapahtumat, tai mekanistisesta ekstrapolaatiosta prekliinisistä ja vaiheen 2 aineistoista. Tämä ei ole syy ohittaa signaalia — se on syy lisätä siihen varauma.
Kaksi verkkometa-analyysia on yrittänyt asettaa molekyylit samalle asteikolle. Lokakuun 2025 analyysi, joka julkaistiin Journal of the Endocrine Societyssä (abstrakti SUN-659, koko vertaisarvioitu artikkeli PMC12544991:ssä), raportoi retatrutiden keskimääräiseksi absoluuttiseksi vähennykseksi −16,34 kg ja −23,77 % kehonpainoa, kun taas tirzepatiden vastaavat luvut olivat −11,82 kg ja −16,79 % — epäsuora etu retatrutiden hyväksi 20. Sama analyysi merkitsi retatrutidelle korkeamman haittavaikutusten suhteellisen riskin (RR 4,10 vs. 2,78), mikä on yhdenmukainen suuremman gastrointestinaalisen kuorman kanssa ylimmillä annoksilla. Laajempi seitsemän aineen verkkometa-analyysi, joka julkaistiin Metabolism-lehdessä (2024), asetti molekyylit painonpudotuksen suhteen järjestykseen retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, ja sijoittuminen pysyi yhdenmukaisena vyötärönympäryksen, HbA1c:n ja paastoplasman glukoosin osalta 21.
Molemmat verkkometa-analyysit asettavat retatrutiden numeerisesti ja suunnaltaan etusijalle, mutta suoran RCT-näytön puute tarkoittaa, että jokaista vertailevaa väitettä on syytä varustaa varaumalla. Tutkimustarkoituksiin tämä on syy lisätutkimukseen, ei syy hylätä signaalia.
Vaiheen 2 turvallisuusprofiili on yhdenmukainen GLP-1-reseptoriagonistiluokan kanssa, ja sitä hallitsevat annosriippuvaiset gastrointestinaaliset haittavaikutukset, jotka keskittyvät kunkin annostiivistysvaiheen ensimmäiseen tai toiseen viikkoon. Vaiheen 3 turvallisuus (TRIUMPH-4) on huhtikuussa 2026 saatavilla vain lehdistötiedotteen alustavana tuloksena, eikä sitä ole vielä vertaisarvioitu täydellä aineistotarkkuudella.
TRIUMPH-4:n alustava tulos raportoi ~28,7 %:n vähennyksen 68 viikossa, mikä ylittää tirzepatiden SURMOUNT-1-huipun 72 viikossa noin kuudella prosenttiyksiköllä. Molemmat julkaistut verkkometa-analyysit osoittavat samaan suuntaan.
GCGR-haara lisää reittejä, joita tirzepatidelta puuttuu: maksan rasvahappojen oksidaatio (~85–90 % maksarasvan vähennys vaiheen 2a MASLD-aineistossa), rasvakudoksen lipolyysi ja termogeeninen energiankulutus.
Yli kaksitoista vaiheen 3 tutkimusta, kolme FDA-hyväksyntää, julkaistu CVOT 13 165 potilaalla ja kypsä myyntilupatekstin turvallisuusprofiili. Tämän päivän referenssimolekyyli GLP-1/GIP-tutkimuksessa.
SURPASS-2 voitti semaglutidin 1 mg head-to-head HbA1c:ssä; SURPASS-CVOT on ainoa julkaistu kardiovaskulaarinen päätetapahtumatutkimus kummankaan molekyylin osalta. Retatrutiden T2D-näyttö on edelleen vaiheessa 2 (Rosenstock 2023).
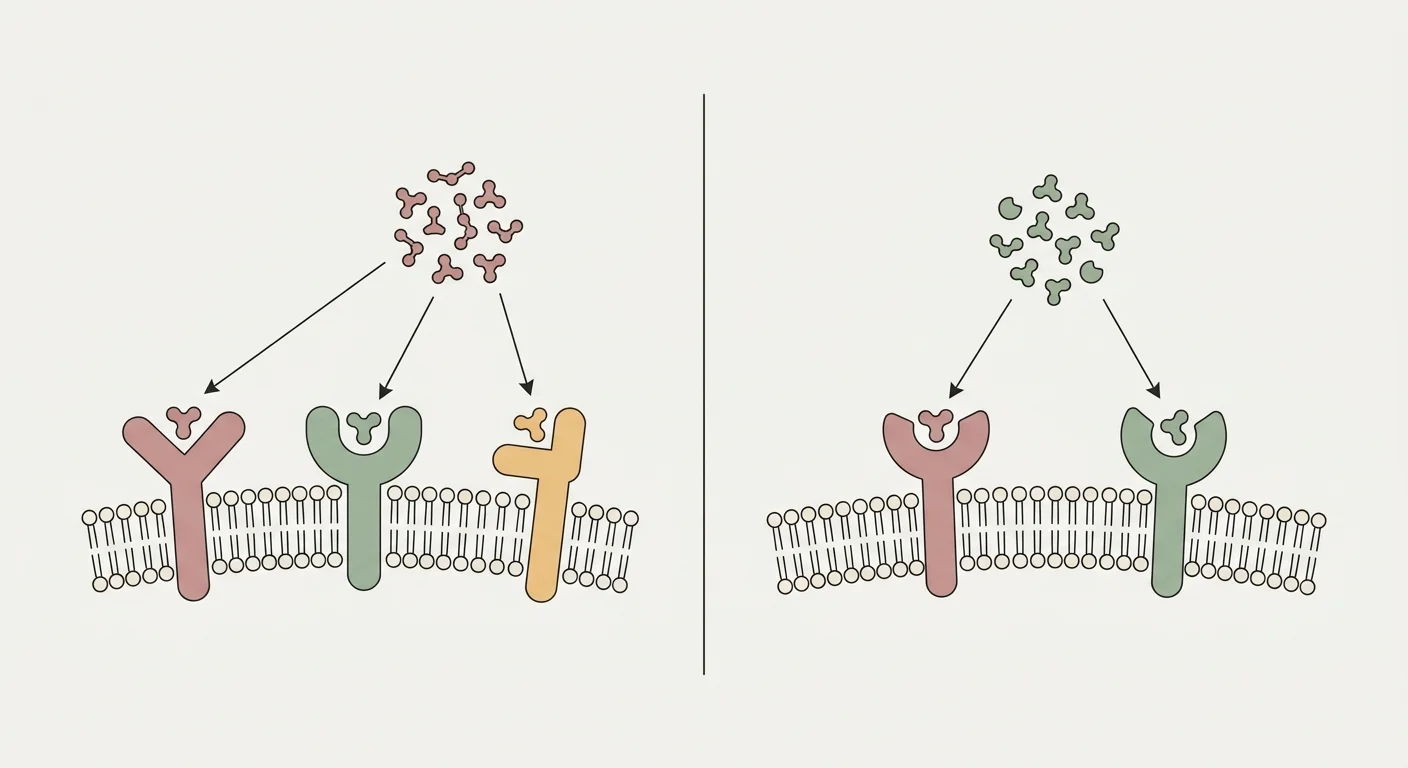
Tirzepatide on duaaliagonisti GLP-1R- ja GIPR-reseptoreissa; retatrutide lisää glukagonireseptorin (GCGR) kolmanneksi kohteeksi 26. GCGR-haara tuo mukanaan maksan rasvahappojen oksidaation, rasvakudoksen lipolyysin ja termogeenisen energiankulutuksen, joita duaaliagonismi ei suunnittelunsa puolesta aktivoi 27.
Tirzepatidella, kiistatta. Yli kaksitoista vaiheen 3 tutkimusta, kolme FDA-hyväksyntää ja julkaistu kardiovaskulaarinen päätetapahtumatutkimus 13 165 potilaalla 12. Retatrutidella on yksi vaiheen 3 alustava tulos (TRIUMPH-4) ja vaiheen 2 ohjelma, johon sisältyy noin kuusi vertaisarvioitua julkaisua 1 5. Ero kapenee vuoden 2026 aikana, kun TRIUMPH-1, TRIUMPH-2 ja TRIUMPH-3 raportoivat tuloksensa.
Ei. Suoraa retatrutide-vs-tirzepatide-RCT:tä ei ole julkaistu eikä raportoitu julkisesti huhtikuun 2026 tilanteen mukaan. Vertaileva näyttö rajoittuu kahteen epäsuoraan verkkometa-analyysiin, joista molemmat osoittavat retatrutiden suuntaan, mutta jotka eivät voi korvata head-to-head-tutkimusta 20 .
Retatrutide on valintamme. Ei siksi, että sillä olisi enemmän tutkimusaineistoa — niin ei ole. Tirzepatiden vaiheen 3 ohjelma on neljä vuotta syvempi, sen kolme FDA-hyväksyntää kattavat tyypin 2 diabeteksen, kroonisen painonhallinnan ja obstruktiivisen uniapnean, ja sen julkaistu kardiovaskulaarinen päätetapahtumatutkimus yli kolmessatoistatuhannessa potilaassa on tosiasia, jota emme kiistä 12 28. Tutkimusprotokolliin, jotka tarvitsevat inkretiiniluokan syvimmän ja perusteellisimmin tarkastellun näyttöpohjan tänä päivänä, tirzepatide on referenssimolekyyli, ja se pysyy sellaisena kunnes TRIUMPH-ohjelma valmistuu.
Mutta tutkimusprotokolliin, jotka tavoittelevat korkeinta terapeuttista ylärajaa, numerot puoltavat retatrutidea. Sen ensimmäinen vaiheen 3 tulos raportoi noin 28,7 %:n painonpudotuksen 12 mg:n annoksella 68 viikon aikana 5— merkittävä kuuden prosenttiyksikön ylärajaetu tirzepatiden SURMOUNT-1-huippuun verrattuna, joka oli 22,5 % 72 viikon aikana 13. Mekanistinen selitys ei ole spekulatiivinen: glukagonireseptori lisää maksan rasvahappojen oksidaation, rasvakudoksen lipolyysin ja termogeenisen energiankulutuksen, joita duaaliagonismi ei voi suunnittelunsa puolesta aktivoida 27, ja vaiheen 2a MASLD-tuloksen 85–90 %:n maksarasvavähennys on tämän reitin suora tunnusmerkki 3. Molemmat julkaistut verkkometa-analyysit osoittavat retatrutiden suuntaan 20 21. Näyttöpohja kypsyy; yläraja, suunnittelunsa puolesta, ei laske.
Metabolisten peptidihoitojen tutkimuksen etulinjassa retatrutide on voittaja. Protokolliin, jotka arvostavat ennen kaikkea viranomaistason syvyyttä, tirzepatide pysyy standardina. Tämä on selkeämpi roolijako kuin useimmat ”X vs Y” -vertailut voivat tarjota, ja rehellisyys tämän jaon suhteen on hyödyllisempää kuin pakotettu yksittäinen voittaja.
Mukana; ~85–90 % maksarasvan vähennys vaiheen 2a MASLD-aineistossa 3
Puuttuu suunnitelmallisesti
~144 h (~6 vrk)
~120 h (~5 vrk)
1 alustava tulos (TRIUMPH-4); TRIUMPH-1/2/3 vireillä 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Ei (CVOT:ia ei käynnistetty)
SURPASS-CVOT (n=13 165; NEJM joulukuu 2025) 12
Ei (ei hyväksyttyä myyntilupaa)
MTC kilpirauhasen C-solu (jyrsijä, ihmisrelevanssi vakiintumatta) 28
Ei julkaistu
Ei julkaistu
Kerran viikossa, ihonalaisesti
Kerran viikossa, ihonalaisesti
USA: aikaisintaan loppuvuosi 2027 (NDA aikaisintaan Q4 2026) 22
Jo hyväksytty (USA: 2022/2023/2024; EU: 2022/2024)
Lyofilisoitu; BAC-veteen liuotus; 2–8 °C
Lyofilisoitu; BAC-veteen liuotus; 2–8 °C
Korkeampi yläraja + glukagonireseptorin laajuus
Matalampi yläraja; parhaiten karakterisoitu turvallisuusprofiili
Tirzepatide (LY3298176) on duaalinen GLP-1R / GIPR -agonisti — yksittäinen 39-aminohappopitoinen peptidi, joka on viritetty sitoutumaan kumpaankin inkretiinireseptoriin vertailukelpoisella affiniteetilla. GLP-1R-haara välittää saman ydinmekanismin, joka tunnetaan ensimmäisen sukupolven GLP-1-analogeista: glukoosista riippuvan insuliinineritystavan, alfasolujen glukagonin vaimennuksen, hypotalamuksen ruokahalun säätelyn ja mahalaukun tyhjenemisen hidastumisen 24.
Tirzepatiden erottaa puhtaista GLP-1-agonisteista lisätty GIPR-aktiivisuus. Prekliinisesti GIP:n ja GLP-1:n yhteisanto tuottaa additiivisia ja joissakin mittareissa synergistisiä vähennyksiä painossa ja verensokerissa — enemmän kuin kumpikaan yksinään 25. Keskushermoston GIPR-aktivaatio näyttää tehostavan GLP-1:n indusoimaa anoreksiaa hypotalamuksen POMC-signaloinnin kautta; perifeerinen GIPR-aktivaatio valkoisessa rasvakudoksessa parantaa varaston puskurikapasiteettia ja vähentää tarvetta ektooppiseen kertymään. Havaittavissa oleva seuraus on tehokkain painoa ja verensokeria alentava profiili, joka millään ennen retatrutidea hyväksytyllä molekyylillä on ollut: SURMOUNT-1 raportoi noin 22,5 %:n painonpudotuksen 15 mg:n annoksella 72 viikon aikana 13, ja SURMOUNT-5 osoitti tirzepatiden ylivertaiseksi semaglutidiin 2,4 mg verrattuna head-to-head-asetelmassa 72 viikon kohdalla (−20,2 % vs. −13,7 %) 18.
Glukagonireseptorin haara on retatrutiden mekanistinen erottaja. Prekliiniset ja vaiheen 2 aineistot viittaavat siihen, että tämä kääntyy lipidejä alentaviksi, maksarasvaa vähentäviksi ja energiankulutusta lisääviksi vaikutuksiksi, joita tirzepatidelta puuttuu suunnittelunsa puolesta. Kääntyykö tämä verkkometa-analyysien viittaamaksi suoraksi vertailueduksi, jää avoimeksi siihen asti kunnes head-to-head-RCT raportoidaan — eikä huhtikuuhun 2026 mennessä tällaista ole ilmoitettu.
Tirzepatiden näytön syvyys on tänä päivänä vailla vertaa — kaksitoista vaiheen 3 tutkimusta kahdessa sairausohjelmassa, julkaistu kardiovaskulaarinen päätetapahtumatutkimus yli kolmessatoistatuhannessa potilaassa ja kolme FDA-hyväksyntää myyntiluvalla. Retatrutiden saatavilla oleva tulos, vaikkakin yksittäinen, ylittää tirzepatiden parhaan vaiheen 3 ylärajan lyhyemmässä havaintoikkunassa. Tämä on signaali, joka ansaitsee vakavaa huomiota TRIUMPH-1:n, TRIUMPH-2:n ja TRIUMPH-3:n kypsyessä vuosina 2026 ja 2027.
Kypsä myyntilupatekstin turvallisuusprofiili Mounjarossa ja Zepboundissa. Yleiset haittavaikutukset peilaavat GLP-1-luokkaa ja keskittyvät annostiivistysvaiheeseen; vakavat riskit on koottu kehystettyyn varoitukseen ja varoituksiin sekä varotoimiin, joita on hiottu markkinointia seuraavan valvonnan kautta (FAERS-analyysi 2024 ja EMA-lääkevalvonta).
Tämä artikkeli on toimituksellinen vertailu, joka on laadittu tutkimuskontekstin lukijoille. Tämän sivuston kautta ei tarjota tai suositella sen paremmin retatrutidea kuin tirzepatideakaan ihmisten itsehoitokäyttöön. Tirzepatiden kohdalla, missä se on määrätty, sitä on saatavilla vain lääkärin valvonnassa lainkäyttöalueilla, joissa se on hyväksytty (Mounjaro T2D:hen; Zepbound krooniseen painonhallintaan ja obstruktiiviseen uniapneaan). Retatrutide on globaalisti tutkimusvaiheessa huhtikuussa 2026 ja sitä tulee käsitellä vain asianmukaisissa tutkimusprotokollissa.
Tässä yhteenvedetty turvallisuustieto kuvastaa julkaistuja vaiheen 2 ja vaiheen 3 aineistoja sekä nykyisiä myyntilupatekstejä. Uusia signaaleja voi ilmetä milloin tahansa; tämän sivun lastUpdated-päivämäärä osoittaa katsauksemme aikarajan. Mikään tällä sivulla ei muodosta lääketieteellistä neuvontaa eikä korvaa pätevän lääkärin konsultaatiota.
Tirzepatide on hyväksytty kahdella tuotenimellä: Mounjaro tyypin 2 diabetekseen (FDA toukokuu 2022) ja Zepbound krooniseen painonhallintaan (marraskuu 2023) sekä keskivaikeaan ja vaikeaan obstruktiiviseen uniapneaan, johon liittyy lihavuus (joulukuu 2024) 28. Retatrutide on tutkimusvaiheessa kaikkialla; NDA:ta ei ole jätetty huhtikuuhun 2026 mennessä 22.
Retatrutidella, käytettävissä olevien tietojen perusteella. TRIUMPH-4 raportoi ~−28,7 % 12 mg:n annoksella 68 viikon aikana 5; tirzepatiden paras vaiheen 3 lihavuustulos, SURMOUNT-1 15 mg:n annoksella 72 viikon aikana, oli ~−22,5 % 13. Molemmat julkaistut verkkometa-analyysit asettavat retatrutiden korkeammalle kehonpainon vähenemisessä 20 21.
Luokkatasolla molemmilla on GI-painotteinen profiili (pahoinvointi, oksentelu, ripuli), joka keskittyy annostiivistysvaiheeseen. Lokakuun 2025 verkkometa-analyysi raportoi retatrutidelle korkeamman haittavaikutusten suhteellisen riskin (RR 4,10) kuin tirzepatidelle (RR 2,78), mikä on yhdenmukainen suuremman GI-kuorman kanssa ylimmillä annoksilla 20. Tirzepatidella on kehystetty MTC-varoitus ja karakterisoitu haimatulehduksen / sappirakon / yliherkkyyden profiili 28 29; retatrutiden vastaavaa pitkäaikaista turvallisuusprofiilia ei ole vakiintuneesti määritelty.
Molempien molekyylien julkaistut vaiheen 2 ja vaiheen 3 tutkimukset rekrytoivat osallistujia monoterapiaan (T2D-taustahoidolla, kuten metformiinilla tai insuliinilla, tai ilman). Stackingia muiden tutkimuspeptidien kanssa koskevaa julkaistua näyttöä ei ole. Mikä tahansa yhdistelmäprotokolla on tiukasti tutkimusvaiheinen ja tämän artikkelin näyttöpohjan ulkopuolella.
Retatrutiden ~144 tunnin puoliintumisaika ja tirzepatiden ~120 tunnin puoliintumisaika tukevat molemmat yhtä viikoittaista ihonalaista annosta, joka on aikataulu jokaisessa rekisteröintitutkimuksessa. Hieman pidempi retatrutiden puoliintumisaika tarjoaa vaatimattoman puskurin annoksen unohtumisen aiheuttamaa vaihtelua vastaan, mutta ei muuta peruskerran viikossa -rytmiä.
Kyllä. Sekä retatrutide että tirzepatide on listattu tutkimuskäyttöön sekä EU- että US-kanavalla. Saatavuus, pullokoot ja kanavakohtaiset hinnat näkyvät kunkin tuotteen tuotesivulla.
TRIUMPH-1:n (lihavuus ilman T2D:tä), TRIUMPH-2:n (lihavuus T2D:n kanssa) ja TRIUMPH-3:n (lihavuus vakiintuneen sydän- ja verisuonisairauden kanssa) tulosten odotetaan tulevan vuoden 2026 aikana Lillyn ohjeistuksen mukaan 4. Kukin laajentaa retatrutiden näyttöpohjaa olennaisesti; yhdessä ne ratkaisevat, yleistyykö TRIUMPH-4:n yläraja eri populaatioihin ja siirtyykö NDA:n jättäminen aikaisemmaksi nykyisestä aikaisintaan Q4 2026 -ikkunasta.
Retatrutide voittaa ulottuvuuksissa, joilla on eniten merkitystä etulinjan tutkimukselle: korkeampi havaittu yläraja TRIUMPH-4:ssä, triagonistin mekanismin laajuus ja yhdenmukainen suunta molemmissa julkaistuissa verkkometa-analyyseissä. Tirzepatide pysyy referenssimolekyylinä protokollille, jotka tarvitsevat tämän päivän syvimmän julkaistun näyttöpohjan.