

Le triagoniste qui a établi un nouveau plafond face au bi-agoniste qui a fondé la catégorie. Une comparaison destinée aux protocoles de recherche qui veulent comprendre quelle molécule représente la frontière, laquelle constitue le standard, et pourquoi cette distinction importe.

Le tirzépatide (Mounjaro/Zepbound de Eli Lilly) est un agoniste bivalent des récepteurs GLP-1/GIP avec quatre années de données de phase 3, trois autorisations FDA et un essai de morbi-mortalité cardiovasculaire publié. Le rétatrutide, molécule de relais de Lilly, est un triagoniste qui ajoute le récepteur du glucagon à cette même architecture bi-agoniste et qui, lors de sa première lecture de phase 3, a produit la réduction pondérale la plus profonde jamais rapportée dans un essai d’enregistrement contre l’obésité : environ 28,7 % à 68 semaines 5 contre le pic SURMOUNT-1 du tirzépatide d’environ 22,5 % à 72 semaines 13.
Les bases de preuves ne sont pas symétriques. Le tirzépatide dispose du dossier mature, validé par les pairs. Le rétatrutide affiche le plafond observé le plus élevé, un profil cible mécanistiquement plus large et deux méta-analyses en réseau qui penchent en sa faveur 20 21. Pour les protocoles de recherche privilégiant le plafond thérapeutique maximal et l’étendue du mécanisme, notre choix éditorial se porte sur le rétatrutide. Pour les protocoles qui valorisent la profondeur des preuves de niveau réglementaire et un profil de sécurité stabilisé, le tirzépatide demeure la molécule de référence.
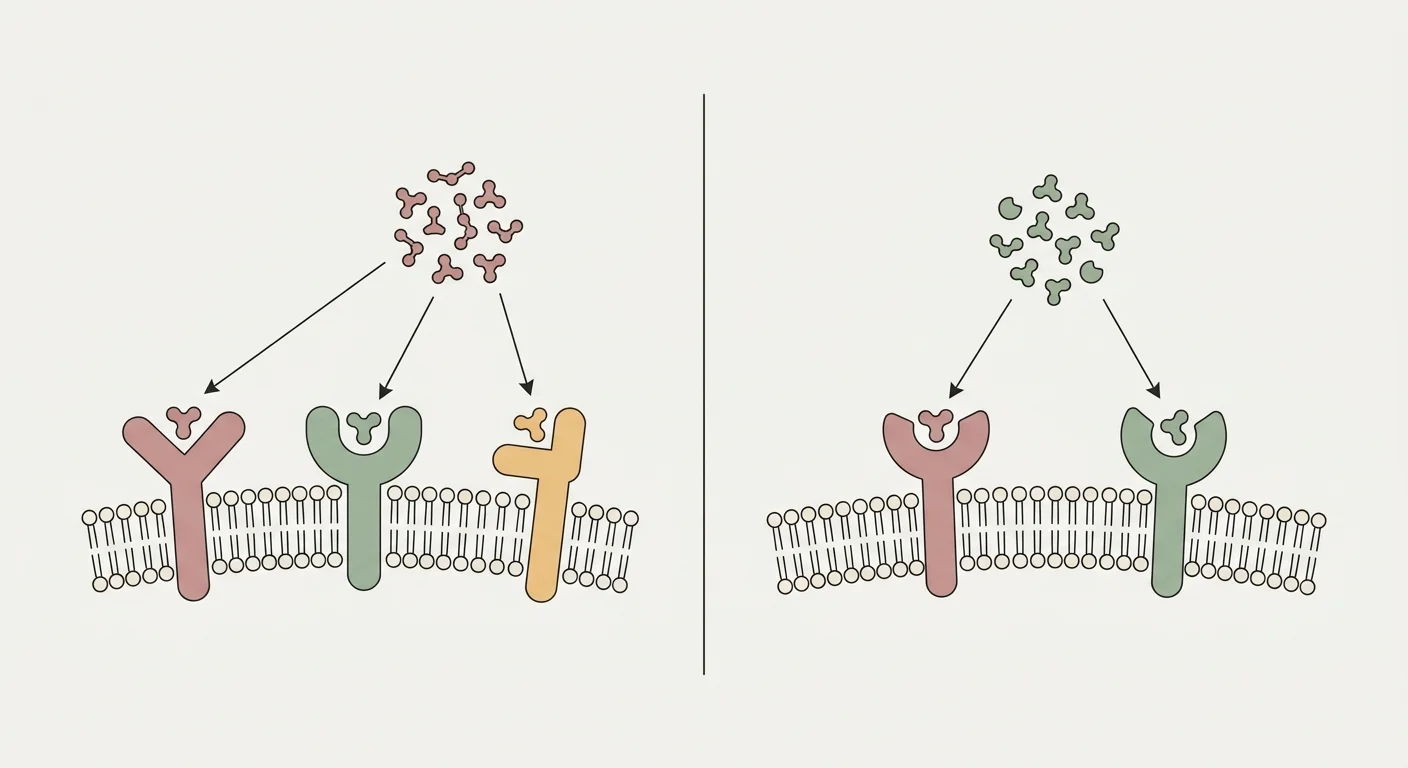
Le rétatrutide (LY3437943) est un peptide unique conçu pour activer simultanément trois récepteurs de la famille des incrétines : le récepteur du glucagon-like peptide-1 (GLP-1R), le récepteur du polypeptide insulinotrope dépendant du glucose (GIPR) et le récepteur du glucagon (GCGR) 26. Le bras GLP-1R commande la suppression centrale de l’appétit, le ralentissement de la vidange gastrique et la sécrétion d’insuline glucose-dépendante, déjà familiers grâce au sémaglutide et au tirzépatide 24. Le bras GIPR ajoute une activité insulinotrope synergique et, dans le tissu adipeux, améliore le tamponnage lipidique sain en réduisant le dépôt de graisse ectopique dans le foie et le muscle 25.
Le bras distinctif est GCGR. Le glucagon est habituellement présenté comme l’hormone contre-régulatrice qui élève la glycémie ; dans le contexte d’un triagoniste équilibré, son effet classique sur la production hépatique de glucose est compensé par l’action insulinotrope simultanée des récepteurs GLP-1R/GIPR, tandis que les effets métaboliques que les concepteurs de peptides recherchent réellement de GCGR sont préservés : augmentation de la dépense énergétique via la thermogenèse du tissu adipeux brun et l’oxydation musculaire squelettique, lipolyse adipeuse avec libération d’acides gras libres pour la bêta-oxydation, et oxydation hépatique des acides gras qui évacue les triglycérides du foie 27. Dans les données MASLD de phase 2a, le rétatrutide a produit environ 85 à 90 % de réduction de la graisse hépatique à la dose la plus élevée ; environ 90 % des participants à 12 mg ont atteint une graisse hépatique inférieure à 5 % à 48 semaines, une amplitude que le bi-agonisme n’a pas démontrée .
Aucun essai contrôlé randomisé direct rétatrutide contre tirzépatide n’a été publié ou annoncé en avril 2026. Un essai d’enregistrement face-à-face (NCT06662383) est visible sur le suivi de pipeline de Lilly, mais aucun résultat n’a été rapporté. Toute affirmation comparative de cet article comporte donc une réserve : il s’agit soit d’une comparaison indirecte entre essais différents par leurs populations, leurs schémas posologiques et leurs critères d’évaluation, soit d’une extrapolation mécanistique à partir de données précliniques et de phase 2. Ce n’est pas une raison pour ignorer le signal — c’est une raison pour le nuancer.
Deux méta-analyses en réseau ont tenté de placer les molécules sur la même échelle. L’analyse d’octobre 2025 publiée dans le Journal of the Endocrine Society (résumé SUN-659, avec article complet validé par les pairs sous PMC12544991) a rapporté pour le rétatrutide une réduction absolue moyenne de −16,34 kg et −23,77 % de poids corporel contre −11,82 kg et −16,79 % pour le tirzépatide, soit un avantage indirect en faveur du rétatrutide 20. La même analyse a signalé un risque relatif d’événements indésirables plus élevé pour le rétatrutide (RR 4,10 vs 2,78), cohérent avec un fardeau gastro-intestinal plus marqué aux doses les plus élevées. Une méta-analyse en réseau plus large portant sur sept agents, publiée dans Metabolism (2024), a classé les molécules pour la perte de poids dans l’ordre rétatrutide 12 mg > rétatrutide 8 mg > tirzépatide 15 mg, avec des classements concordants pour le tour de taille, l’HbA1c et la glycémie à jeun 21.
Les deux méta-analyses en réseau favorisent numériquement et directionnellement le rétatrutide, mais l’absence de preuves issues d’un ECR direct impose qu’une réserve accompagne toute affirmation comparative. À des fins de recherche, c’est un motif d’investigation supplémentaire, non une raison d’écarter le signal.
Le profil de sécurité de phase 2 est cohérent avec la classe des agonistes du récepteur GLP-1, dominé par des événements indésirables gastro-intestinaux dose-dépendants qui se concentrent durant la première à la deuxième semaine de chaque palier d'escalade. La sécurité de phase 3 (TRIUMPH-4) n'est disponible qu'à titre de résultats principaux par communiqué de presse en avril 2026 et n'a pas encore été validée par les pairs à la résolution complète des données.
Les résultats principaux de TRIUMPH-4 rapportent une réduction d'environ 28,7 % à 68 semaines, dépassant le pic SURMOUNT-1 du tirzépatide à 72 semaines d'environ six points de pourcentage. Les deux méta-analyses en réseau publiées vont dans le même sens.
Le bras GCGR ajoute des voies que le tirzépatide n'a pas : oxydation hépatique des acides gras (~85–90 % de réduction de la graisse hépatique en phase 2a MASLD), lipolyse adipeuse et dépense énergétique thermogénique.
Plus de douze essais de phase 3, trois autorisations FDA, un CVOT publié sur 13 165 patients, et une enveloppe de sécurité d'information posologique mature. La molécule de référence pour la recherche GLP-1/GIP aujourd'hui.
SURPASS-2 a battu le sémaglutide 1 mg en face-à-face sur l'HbA1c ; SURPASS-CVOT est le seul essai de morbi-mortalité cardiovasculaire publié pour l'une ou l'autre de ces molécules. Les preuves DT2 du rétatrutide demeurent en phase 2 (Rosenstock 2023).
Le tirzépatide est un agoniste bivalent de GLP-1R et GIPR ; le rétatrutide ajoute le récepteur du glucagon (GCGR) comme troisième cible 26. Le bras GCGR contribue à l’oxydation hépatique des acides gras, à la lipolyse adipeuse et à la dépense énergétique thermogénique que le bi-agonisme n’engage pas par conception 27.
Le tirzépatide, sans ambiguïté. Plus de douze essais de phase 3, trois autorisations FDA, et un essai de morbi-mortalité cardiovasculaire publié sur 13 165 patients 12. Le rétatrutide n’a qu’un résultat principal de phase 3 (TRIUMPH-4) et un programme de phase 2 comprenant environ six publications validées par les pairs 1 5. L’écart se réduira tout au long de 2026 à mesure que TRIUMPH-1, TRIUMPH-2 et TRIUMPH-3 livreront leurs résultats.
Non. Aucun ECR direct rétatrutide contre tirzépatide n’a été publié ou rapporté publiquement en avril 2026. Les preuves comparatives se limitent à deux méta-analyses en réseau indirectes, qui penchent toutes deux dans le sens du rétatrutide mais ne peuvent se substituer à un essai face-à-face .
Le rétatrutide est notre choix. Non parce qu’il dispose de plus de données d’essais — ce n’est pas le cas. Le programme de phase 3 du tirzépatide est plus profond de quatre années, ses trois autorisations FDA couvrent le diabète de type 2, la gestion chronique du poids et le syndrome d’apnée obstructive du sommeil, et son essai de morbi-mortalité cardiovasculaire publié sur plus de treize mille patients est un fait que nous ne contestons pas 12 28. Pour les protocoles de recherche qui ont besoin de la base de preuves la plus profonde et la mieux scrutée disponible aujourd’hui dans la classe incrétinique, le tirzépatide est la molécule de référence et le restera jusqu’à l’achèvement du programme TRIUMPH.
Mais pour les protocoles de recherche qui visent le plafond thérapeutique le plus élevé, les chiffres favorisent le rétatrutide. Son premier résultat de phase 3 a rapporté une réduction pondérale d’environ 28,7 % à 12 mg sur 68 semaines 5— un avantage de plafond significatif d’environ six points de pourcentage sur le pic SURMOUNT-1 du tirzépatide de 22,5 % sur 72 semaines 13. L’explication mécanistique n’est pas spéculative : le récepteur du glucagon ajoute l’oxydation hépatique des acides gras, la lipolyse adipeuse et la dépense énergétique thermogénique que le bi-agonisme ne peut pas engager par conception 27, et la réduction de 85 à 90 % de la graisse hépatique observée dans le résultat MASLD de phase 2a est une signature directe de cette voie 3. Les deux méta-analyses en réseau publiées vont dans le sens du rétatrutide 20 21. La base de preuves mûrira ; le plafond, par conception, ne descendra pas.
Pour la frontière de recherche en thérapie peptidique métabolique, le rétatrutide est le vainqueur. Pour les protocoles qui valorisent avant tout la profondeur de niveau réglementaire, le tirzépatide demeure le standard. C’est une division des rôles plus claire que ce que la plupart des comparaisons « X vs Y » peuvent offrir, et l’honnêteté quant à cette division est plus utile qu’un vainqueur unique forcé.
Présent ; ~85–90 % de réduction de la graisse hépatique en phase 2a MASLD 3
Absent par conception
~144 h (~6 jours)
~120 h (~5 jours)
1 résultat principal (TRIUMPH-4) ; TRIUMPH-1/2/3 en cours 4
12+ (SURPASS 1–6, CVOT, PEDS ; SURMOUNT 1–5, OSA)
Aucun (aucun CVOT lancé)
SURPASS-CVOT (n=13 165 ; NEJM déc. 2025) 12
Aucune (pas d'étiquette approuvée)
Cellules C thyroïdiennes MTC (rongeur, pertinence humaine non établie) 28
Aucun publié
Aucun publié
Hebdomadaire, sous-cutanée
Hebdomadaire, sous-cutanée
États-Unis : fin 2027 au plus tôt (NDA T4 2026 au plus tôt) 22
Déjà autorisé (États-Unis : 2022/2023/2024 ; UE : 2022/2024)
Lyophilisé ; reconstitution à l'eau bactériostatique ; 2–8 °C
Lyophilisé ; reconstitution à l'eau bactériostatique ; 2–8 °C
Plafond plus élevé + étendue du récepteur du glucagon
Plafond plus bas ; enveloppe de sécurité la mieux caractérisée
Le tirzépatide (LY3298176) est un agoniste bivalent GLP-1R / GIPR — un peptide unique de 39 résidus calibré pour engager les deux récepteurs incrétiniques avec une puissance comparable. Le bras GLP-1R apporte le même mécanisme central que celui de la première génération d’analogues du GLP-1 : sécrétion d’insuline glucose-dépendante, suppression du glucagon par les cellules alpha, régulation hypothalamique de l’appétit et ralentissement de la vidange gastrique 24.
Ce qui distingue le tirzépatide des agonistes GLP-1 purs, c’est l’activité GIPR additionnelle. En préclinique, la coadministration de GIP avec GLP-1 produit des réductions additives, voire synergiques sur certaines mesures, du poids corporel et de la glycémie, supérieures à chacun pris isolément 25. L’activation centrale de GIPR semble potentialiser l’anorexie induite par GLP-1 via la signalisation hypothalamique POMC ; l’activation périphérique de GIPR dans le tissu adipeux blanc accroît la capacité tampon du dépôt et réduit le besoin de stockage ectopique. La conséquence observable est le profil le plus puissant de réduction pondérale et glycémique de toute molécule autorisée avant le rétatrutide : SURMOUNT-1 a rapporté environ 22,5 % de réduction pondérale à la dose de 15 mg sur 72 semaines 13, et SURMOUNT-5 a montré la supériorité du tirzépatide sur le sémaglutide 2,4 mg en face-à-face à 72 semaines (−20,2 % vs −13,7 %) 18.
Le bras récepteur du glucagon est le différenciateur mécanistique du rétatrutide. Les données précliniques et de phase 2 suggèrent que cela se traduit par des effets hypolipémiants, réducteurs de la graisse hépatique et stimulants de la dépense énergétique que le tirzépatide, par conception, ne possède pas. Que cela se traduise ou non par l’avantage en comparaison directe sous-entendu par les méta-analyses en réseau restera ouvert jusqu’à ce qu’un ECR face-à-face livre ses résultats — ce qui, en avril 2026, n’a fait l’objet d’aucune annonce.
La profondeur des preuves du tirzépatide est aujourd’hui inégalée — douze essais de phase 3 sur deux programmes pathologiques, un essai de morbi-mortalité cardiovasculaire publié sur plus de treize mille patients, et trois autorisations FDA inscrites à l’étiquetage. Le résultat disponible pour le rétatrutide, bien que singulier, dépasse le meilleur plafond de phase 3 du tirzépatide sur une fenêtre d’observation plus courte. C’est un signal qui mérite une attention sérieuse à mesure que TRIUMPH-1, TRIUMPH-2 et TRIUMPH-3 mûriront en 2026 et 2027.
Enveloppe de sécurité d'information posologique mature pour Mounjaro et Zepbound. Les EI fréquents reflètent la classe GLP-1 et se concentrent à l'escalade de dose ; les risques graves sont saisis dans une mise en garde encadrée et un ensemble d'avertissements et précautions affinés par la pharmacovigilance post-commercialisation (analyse FAERS 2024 et pharmacovigilance EMA).
Cet article est une comparaison éditoriale rédigée pour des lecteurs en contexte de recherche. Ni le rétatrutide ni le tirzépatide ne sont proposés ou recommandés pour une auto-administration humaine via ce site. Lorsque le tirzépatide est prescrit, il n’est disponible que sous la supervision d’un médecin dans les juridictions où il a été autorisé (Mounjaro pour le DT2 ; Zepbound pour la gestion chronique du poids et le syndrome d’apnée obstructive du sommeil). Le rétatrutide est expérimental à l’échelle mondiale en avril 2026 et ne doit être manipulé que dans le cadre de protocoles de recherche appropriés.
Les données de sécurité résumées ici reflètent les ensembles de données publiés en phase 2 et phase 3 ainsi que les informations posologiques actuelles. De nouveaux signaux peuvent émerger à tout moment ; la date lastUpdated de cette page indique la limite de notre revue. Rien sur cette page ne constitue un avis médical ni un substitut à une consultation auprès d’un clinicien qualifié.
Le tirzépatide est autorisé sous deux noms commerciaux : Mounjaro pour le diabète de type 2 (FDA mai 2022) et Zepbound pour la gestion chronique du poids (novembre 2023) et le syndrome d’apnée obstructive du sommeil modéré à sévère avec obésité (décembre 2024) 28. Le rétatrutide est expérimental partout ; aucune NDA n’a été déposée en avril 2026 22.
Le rétatrutide, sur la base des données disponibles. TRIUMPH-4 a rapporté ~−28,7 % à 12 mg sur 68 semaines 5; le meilleur résultat de phase 3 obésité du tirzépatide, SURMOUNT-1 à 15 mg sur 72 semaines, a été d’environ −22,5 % 13. Les deux méta-analyses en réseau publiées classent le rétatrutide plus haut sur la réduction du poids corporel 20 21.
Au niveau de la classe, les deux présentent un profil à dominance gastro-intestinale (nausées, vomissements, diarrhée) qui se concentre à l’escalade de dose. La méta-analyse en réseau d’octobre 2025 a rapporté un risque relatif d’événements indésirables plus élevé pour le rétatrutide (RR 4,10) que pour le tirzépatide (RR 2,78), cohérent avec un fardeau gastro-intestinal supérieur aux doses les plus élevées 20. Le tirzépatide porte une mise en garde encadrée MTC et un profil caractérisé de pancréatite, d’affections vésiculaires et d’hypersensibilité 28 29; l’enveloppe de sécurité analogue à long terme du rétatrutide n’est pas établie.
Les essais de phase 2 et de phase 3 publiés pour les deux molécules recrutent en monothérapie (avec ou sans traitement de fond du DT2 tel que la metformine ou l’insuline). Aucune preuve publiée n’existe sur le cumul de l’une ou l’autre avec d’autres peptides de recherche. Tout protocole combinatoire est strictement expérimental et hors du cadre des preuves résumées dans cet article.
La demi-vie d’environ 144 heures du rétatrutide et celle d’environ 120 heures du tirzépatide soutiennent toutes deux une dose sous-cutanée hebdomadaire unique, le schéma utilisé dans chaque essai d’enregistrement. La demi-vie légèrement plus longue du rétatrutide procure une marge modeste face à la variabilité des doses manquées, mais ne modifie pas la cadence hebdomadaire fondamentale.
Oui. Le rétatrutide et le tirzépatide sont tous deux référencés à des fins de recherche dans les canaux UE et États-Unis. La disponibilité, les volumes de flacons et les tarifs spécifiques au canal figurent sur la page détail de chaque produit.
Les résultats de TRIUMPH-1 (obésité sans DT2), TRIUMPH-2 (obésité avec DT2) et TRIUMPH-3 (obésité avec maladie cardiovasculaire établie) sont attendus en 2026 selon les indications de Lilly 4. Chacun élargira matériellement la base de preuves du rétatrutide ; collectivement, ils détermineront si le plafond de TRIUMPH-4 se généralise à l’ensemble des populations et si un dépôt de NDA peut être avancé par rapport à la fenêtre actuelle T4 2026 au plus tôt.
Le rétatrutide l'emporte sur les dimensions qui comptent le plus pour la recherche de pointe : plafond observé plus élevé dans TRIUMPH-4, étendue mécanistique du triagonisme et direction concordante des deux méta-analyses en réseau publiées. Le tirzépatide demeure la molécule de référence pour les protocoles qui ont besoin de la base de preuves publiée la plus profonde aujourd'hui.