

Triplu-agonistul care a stabilit un nou plafon contra dublu-agonistului care a construit categoria. O comparație pentru protocoalele de cercetare care vor să înțeleagă ce moleculă reprezintă frontiera, care este standardul și de ce această distincție contează.

Tirzepatide (Mounjaro/Zepbound de la Eli Lilly) este un dublu agonist al receptorilor GLP-1/GIP, cu patru ani de date din faza 3, trei aprobări FDA și un studiu publicat privind rezultatele cardiovasculare. Retatrutide, molecula succesoare a Lilly, este un triplu agonist care adaugă receptorul de glucagon la aceeași schelă duală și, în primul său raport de fază 3, a produs cea mai profundă reducere ponderală raportată vreodată într-un studiu de înregistrare pentru obezitate: aproximativ 28,7% la 68 de săpt. 5 vs vârful tirzepatidului din SURMOUNT-1 de aproximativ 22,5% la 72 de săpt. 13.
Bazele de dovezi nu sunt simetrice. Tirzepatide are dosarul matur, evaluat colegial. Retatrutide are plafonul observat mai înalt, un profil de țintă mecanistic mai larg și două meta-analize de rețea care indică în direcția sa 20 21. Pentru protocoalele de cercetare care prioritizează plafonul terapeutic maxim și amploarea mecanistică, alegerea noastră editorială este retatrutide. Pentru protocoalele care apreciază profunzimea dovezilor de calitate reglementară și un profil de siguranță stabilizat, tirzepatide rămâne molecula de referință.
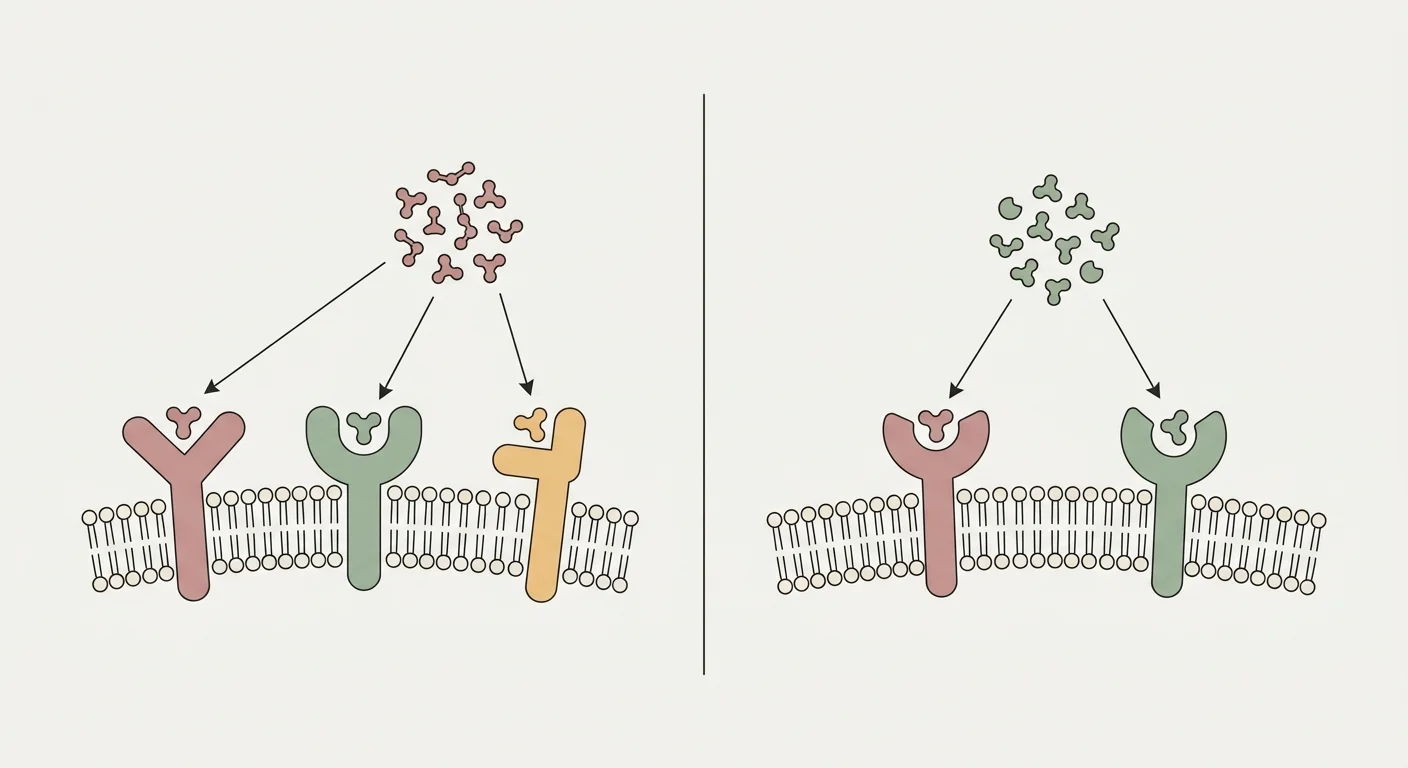
Retatrutide (LY3437943) este o singură peptidă proiectată să agonizeze simultan trei receptori din familia incretinelor: receptorul peptidei-1 asemănătoare glucagonului (GLP-1R), receptorul polipeptidei insulinotrope dependente de glucoză (GIPR) și receptorul de glucagon (GCGR) 26. Brațul GLP-1R determină supresia centrală a apetitului, întârzierea golirii gastrice și secreția de insulină dependentă de glucoză, familiare din semaglutid și tirzepatide 24. Brațul GIPR adaugă activitate insulinotropă sinergică și, în țesutul adipos, îmbunătățește tamponarea sănătoasă a lipidelor, reducând depunerea ectopică de grăsime în ficat și mușchi 25.
Brațul distinctiv este GCGR. Glucagonul este de obicei prezentat ca hormonul contra-reglator care crește glicemia; în contextul unui triplu agonist echilibrat, efectul său clasic asupra producției hepatice de glucoză este compensat de acțiunea insulinotropă simultană a GLP-1R/GIPR, în timp ce efectele metabolice pe care proiectanții de peptide le doresc de fapt din partea GCGR sunt păstrate: cheltuiala energetică crescută prin termogeneza adipoasă brună și oxidarea musculară scheletică, lipoliza adipoasă cu eliberare de acizi grași liberi pentru beta-oxidare și oxidarea hepatică a acizilor grași care eliberează ficatul de trigliceride 27. În datele de fază 2a MASLD, retatrutide a produs aproximativ 85–90% reducere a grăsimii hepatice la doza maximă; aproximativ 90% dintre participanții la 12 mg au atins o grăsime hepatică sub 5% la 48 de săptămâni, o magnitudine pe care dublu-agonismul nu a demonstrat-o 3.
Niciun studiu randomizat controlat direct retatrutide-versus-tirzepatide nu a fost publicat sau anunțat până în aprilie 2026. Un studiu de înregistrare cap-la-cap (NCT06662383) este vizibil în trackerul de pipeline al Lilly, însă niciun raport nu a fost transmis. Prin urmare, fiecare afirmație comparativă din acest articol poartă o avertizare: este fie o comparație indirectă între studii cu populații, scheme de dozare și criterii diferite, fie o extrapolare mecanistică pornind de la date preclinice și de fază 2. Acesta nu este un motiv pentru a ignora semnalul — este un motiv pentru a-l califica.
Două meta-analize de rețea au încercat să plaseze moleculele pe aceeași scară. Analiza din octombrie 2025, publicată în Journal of the Endocrine Society (rezumat SUN-659, cu articolul integral evaluat colegial la PMC12544991), a raportat retatrutide cu o reducere absolută medie de −16,34 kg și −23,77% greutate corporală vs −11,82 kg și −16,79% pentru tirzepatide, un avantaj indirect în favoarea retatrutidului 20. Aceeași analiză a semnalat un risc relativ mai mare pentru evenimentele adverse în cazul retatrutidului (RR 4,10 vs 2,78), în concordanță cu o sarcină gastrointestinală mai mare la dozele maxime. O meta-analiză de rețea mai amplă, cu șapte agenți, publicată în Metabolism (2024), a clasat moleculele pentru pierderea ponderală astfel: retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, cu clasamente consecvente pe circumferința taliei, HbA1c și glicemia plasmatică à jeun 21.
Ambele meta-analize de rețea favorizează retatrutide numeric și direcțional, însă absența dovezilor directe din RCT înseamnă că orice afirmație comparativă trebuie să poarte o avertizare. În scop de cercetare, acesta este un motiv pentru investigații suplimentare, nu un motiv pentru a respinge semnalul.
Profilul de siguranță din faza 2 este în concordanță cu clasa agoniștilor receptorului GLP-1, dominat de evenimente adverse gastrointestinale dependente de doză, care se concentrează în prima sau a doua săptămână a fiecărei trepte de escaladare. Siguranța din faza 3 (TRIUMPH-4) este disponibilă, începând cu aprilie 2026, doar ca raport preliminar prin comunicat de presă și nu a fost încă evaluată colegial la rezoluție de set complet de date.
Raportul preliminar TRIUMPH-4 indică o reducere de ~28,7% la 68 de săptămâni, depășind vârful tirzepatidului din SURMOUNT-1 la 72 de săptămâni cu aproximativ șase puncte procentuale. Ambele meta-analize de rețea publicate indică în aceeași direcție.
Brațul GCGR adaugă căi pe care tirzepatide nu le are: oxidarea hepatică a acizilor grași (~85–90% reducere a grăsimii hepatice în faza 2a MASLD), lipoliza adipoasă și cheltuiala energetică termogenică.
Peste douăsprezece studii de fază 3, trei aprobări FDA, un CVOT publicat la 13.165 de pacienți și un profil matur de siguranță în informațiile de prescriere. Molecula de referință pentru cercetarea GLP-1/GIP astăzi.
SURPASS-2 a învins semaglutidul 1 mg cap-la-cap la HbA1c; SURPASS-CVOT este singurul studiu publicat privind rezultatele cardiovasculare pentru oricare dintre cele două molecule. Dovezile pentru retatrutide în T2D rămân la nivel de fază 2 (Rosenstock 2023).
Tirzepatide, fără echivoc. Peste douăsprezece studii de fază 3, trei aprobări FDA și un studiu publicat privind rezultatele cardiovasculare la 13.165 de pacienți 12. Retatrutide are un singur raport preliminar de fază 3 (TRIUMPH-4) și un program de fază 2 cu aproximativ șase publicații evaluate colegial 1 5. Decalajul se va reduce în 2026, pe măsură ce TRIUMPH-1, TRIUMPH-2 și TRIUMPH-3 raportează rezultate.
Nu. Niciun RCT direct retatrutide-vs-tirzepatide nu a fost publicat sau raportat public începând cu aprilie 2026. Dovezile comparative se limitează la două meta-analize de rețea indirecte, ambele indicând în direcția retatrutidului, dar care nu pot înlocui un studiu cap-la-cap 20 .
Retatrutide este alegerea noastră. Nu pentru că ar avea mai multe date din studii — nu are. Programul de fază 3 al tirzepatidului este cu patru ani mai matur, cele trei aprobări FDA acoperă diabetul zaharat de tip 2, managementul cronic al greutății și apneea obstructivă în somn, iar studiul publicat privind rezultatele cardiovasculare la peste treisprezece mii de pacienți este un fapt pe care nu îl contestăm 12 28. Pentru protocoalele de cercetare care au nevoie de cea mai profundă și mai scrutinată bază de dovezi disponibilă astăzi în clasa incretinelor, tirzepatide este molecula de referință și va rămâne așa până la finalizarea programului TRIUMPH.
Dar pentru protocoalele de cercetare care urmăresc cel mai înalt plafon terapeutic, cifrele favorizează retatrutide. Primul său raport de fază 3 a indicat o reducere ponderală de aproximativ 28,7% la 12 mg pe parcursul a 68 de săptămâni 5— un avantaj de plafon semnificativ, de șase puncte procentuale, față de vârful tirzepatidului din SURMOUNT-1 de 22,5% pe parcursul a 72 de săptămâni 13. Explicația mecanistică nu este speculativă: receptorul de glucagon adaugă oxidarea hepatică a acizilor grași, lipoliza adipoasă și cheltuiala energetică termogenică pe care dublu-agonismul nu le poate angaja prin design 27, iar reducerea grăsimii hepatice de 85–90% din raportul de fază 2a MASLD este o semnătură directă a acestei căi 3. Ambele meta-analize de rețea publicate indică în direcția retatrutidului 20 21. Baza de dovezi se va maturiza; plafonul, prin design, nu va coborî.
Pentru frontiera de cercetare a terapiei cu peptide metabolice, retatrutide este câștigătorul. Pentru protocoalele care prețuiesc, mai presus de orice, profunzimea de calitate reglementară, tirzepatide rămâne standardul. Aceasta este o împărțire a rolurilor mai clară decât pot oferi majoritatea comparațiilor „X vs Y”, iar onestitatea în privința acestei împărțiri este mai utilă decât un câștigător unic forțat.
Prezent; ~85–90% reducere a grăsimii hepatice în faza 2a MASLD 3
Absent prin design
~144 h (~6 zile)
~120 h (~5 zile)
1 raport preliminar (TRIUMPH-4); TRIUMPH-1/2/3 în desfășurare 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Niciunul (CVOT neinițiat)
SURPASS-CVOT (n=13.165; NEJM dec. 2025) 12
Niciunul (fără etichetă aprobată)
Celule C tiroidiene MTC (rozătoare, relevanța la om nestabilită) 28
Niciunul publicat
Niciunul publicat
O dată pe săptămână, subcutanat
O dată pe săptămână, subcutanat
SUA: cel mai devreme la finalul lui 2027 (NDA cel mai devreme T4 2026) 22
Deja aprobat (SUA: 2022/2023/2024; UE: 2022/2024)
Liofilizat; reconstituire cu apă BAC; 2–8 °C
Liofilizat; reconstituire cu apă BAC; 2–8 °C
Plafon mai înalt + amploarea receptorului de glucagon
Plafon mai scăzut; cel mai bine caracterizat profil de siguranță
Tirzepatide (LY3298176) este un agonist dual GLP-1R/GIPR — o singură peptidă de 39 de reziduuri reglată să angajeze ambii receptori incretinici cu potență comparabilă. Brațul GLP-1R contribuie cu același mecanism central familiar din prima generație de analogi GLP-1: secreția de insulină dependentă de glucoză, supresia glucagonului din celulele alfa, reglarea hipotalamică a apetitului și încetinirea golirii gastrice 24.
Ceea ce diferențiază tirzepatide de agoniștii GLP-1 puri este activitatea suplimentară GIPR. Preclinic, co-administrarea de GIP cu GLP-1 produce reduceri aditive și, în unele măsurători, sinergice ale greutății corporale și glicemiei, mai mari decât oricare administrate singure 25. Activarea GIPR centrală pare să potențeze anorexia indusă de GLP-1 prin semnalizarea hipotalamică POMC; activarea GIPR periferică în țesutul adipos alb îmbunătățește capacitatea de tamponare a depozitului și reduce nevoia de depunere ectopică. Consecința observabilă este cel mai potent profil de scădere ponderală și glicemică al oricărei molecule aprobate înainte de retatrutide: SURMOUNT-1 a raportat o reducere ponderală de aproximativ 22,5% la doza de 15 mg pe parcursul a 72 de săptămâni 13, iar SURMOUNT-5 a arătat că tirzepatide este superior semaglutidului 2,4 mg cap-la-cap la 72 de săptămâni (−20,2% vs −13,7%) 18.
Brațul receptorului de glucagon este diferențiatorul mecanistic al retatrutidului. Datele preclinice și cele din faza 2 sugerează că acest lucru se traduce în efecte de scădere a lipidelor, de reducere a grăsimii hepatice și de cheltuieli energetice care lipsesc tirzepatidului prin design. Dacă acest lucru se va traduce în avantajul de comparație directă sugerat de meta-analizele de rețea va rămâne deschis până la raportarea unui RCT cap-la-cap — care, din aprilie 2026, nu a fost anunțat.
Profunzimea dovezilor pentru tirzepatide este astăzi neegalată — douăsprezece studii de fază 3 în două programe de boală, un studiu publicat privind rezultatele cardiovasculare la peste treisprezece mii de pacienți și trei aprobări FDA în etichetă. Raportul disponibil al retatrutidului, deși singular, depășește cel mai bun plafon din faza 3 al tirzepatidului într-o fereastră de observație mai scurtă. Acesta este un semnal care merită o atenție serioasă pe măsură ce TRIUMPH-1, TRIUMPH-2 și TRIUMPH-3 se maturizează pe parcursul lui 2026 și 2027.
Profil matur de siguranță în informațiile de prescriere pentru Mounjaro și Zepbound. Evenimentele adverse comune oglindesc clasa GLP-1 și se concentrează la escaladarea dozei; riscurile grave sunt surprinse într-un avertisment încadrat și un set de avertismente și precauții rafinate prin supraveghere post-marketing (analiza FAERS 2024 și farmacovigilența EMA).
Acest articol este o comparație editorială pregătită pentru cititori în context de cercetare. Nici retatrutide, nici tirzepatide nu sunt oferite sau recomandate pentru auto-administrare la om prin acest site. Acolo unde tirzepatide este prescris, este disponibil exclusiv sub supravegherea unui medic, în jurisdicțiile în care a fost aprobat (Mounjaro pentru T2D; Zepbound pentru managementul cronic al greutății și apneea obstructivă în somn). Retatrutide este investigațional la nivel global începând cu aprilie 2026 și ar trebui manipulat numai în cadrul unor protocoale de cercetare adecvate.
Datele de siguranță rezumate aici reflectă seturile de date publicate din fazele 2 și 3 și informațiile actuale de prescriere. Pot apărea semnale noi în orice moment; data lastUpdated de pe această pagină indică termenul-limită al evaluării noastre. Nimic din această pagină nu constituie sfat medical sau un substitut pentru consultarea unui medic calificat.
Tirzepatide este aprobat sub două nume comerciale: Mounjaro pentru diabetul zaharat de tip 2 (FDA mai 2022) și Zepbound pentru managementul cronic al greutății (noiembrie 2023) și apnee obstructivă moderată-severă în somn cu obezitate (decembrie 2024) 28. Retatrutide este investigațional pretutindeni; nicio NDA nu a fost depusă începând cu aprilie 2026 22.
Retatrutide, pe baza datelor disponibile. TRIUMPH-4 a raportat ~−28,7% la 12 mg pe parcursul a 68 de săptămâni 5; cel mai bun raport de fază 3 pentru obezitate al tirzepatidului, SURMOUNT-1 la 15 mg pe parcursul a 72 de săptămâni, a fost de ~−22,5% 13. Ambele meta-analize de rețea publicate clasează retatrutide mai sus la reducerea greutății corporale 20 21.
La nivel de clasă, ambele au un profil dominat gastrointestinal (greață, vărsături, diaree) care se concentrează la escaladarea dozei. Meta-analiza de rețea din octombrie 2025 a raportat un risc relativ mai mare al evenimentelor adverse pentru retatrutide (RR 4,10) decât pentru tirzepatide (RR 2,78), în concordanță cu o sarcină gastrointestinală mai mare la dozele maxime 20. Tirzepatide poartă un avertisment încadrat MTC și un profil caracterizat de pancreatită / vezică biliară / hipersensibilitate 28 29; profilul analog de siguranță pe termen lung al retatrutidului nu a fost stabilit.
Studiile de fază 2 și 3 publicate pentru ambele molecule includ pacienți în monoterapie (cu sau fără terapie de fond pentru T2D, cum ar fi metformina sau insulina). Nu există dovezi publicate privind combinarea oricăreia dintre ele cu alte peptide de cercetare. Orice protocol de combinație este strict investigațional și în afara bazei de dovezi rezumate în acest articol.
Timpul de înjumătățire de ~144 de ore al retatrutidului și cel de ~120 de ore al tirzepatidului susțin amândouă o singură doză săptămânală subcutanată, schema utilizată în fiecare studiu de înregistrare. Timpul de înjumătățire ușor mai lung al retatrutidului oferă o margine de siguranță modestă față de variabilitatea unei doze omise, dar nu modifică ritmul fundamental săptămânal.
Da. Atât retatrutide, cât și tirzepatide sunt listate pentru utilizare în cercetare în ambele canale, UE și SUA. Disponibilitatea, dimensiunile flacoanelor și prețurile specifice canalului sunt afișate pe pagina de detaliu a fiecărui produs.
Rapoartele TRIUMPH-1 (obezitate fără T2D), TRIUMPH-2 (obezitate cu T2D) și TRIUMPH-3 (obezitate cu boală cardiovasculară stabilită) sunt așteptate pe parcursul lui 2026, conform indicațiilor Lilly 4. Fiecare va extinde substanțial baza de dovezi a retatrutidului; împreună vor determina dacă plafonul TRIUMPH-4 se generalizează între populații și dacă o depunere NDA va fi devansată față de actuala fereastră, cel mai devreme T4 2026.
Retatrutide câștigă pe dimensiunile cele mai relevante pentru cercetarea de frontieră: plafon observat mai înalt în TRIUMPH-4, amploarea mecanistică triplu-agonistă și direcția consecventă în ambele meta-analize de rețea publicate. Tirzepatide rămâne molecula de referință pentru protocoalele care au nevoie astăzi de cea mai profundă bază de dovezi publicate.