

Trippelagonisten som satte ett nytt tak mot dubbelagonisten som byggde kategorin. En jämförelse för forskningsprotokoll som vill förstå vilken molekyl som är fronten, vilken som är standarden och varför skillnaden spelar roll.

Tirzepatide (Eli Lillys Mounjaro/Zepbound) är en dubbel GLP-1/GIP-receptoragonist med fyra års fas 3-data, tre FDA-godkännanden och en publicerad kardiovaskulär utfallsstudie. Retatrutide, Lillys uppföljarmolekyl, är en trippelagonist som lägger till glukagonreceptorn på samma dubbla grundstruktur och som i sin första fas 3-avläsning gav den djupaste viktminskning som någonsin rapporterats i en registreringsstudie för obesitas: omkring 28,7 % vid 68 veckor 5 mot tirzepatides SURMOUNT-1-topp på cirka 22,5 % vid 72 veckor 13.
Evidensbaserna är inte symmetriska. Tirzepatide har det mogna, expertgranskade underlaget. Retatrutide har det högre observerade taket, en mekanistiskt bredare målprofil och två nätverksmetaanalyser som pekar i dess riktning 20 21. För forskningsprotokoll som prioriterar maximalt terapeutiskt tak och mekanismbredd är vårt redaktionella val retatrutide. För protokoll som värdesätter regulatorisk evidensdjup och en fastställd säkerhetsetikett är tirzepatide fortfarande referensmolekylen.
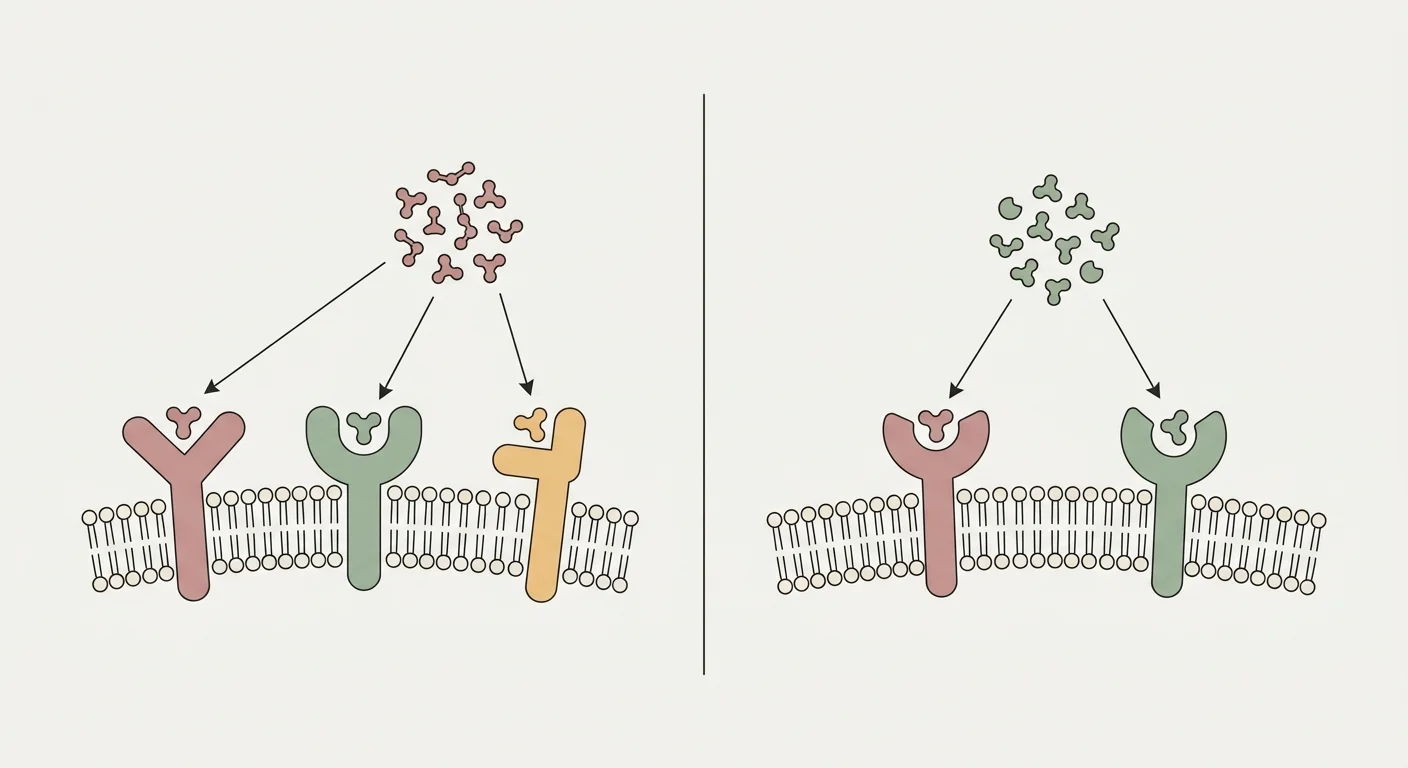
Retatrutide (LY3437943) är en enskild peptid konstruerad för att samtidigt agonisera tre receptorer i inkretinfamiljen: receptorn för glukagonliknande peptid-1 (GLP-1R), receptorn för glukosberoende insulinotropisk polypeptid (GIPR) och glukagonreceptorn (GCGR) 26. GLP-1R-armen driver den centrala aptitdämpningen, fördröjd ventrikeltömning och glukosberoende insulinfrisättning som vi känner igen från semaglutide och tirzepatide 24. GIPR-armen tillför synergistisk insulinotropisk aktivitet och förbättrar i fettväv den hälsosamma lipidbufferten, vilket minskar ektopisk fettinlagring i lever och muskulatur 25.
Den särskiljande armen är GCGR. Glukagon brukar beskrivas som det kontraregulatoriska hormonet som höjer blodsockret; i en balanserad trippelagonist motverkas dess klassiska effekt på hepatisk glukosproduktion av den samtidiga insulinotropiska GLP-1R/GIPR-aktiviteten, samtidigt som de metabola effekter peptiddesignerna faktiskt vill ha av GCGR bevaras: ökad energiomsättning via termogenes i brunt fett och oxidation i skelettmuskulatur, lipolys i fettväv med frigörelse av fria fettsyror för betaoxidation samt hepatisk fettsyraoxidation som rensar triglycerider ur levern 27. I fas 2a-data vid MASLD gav retatrutide ungefär 85–90 % minskning av leverfett vid högsta dosen; cirka 90 % av deltagarna på 12 mg nådde leverfett under 5 % vid 48 veckor, en storleksordning som dubbelagonism inte har visat 3.
Ingen direkt randomiserad kontrollerad studie av retatrutide mot tirzepatide har publicerats eller aviserats per april 2026. En registreringsstudie head-to-head (NCT06662383) syns i Lillys pipelineverktyg, men inget resultat har rapporterats. Varje jämförande påstående i denna artikel bär därför med sig ett förbehåll: det är antingen en indirekt jämförelse mellan studier med olika populationer, doseringsscheman och effektmått, eller en mekanistisk extrapolering från prekliniska data och fas 2-data. Det är inte ett skäl att ignorera signalen — det är ett skäl att kvalificera den.
Två nätverksmetaanalyser har försökt placera molekylerna på samma skala. Analysen från oktober 2025, publicerad i Journal of the Endocrine Society (abstract SUN-659, med fullständig expertgranskad artikel på PMC12544991), rapporterade retatrutide vid en absolut genomsnittlig minskning på −16,34 kg och −23,77 % kroppsvikt mot −11,82 kg och −16,79 % för tirzepatide, en indirekt fördel till retatrutides förmån 20. Samma analys flaggade en högre relativ risk för biverkningar för retatrutide (RR 4,10 mot 2,78), vilket stämmer överens med en högre gastrointestinal belastning vid de högsta doserna. En bredare nätverksmetaanalys över sju substanser, publicerad i Metabolism (2024), rangordnade molekylerna för viktminskning som retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, med konsekvent rangordning även för midjemått, HbA1c och fastande plasmaglukos 21.
Båda nätverksmetaanalyserna gynnar retatrutide numeriskt och riktningsmässigt, men avsaknaden av direkt RCT-evidens innebär att varje jämförande påstående måste bära ett förbehåll. För forskningsändamål är detta ett skäl till vidare undersökning, inte ett skäl att avfärda signalen.
Säkerhetsprofilen i fas 2 är förenlig med GLP-1-receptoragonistklassen och domineras av dosberoende gastrointestinala biverkningar som är koncentrerade till de första en till två veckorna i varje upptitreringssteg. Säkerhetsdata från fas 3 (TRIUMPH-4) finns per april 2026 endast tillgängliga som toppresultat i pressmeddelande och har ännu inte expertgranskats på fullständig datasetnivå.
TRIUMPH-4 toppresultat rapporterar ~28,7 % minskning vid 68 veckor, vilket överstiger tirzepatides SURMOUNT-1-topp vid 72 veckor med ungefär sex procentenheter. Båda publicerade nätverksmetaanalyser pekar i samma riktning.
GCGR-armen tillför vägar som tirzepatide saknar: hepatisk fettsyraoxidation (~85–90 % minskning av leverfett i fas 2a vid MASLD), lipolys i fettväv och termogen energiomsättning.
Tolv plus fas 3-studier, tre FDA-godkännanden, en publicerad CVOT med 13 165 patienter och en mogen säkerhetsprofil i förskrivarinformationen. Referensmolekylen för GLP-1/GIP-forskning idag.
SURPASS-2 slog semaglutide 1 mg head-to-head på HbA1c; SURPASS-CVOT är den enda publicerade kardiovaskulära utfallsstudien för någon av molekylerna. Retatrutides T2D-evidens är fortfarande på fas 2-nivå (Rosenstock 2023).
Tirzepatide, otvetydigt. Tolv plus fas 3-studier, tre FDA-godkännanden och en publicerad kardiovaskulär utfallsstudie med 13 165 patienter 12. Retatrutide har ett toppresultat från fas 3 (TRIUMPH-4) och ett fas 2-program på ungefär sex expertgranskade publikationer 1 5. Gapet kommer att minska under 2026 i takt med att TRIUMPH-1, TRIUMPH-2 och TRIUMPH-3 rapporterar.
Retatrutide är vårt val. Inte för att den har mer studiedata — det har den inte. Tirzepatides fas 3-program har fyra års försprång, dess tre FDA-godkännanden spänner över typ 2-diabetes, kronisk viktkontroll och obstruktiv sömnapné, och den publicerade kardiovaskulära utfallsstudien med över trettontusen patienter är ett faktum vi inte ifrågasätter 12 28. För forskningsprotokoll som behöver den djupaste, mest genomgranskade evidensbasen som finns tillgänglig i inkretinklassen idag är tirzepatide referensmolekylen och kommer att förbli det tills TRIUMPH-programmet är avslutat.
Men för forskningsprotokoll som strävar efter det högsta terapeutiska taket talar siffrorna för retatrutide. Den första fas 3-avläsningen rapporterade omkring 28,7 % viktminskning vid 12 mg över 68 veckor 5— en betydelsefull takfördel på sex procentenheter över tirzepatides SURMOUNT-1-topp på 22,5 % över 72 veckor 13. Den mekanistiska förklaringen är inte spekulativ: glukagonreceptorn tillför hepatisk fettsyraoxidation, lipolys i fettväv och termogen energiomsättning som dubbelagonism enligt sin design inte kan aktivera 27, och fas 2a-avläsningen vid MASLD med 85–90 % minskning av leverfett är en direkt signatur från den vägen 3. Båda publicerade nätverksmetaanalyser pekar i retatrutides riktning 20 21. Evidensbasen kommer att mogna; taket, enligt designen, kommer inte att sjunka.
För forskningsfronten inom metabol peptidterapi är retatrutide vinnaren. För protokoll som värdesätter regulatoriskt djup framför allt annat förblir tirzepatide standarden. Det är en tydligare uppdelning av roller än de flesta "X mot Y"-jämförelser kan erbjuda, och ärlighet om uppdelningen är mer användbar än en framtvingad ensam vinnare.
Retatrutide vinner på de dimensioner som spelar störst roll för forskning i framkant: högre observerat tak i TRIUMPH-4, bredd i trippelagonistens mekanism och samstämmig riktning i båda publicerade nätverksmetaanalyser. Tirzepatide förblir referensmolekylen för protokoll som behöver den djupaste publicerade evidensbasen idag.
Närvarande; ~85–90 % minskning av leverfett i fas 2a vid MASLD 3
Saknas i designen
~144 h (~6 dagar)
~120 h (~5 dagar)
1 toppresultat (TRIUMPH-4); TRIUMPH-1/2/3 pågår 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Saknas (ingen CVOT initierad)
SURPASS-CVOT (n=13 165; NEJM dec 2025) 12
Ingen (ingen godkänd etikett)
MTC-tyreoideans C-celler (gnagare, human relevans ej fastställd) 28
Ingen publicerad
Ingen publicerad
En gång per vecka, subkutant
En gång per vecka, subkutant
USA: tidigast slutet av 2027 (NDA Q4 2026 som tidigast) 22
Redan godkänd (USA: 2022/2023/2024; EU: 2022/2024)
Lyofiliserad; beredning med BAC-vatten; 2–8 °C
Lyofiliserad; beredning med BAC-vatten; 2–8 °C
Högre tak + glukagonreceptorbredd
Lägre tak; bäst karaktäriserad säkerhetsprofil
Tirzepatide (LY3298176) är en dubbel GLP-1R/GIPR-agonist — en enskild 39-aminosyrors peptid som är finstämd för att engagera båda inkretinreceptorerna med jämförbar potens. GLP-1R-armen bidrar med samma kärnmekanism som första generationens GLP-1-analoger: glukosberoende insulinfrisättning, glukagonsuppression i alfaceller, hypotalamisk aptitreglering och fördröjd ventrikeltömning 24.
Det som skiljer tirzepatide från rena GLP-1-agonister är den tillagda GIPR-aktiviteten. Prekliniskt ger samtidig administrering av GIP och GLP-1 additiva och i vissa avseenden synergistiska minskningar av kroppsvikt och glukos, mer än vad någondera ger ensam 25. Central GIPR-aktivering förefaller förstärka den GLP-1-inducerade anorexin via hypotalamisk POMC-signalering; perifer GIPR-aktivering i vit fettväv ökar depåns buffringskapacitet och minskar behovet av ektopisk inlagring. Den observerbara följden är den mest potenta vikt- och glukossänkande profilen hos någon molekyl som godkändes före retatrutide: SURMOUNT-1 rapporterade omkring 22,5 % viktminskning vid 15 mg-dosen över 72 veckor 13, och SURMOUNT-5 visade tirzepatide som överlägset semaglutide 2,4 mg head-to-head vid 72 veckor (−20,2 % mot −13,7 %) 18.
Glukagonreceptorarmen är retatrutides mekanistiska differentiator. Prekliniska data och fas 2-data tyder på att detta omsätts i lipidsänkande, leverfettminskande och energiomsättande effekter som tirzepatide enligt sin design saknar. Huruvida detta omsätts i den direkta jämförelsefördel som nätverksmetaanalyserna antyder förblir öppet tills en head-to-head-RCT rapporterar — och per april 2026 har ingen aviserats.
Tirzepatides evidensdjup är oöverträffat idag — tolv fas 3-studier över två sjukdomsprogram, en publicerad kardiovaskulär utfallsstudie med över trettontusen patienter och tre FDA-godkännanden på etiketten. Retatrutides tillgängliga avläsning är visserligen ensam i sitt slag, men överträffar tirzepatides bästa fas 3-tak vid ett kortare observationsfönster. Det är en signal värd att ta på allvar i takt med att TRIUMPH-1, TRIUMPH-2 och TRIUMPH-3 mognar fram under 2026 och 2027.
Mogen säkerhetsprofil i förskrivarinformationen för Mounjaro och Zepbound. Vanliga biverkningar speglar GLP-1-klassen och koncentreras till dosupptitrering; allvarliga risker fångas i en inramad varning samt en uppsättning varningar och försiktighetsåtgärder som förfinats genom övervakning efter marknadsintroduktion (FAERS-analys 2024 och EMA:s farmakovigilans).
Denna artikel är en redaktionell jämförelse framtagen för läsare i forskningssammanhang. Varken retatrutide eller tirzepatide erbjuds eller rekommenderas för självadministrering på människa via denna webbplats. Där tirzepatide förskrivs är det endast tillgängligt under läkares övervakning i jurisdiktioner där det har godkänts (Mounjaro för T2D; Zepbound för kronisk viktkontroll och obstruktiv sömnapné). Retatrutide är globalt under utredning per april 2026 och bör endast hanteras inom lämpliga forskningsprotokoll.
Säkerhetsdata som sammanfattas här återspeglar publicerade fas 2- och fas 3-dataset samt aktuell förskrivarinformation. Nya signaler kan dyka upp när som helst; datumet lastUpdated på denna sida anger tidsgränsen för vår granskning. Inget på denna sida utgör medicinsk rådgivning eller en ersättning för konsultation med en kvalificerad kliniker.
Tirzepatide är godkänd under två varumärken: Mounjaro för typ 2-diabetes (FDA maj 2022) och Zepbound för kronisk viktkontroll (november 2023) samt måttlig till svår obstruktiv sömnapné vid obesitas (december 2024) 28. Retatrutide är under utredning överallt; ingen NDA har lämnats in per april 2026 22.
Retatrutide, baserat på tillgängliga data. TRIUMPH-4 rapporterade ~−28,7 % vid 12 mg över 68 veckor 5; tirzepatides bästa fas 3-avläsning vid obesitas, SURMOUNT-1 vid 15 mg över 72 veckor, var ~−22,5 % 13. Båda publicerade nätverksmetaanalyser rangordnar retatrutide högre på minskning av kroppsvikt 20 21.
På klassnivå har båda en GI-dominerad profil (illamående, kräkningar, diarré) som koncentreras vid dosupptitrering. Nätverksmetaanalysen från oktober 2025 rapporterade en högre relativ risk för biverkningar för retatrutide (RR 4,10) än för tirzepatide (RR 2,78), vilket stämmer överens med högre GI-belastning vid högsta doserna 20. Tirzepatide bär en inramad MTC-varning och en karaktäriserad profil för pankreatit, gallblåsa och överkänslighet 28 29; retatrutides motsvarande långsiktiga säkerhetsprofil har ännu inte fastställts.
Publicerade fas 2- och fas 3-studier för båda molekylerna inkluderar deltagare i monoterapi (med eller utan grundläggande T2D-behandling såsom metformin eller insulin). Det finns ingen publicerad evidens för stapling av någondera tillsammans med andra forskningspeptider. Varje kombinationsprotokoll är strikt under utredning och utanför evidensbasen som sammanfattas i denna artikel.
Retatrutides halveringstid på cirka 144 timmar och tirzepatides på cirka 120 timmar stödjer båda en enskild veckodos subkutant, schemat som använts i samtliga registreringsstudier. Den något längre halveringstiden för retatrutide ger en blygsam buffert mot variabilitet vid missad dos men ändrar inte den grundläggande veckokadensen.
Ja. Både retatrutide och tirzepatide finns listade för forskningsbruk i både EU- och USA-kanalen. Tillgänglighet, vialstorlekar och kanalspecifik prissättning visas på respektive produkts detaljsida.
Resultaten från TRIUMPH-1 (obesitas utan T2D), TRIUMPH-2 (obesitas med T2D) och TRIUMPH-3 (obesitas med etablerad kardiovaskulär sjukdom) väntas under 2026 enligt Lillys vägledning 4. Var och en kommer på ett påtagligt sätt att utöka retatrutides evidensbas; tillsammans avgör de om TRIUMPH-4-taket håller över olika populationer och om en NDA-inlämning kan tidigareläggas från det nuvarande tidigaste fönstret i Q4 2026.