

Tripel-agonisten, der satte et nyt loft, mod dual-agonisten, der opbyggede kategorien. En sammenligning til forskningsprotokoller, der ønsker at forstå, hvilket molekyle der er på fronten, hvilket der er standarden, og hvorfor sondringen betyder noget.

Tirzepatide (Eli Lillys Mounjaro/Zepbound) er en dual GLP-1/GIP-receptoragonist med fire års Fase 3-data, tre FDA-godkendelser og et publiceret kardiovaskulært outcome-studie. Retatrutide, Lillys efterfølgermolekyle, er en tripel-agonist, der tilføjer glukagonreceptoren til den samme duale rygrad og i sin første Fase 3-aflæsning producerede den dybeste vægtreduktion, der nogensinde er rapporteret i et registreringsstudie for fedme: omkring 28,7 % efter 68 uger 5 mod tirzepatides SURMOUNT-1-top på cirka 22,5 % efter 72 uger 13.
Evidensgrundlagene er ikke symmetriske. Tirzepatide har den modne, peer-reviewede sag. Retatrutide har det højere observerede loft, en mekanistisk bredere målprofil og to netværks- metaanalyser, der peger i dets retning 20 21. For forskningsprotokoller, der prioriterer maksimalt terapeutisk loft og mekanistisk bredde, er vores redaktionelle valg retatrutide. For protokoller, der vægter evidensdybde i regulatorisk kvalitet og en afklaret sikkerhedsetiket, forbliver tirzepatide referencemolekylet.
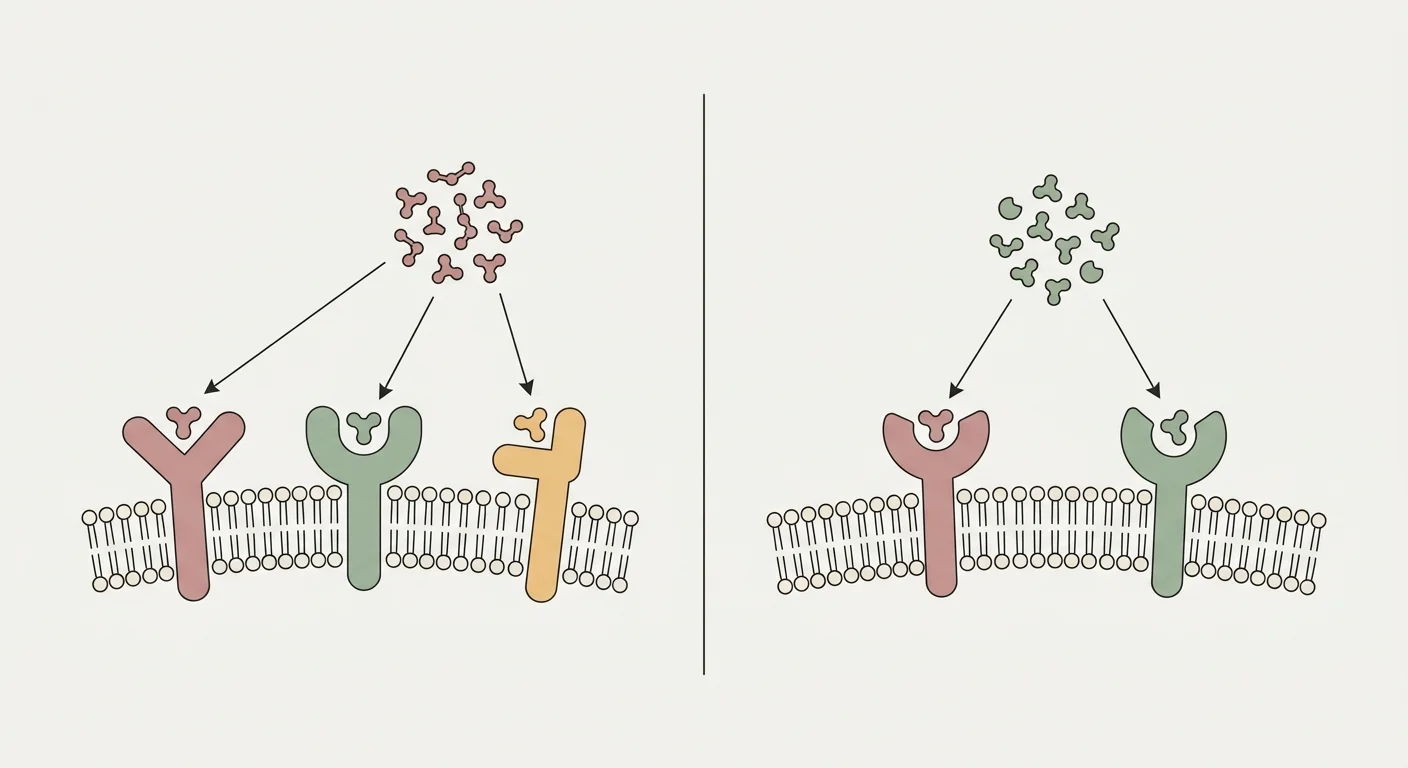
Retatrutide (LY3437943) er et enkelt peptid, designet til at agonisere tre receptorer i incretin-familien på én gang: glukagon-lignende peptid-1-receptoren (GLP-1R), den glukoseafhængige insulinotrope polypeptidreceptor (GIPR) og glukagonreceptoren (GCGR) 26. GLP-1R-armen driver den centrale appetitundertrykkelse, forsinket ventrikeltømning og glukoseafhængige insulinsekretion, der er kendt fra semaglutide og tirzepatide 24. GIPR-armen tilføjer synergistisk insulinotrop aktivitet og forbedrer i fedtvæv den sunde lipidbuffring, hvilket reducerer ektopisk fedtaflejring i lever og muskel 25.
Den særegne arm er GCGR. Glukagon fremstilles normalt som det modregulerende hormon, der hæver blodglukose; i konteksten af en afbalanceret tripel-agonist opvejes dets klassiske virkning på hepatisk glukoseproduktion af den samtidige GLP-1R/GIPR-insulinotrope effekt, mens de metaboliske virkninger, som peptiddesignere faktisk ønsker fra GCGR, bevares: øget energiforbrug via brun-fedtvævs-termogenese og skeletmuskeloxidation, fedtvævslipolyse med frigivelse af frie fedtsyrer til betaoxidation, og hepatisk fedtsyreoxidation, der fjerner triglycerid fra leveren 27. I Fase 2a MASLD-data producerede retatrutide cirka 85–90 % reduktion i leverfedt ved den højeste dosis; omkring 90 % af deltagerne i 12 mg-armen nåede leverfedt under 5 % efter 48 uger, en størrelsesorden som dual-agonisme ikke har påvist 3.
Intet direkte randomiseret kontrolleret studie af retatrutide mod tirzepatide er publiceret eller annonceret pr. april 2026. Ét registreringsstudie head-to-head (NCT06662383) er synligt i Lillys pipeline-tracker, men ingen aflæsning er rapporteret. Enhver komparativ påstand i denne artikel bærer derfor en forbehold: enten er det en indirekte sammenligning på tværs af studier med forskellige populationer, doseringsregimer og endepunkter, eller også er det en mekanistisk ekstrapolation fra prækliniske og Fase 2-data. Det er ikke en grund til at ignorere signalet — det er en grund til at kvalificere det.
To netværks-metaanalyser har forsøgt at placere molekylerne på samme skala. Analysen fra oktober 2025, publiceret i Journal of the Endocrine Society (abstract SUN-659, med fuld peer-reviewet artikel på PMC12544991), rapporterede retatrutide ved en gennemsnitlig absolut reduktion på −16,34 kg og −23,77 % kropsvægt mod −11,82 kg og −16,79 % for tirzepatide, en indirekte fordel til retatrutides side 20. Samme analyse markerede en højere relativ risiko for bivirkninger for retatrutide (RR 4,10 vs 2,78), foreneligt med en højere gastrointestinal byrde ved de højeste doser. En bredere syv-agent netværks-metaanalyse, publiceret i Metabolism (2024), rangerede molekylerne for vægttab som retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, med konsistente rangeringer på tværs af taljemål, HbA1c og fasteplasmaglukose 21.
Begge netværks-metaanalyser favoriserer retatrutide numerisk og retningsmæssigt, men fraværet af direkte RCT-evidens betyder, at enhver komparativ påstand må bære et forbehold. Til forskningsformål er dette en grund til yderligere undersøgelse, ikke en grund til at afvise signalet.
Fase 2-sikkerhedsprofilen er forenelig med GLP-1-receptoragonistklassen, domineret af dosisafhængige gastrointestinale bivirkninger, der koncentreres i den første eller anden uge af hvert optitreringstrin. Fase 3-sikkerhed (TRIUMPH-4) er kun tilgængelig som top-line via pressemeddelelse pr. april 2026 og er endnu ikke peer-reviewet i fuld datasæt-opløsning.
TRIUMPH-4 top-line rapporterer ~28,7 % reduktion efter 68 uger, hvilket overgår tirzepatides SURMOUNT-1-top efter 72 uger med cirka seks procentpoint. Begge publicerede netværks-metaanalyser peger i samme retning.
GCGR-armen tilføjer veje, som tirzepatide mangler: hepatisk fedtsyreoxidation (~85–90 % leverfedtsreduktion i Fase 2a MASLD), fedtvævslipolyse og termogent energiforbrug.
Tolv+ Fase 3-studier, tre FDA-godkendelser, et publiceret CVOT i 13.165 patienter, og en moden sikkerhedsenvelope på produktresumé-niveau. Referencemolekylet for GLP-1/GIP-forskning i dag.
SURPASS-2 slog semaglutide 1 mg head-to-head på HbA1c; SURPASS-CVOT er det eneste publicerede kardiovaskulære outcome-studie for nogen af molekylerne. Retatrutides T2D-evidens forbliver Fase 2 (Rosenstock 2023).
Tirzepatide, utvetydigt. Tolv+ Fase 3-studier, tre FDA-godkendelser og et publiceret kardiovaskulært outcome-studie i 13.165 patienter 12. Retatrutide har én Fase 3 top-line (TRIUMPH-4) og et Fase 2-program på cirka seks peer-reviewede publikationer 1 5. Forskellen vil indsnævres gennem 2026, efterhånden som TRIUMPH-1, TRIUMPH-2 og TRIUMPH-3 læser ud.
Retatrutide er vores valg. Ikke fordi det har flere studiedata — det har det ikke. Tirzepatides Fase 3-program er fire år dybere, dets tre FDA-godkendelser dækker type 2-diabetes, kronisk vægthåndtering og obstruktiv søvnapnø, og dets publicerede kardiovaskulære outcome-studie i mere end tretten tusinde patienter er en kendsgerning, vi ikke bestrider 12 28. For forskningsprotokoller, der har brug for det dybeste, mest gennemgranskede evidensgrundlag, der er tilgængeligt i incretinklassen i dag, er tirzepatide referencemolekylet og vil forblive det, indtil TRIUMPH-programmet er afsluttet.
Men for forskningsprotokoller, der forfølger det højeste terapeutiske loft, favoriserer tallene retatrutide. Dets første Fase 3-aflæsning rapporterede cirka 28,7 % vægtreduktion ved 12 mg over 68 uger 5— en meningsfuld loftsfordel på seks procentpoint i forhold til tirzepatides SURMOUNT-1-top på 22,5 % over 72 uger 13. Den mekanistiske forklaring er ikke spekulativ: glukagonreceptoren tilføjer hepatisk fedtsyreoxidation, fedtvævslipolyse og termogent energiforbrug, som dual-agonisme efter design ikke kan engagere 27, og Fase 2a MASLD-aflæsningens 85–90 % leverfedtsreduktion er en direkte signatur af den vej 3. Begge publicerede netværks-metaanalyser peger i retatrutides retning 20 21. Evidensgrundlaget vil modnes; loftet vil efter design ikke flytte sig nedad.
For den metaboliske peptidterapis forskningsfront er retatrutide vinderen. For protokoller, der vægter regulatorisk kvalitetsdybde over alt andet, forbliver tirzepatide standarden. Det er en klarere arbejdsdeling, end de fleste »X vs Y«-sammenligninger kan tilbyde, og ærlighed om delingen er mere nyttig end en tvungen enkelt vinder.
Retatrutide vinder på de dimensioner, der betyder mest for forskning på fronten: højere observeret loft i TRIUMPH-4, tripel-agonistisk mekanistisk bredde, og konsistent retning på tværs af begge publicerede netværks-metaanalyser. Tirzepatide forbliver referencemolekylet for protokoller, der har brug for det dybeste publicerede evidensgrundlag i dag.
Til stede; ~85–90 % leverfedtsreduktion i Fase 2a MASLD 3
Fraværende efter design
~144 t (~6 dage)
~120 t (~5 dage)
1 top-line (TRIUMPH-4); TRIUMPH-1/2/3 afventer 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Ingen (intet CVOT igangsat)
SURPASS-CVOT (n=13.165; NEJM dec. 2025) 12
Ingen (ingen godkendt etiket)
MTC thyroidea C-celle (gnaver, human relevans uafklaret) 28
Ingen publiceret
Ingen publiceret
En gang ugentligt, subkutant
En gang ugentligt, subkutant
USA: tidligst sent 2027 (NDA Q4 2026 tidligst) 22
Allerede godkendt (USA: 2022/2023/2024; EU: 2022/2024)
Lyofiliseret; rekonstitution med BAC-vand; 2–8 °C
Lyofiliseret; rekonstitution med BAC-vand; 2–8 °C
Højere loft + glukagonreceptor-bredde
Lavere loft; bedst karakteriserede sikkerhedsenvelope
Tirzepatide (LY3298176) er en dual GLP-1R / GIPR-agonist — et enkelt 39-aminosyrers peptid, justeret til at engagere begge incretinreceptorer med sammenlignelig potens. GLP-1R-armen bidrager med den samme kernemekanisme, der er kendt fra første generation af GLP-1-analoger: glukoseafhængig insulinsekretion, alfa-celle-glukagonsuppression, hypothalamisk appetitregulering og forsinket ventrikeltømning 24.
Det, der adskiller tirzepatide fra rene GLP-1-agonister, er den tilføjede GIPR-aktivitet. Præklinisk producerer samtidig administration af GIP med GLP-1 additive og på visse mål synergistiske reduktioner i kropsvægt og glukose, mere end hver for sig 25. Central GIPR-aktivering ser ud til at potensere GLP-1-induceret anoreksi via hypothalamisk POMC-signalering; perifer GIPR-aktivering i hvidt fedtvæv øger depotets bufferkapacitet og reducerer behovet for ektopisk aflejring. Den observerbare konsekvens er den mest potente vægt- og glukosesænkende profil for noget molekyle godkendt før retatrutide: SURMOUNT-1 rapporterede cirka 22,5 % vægtreduktion ved 15 mg-dosis over 72 uger 13, og SURMOUNT-5 viste tirzepatide overlegen i forhold til semaglutide 2,4 mg head-to-head efter 72 uger (−20,2 % vs −13,7 %) 18.
Glukagonreceptor-armen er retatrutides mekanistiske differentiator. Prækliniske og Fase 2-data tyder på, at dette omsættes til lipidsænkende, leverfedtsreducerende og energiforbrugsøgende virkninger, som tirzepatide efter design mangler. Hvorvidt dette omsættes til den direkte-sammenligningsfordel, som netværks-metaanalyserne antyder, forbliver åbent, indtil et head-to-head RCT læser ud — hvilket pr. april 2026 ikke er annonceret.
Tirzepatides evidensdybde er uden sidestykke i dag — tolv Fase 3-studier på tværs af to sygdomsprogrammer, et publiceret kardiovaskulært outcome-studie i mere end tretten tusinde patienter, og tre FDA-godkendelser på etiketten. Retatrutides foreliggende aflæsning, omend enkeltstående, overgår tirzepatides bedste Fase 3-loft ved et kortere observationsvindue. Det er et signal, der fortjener seriøs opmærksomhed, efterhånden som TRIUMPH-1, TRIUMPH-2 og TRIUMPH-3 modnes gennem 2026 og 2027.
Moden sikkerhedsenvelope på produktresumé-niveau på tværs af Mounjaro og Zepbound. Almindelige bivirkninger afspejler GLP-1-klassen og koncentreres ved dosisoptitrering; alvorlige risici er fanget i en boxed warning og et sæt advarsler og forsigtighedsregler, forfinet gennem post-marketing-overvågning (FAERS-analyse 2024 og EMA-pharmakovigilans).
Denne artikel er en redaktionel sammenligning udarbejdet til læsere i forskningskontekst. Hverken retatrutide eller tirzepatide tilbydes eller anbefales til menneskelig selv-administration via dette site. Hvor tirzepatide ordineres, er det udelukkende tilgængeligt under en lægelig overvågning i jurisdiktioner, hvor det er godkendt (Mounjaro til T2D; Zepbound til kronisk vægthåndtering og obstruktiv søvnapnø). Retatrutide er forsøgsmæssig globalt pr. april 2026 og bør kun håndteres inden for passende forskningsprotokoller.
Sikkerhedsdata, der er opsummeret her, afspejler publicerede Fase 2- og Fase 3-datasæt og aktuel produktinformation. Nye signaler kan dukke op til enhver tid; lastUpdated-datoen på denne side angiver skæringsdatoen for vores gennemgang. Intet på denne side udgør medicinsk rådgivning eller en erstatning for konsultation med en kvalificeret kliniker.
På klasseniveau har begge en GI-domineret profil (kvalme, opkastning, diarré), der koncentreres ved dosisoptitrering. Netværks-metaanalysen fra oktober 2025 rapporterede en højere relativ risiko for bivirkninger for retatrutide (RR 4,10) end for tirzepatide (RR 2,78), foreneligt med højere GI-byrde ved de højeste doser 20. Tirzepatide bærer en boxed MTC-advarsel og en karakteriseret pankreatitis- / galdeblære- / overfølsomhedsprofil 28 29; retatrutides analoge langtidssikkerhedsenvelope er ikke etableret.
Publicerede Fase 2- og Fase 3-studier for begge molekyler indrullerer som monoterapi (med eller uden T2D-baggrundsbehandling som metformin eller insulin). Der er ingen publiceret evidens om stabling af nogen af dem med andre forskningspeptider. Enhver kombinationsprotokol er strengt forsøgsmæssig og uden for evidensgrundlaget, der er opsummeret i denne artikel.
Retatrutides ~144-timers halveringstid og tirzepatides ~120-timers halveringstid understøtter begge en enkelt ugentlig subkutan dosis, det skema, der anvendes i ethvert registreringsstudie. Den lidt længere halveringstid for retatrutide giver en moderat buffer mod variabilitet ved glemte doser, men ændrer ikke den grundlæggende ugentlige kadence.
Ja. Både retatrutide og tirzepatide er listet til forskningsbrug i både EU- og US-kanalen. Tilgængelighed, hætteglasstørrelser og kanalspecifik prissætning vises på hvert produkts detaljeside.
Aflæsningerne af TRIUMPH-1 (fedme uden T2D), TRIUMPH-2 (fedme med T2D) og TRIUMPH-3 (fedme med etableret kardiovaskulær sygdom) forventes igennem 2026 ifølge Lillys vejledning 4. Hver vil væsentligt udvide retatrutides evidensgrundlag; samlet vil de afgøre, om TRIUMPH-4-loftet generaliserer på tværs af populationer, og om en NDA-indgivelse rykker frem fra det nuværende tidligste vindue i Q4 2026.