

Trostruki agonist koji je postavio novu gornju granicu, suprotstavljen dvostrukom agonistu koji je izgradio kategoriju. Usporedba namijenjena istraživačkim protokolima koji žele razumjeti koja je molekula granica, koja je standard i zašto je ta razlika važna.

Tirzepatid (Mounjaro/Zepbound tvrtke Eli Lilly) dvostruki je agonist GLP-1/GIP receptora s četiri godine podataka iz faze 3, tri odobrenja FDA-e i objavljenim ispitivanjem kardiovaskularnih ishoda. Retatrutid, Lillyjeva nasljedna molekula, trostruki je agonist koji istoj dvostrukoj okosnici dodaje glukagonski receptor te je u prvom čitanju faze 3 ostvario najdublje smanjenje tjelesne težine ikada zabilježeno u registracijskom ispitivanju pretilosti: oko 28,7 % nakon 68 tj. 5 u odnosu na vrhunac tirzepatida iz studije SURMOUNT-1 od približno 22,5 % nakon 72 tj. 13.
Baze dokaza nisu simetrične. Tirzepatid ima zreo, recenzirani slučaj. Retatrutid ima viši izmjereni vrhunac, mehanistički širi profil meta i dvije mrežne meta-analize koje govore u njegovu korist 20 21. Za istraživačke protokole kojima je prioritet maksimalan terapijski plafon i širina mehanizma, naš urednički izbor je retatrutid. Za protokole koji cijene regulatorno potkrijepljenu dubinu dokaza i utvrđenu sigurnosnu dokumentaciju, tirzepatid ostaje referentna molekula.
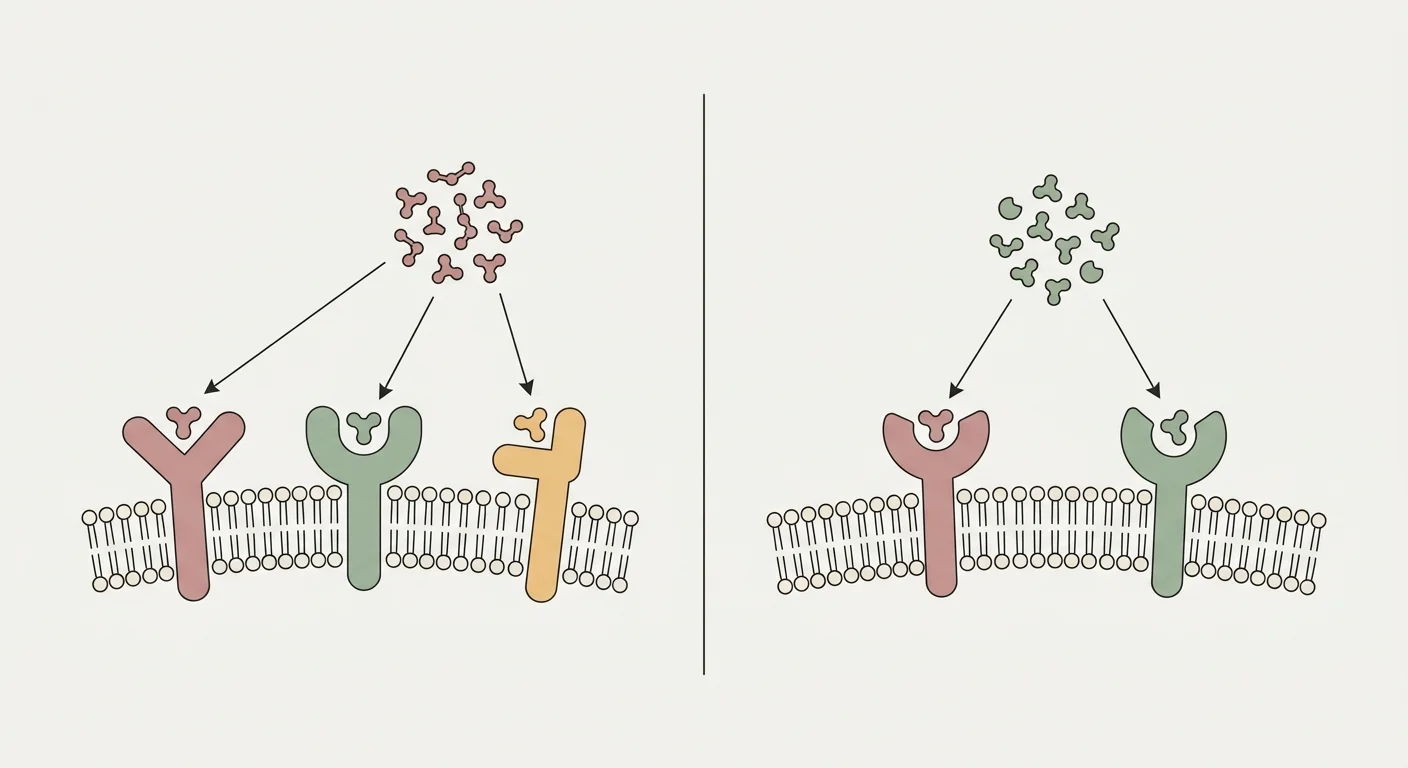
Retatrutid (LY3437943) jedinstveni je peptid dizajniran tako da istodobno agonizira tri receptora iz porodice inkretina: receptor za peptid sličan glukagonu-1 (GLP-1R), receptor za inzulinotropni polipeptid ovisan o glukozi (GIPR) i glukagonski receptor (GCGR) 26. Krak GLP-1R pokreće središnju supresiju apetita, usporeno pražnjenje želuca i o glukozi ovisno izlučivanje inzulina, mehanizme dobro poznate iz semaglutida i tirzepatida 24. Krak GIPR doprinosi sinergističnom inzulinotropnom djelovanju, a u masnom tkivu pojačava zdravo puferiranje lipida čime smanjuje ektopično odlaganje masti u jetri i mišićima 25.
Razlikovni krak je GCGR. Glukagon se uobičajeno opisuje kao kontraregulatorni hormon koji povisuje glukozu u krvi; u kontekstu uravnoteženog trostrukog agonista njegov klasični učinak na hepatičku proizvodnju glukoze poništen je istodobnim inzulinotropnim djelovanjem GLP-1R/GIPR, dok se zadržavaju metabolički učinci koje dizajneri peptida zaista žele od GCGR-a: povećana energetska potrošnja kroz termogenezu smeđeg masnog tkiva i oksidaciju u skeletnoj muskulaturi, lipoliza u masnom tkivu uz oslobađanje slobodnih masnih kiselina za beta-oksidaciju te hepatička oksidacija masnih kiselina koja iz jetre uklanja trigliceride 27. U podacima iz faze 2a kod MASLD-a retatrutid je u najvišoj dozi proizveo otprilike 85–90 % smanjenja masnoće jetre; nakon 48 tjedana oko 90 % sudionika na 12 mg postiglo je razinu masnoće jetre ispod 5 %, što je veličina koju dvostruki agonizam nije pokazao 3.
Prema stanju u travnju 2026., nije objavljeno niti najavljeno nijedno izravno randomizirano kontrolirano ispitivanje retatrutida i tirzepatida. Registracijsko izravno usporedno ispitivanje (NCT06662383) vidljivo je u Lillyjevu pregledu portfelja, ali rezultati nisu prijavljeni. Svaka usporedna tvrdnja u ovom članku stoga nosi ogradu: ili je riječ o neizravnoj usporedbi između ispitivanja s različitim populacijama, rasporedima doziranja i ishodima, ili o mehanističkoj ekstrapolaciji iz pretkliničkih podataka i podataka faze 2. To nije razlog da se signal zanemari — razlog je da ga se kvalificira.
Dvije mrežne meta-analize pokušale su molekule postaviti na istu mjernu skalu. Analiza objavljena u listopadu 2025. u časopisu Journal of the Endocrine Society (sažetak SUN-659, s recenziranim cjelovitim člankom u PMC12544991) prijavila je za retatrutid prosječno apsolutno smanjenje od −16,34 kg i −23,77 % tjelesne težine, naspram −11,82 kg i −16,79 % za tirzepatid, što ukazuje na neizravnu prednost retatrutida 20. Ista analiza upozorila je na viši relativni rizik nepoželjnih događaja za retatrutid (RR 4,10 prema 2,78), u skladu s većim probavnim opterećenjem pri najvišim dozama. Šira mrežna meta-analiza sa sedam sredstava objavljena u časopisu Metabolism (2024.) rangirala je molekule po gubitku težine kao retatrutid 12 mg > retatrutid 8 mg > tirzepatid 15 mg, uz dosljedne plasmane po opsegu struka, HbA1c i glukozi natašte 21.
Obje mrežne meta-analize numerički i smjerno favoriziraju retatrutid, ali izostanak izravnih dokaza iz randomiziranih ispitivanja znači da svaka usporedna tvrdnja mora nositi ogradu. Za istraživačke svrhe to je razlog za daljnje ispitivanje, a ne razlog za odbacivanje signala.
Sigurnosni profil iz faze 2 dosljedan je profilu klase agonista GLP-1 receptora i dominiraju mu nuspojave probavnog sustava ovisne o dozi koje su koncentrirane u prvim do drugim tjednima svake titracijske stepenice. Sigurnosni podaci faze 3 (TRIUMPH-4) prema stanju u travnju 2026. dostupni su samo kao vodeći nalaz iz priopćenja za javnost te još nisu recenzirani u rezoluciji cjelovitog skupa podataka.
Vodeći rezultati TRIUMPH-4 izvještavaju o ~28,7 % smanjenja nakon 68 tjedana, što vrhunac tirzepatida iz studije SURMOUNT-1 nakon 72 tjedna nadmašuje za otprilike šest postotnih bodova. Obje objavljene mrežne meta-analize idu u istom smjeru.
Krak GCGR dodaje putove koji tirzepatidu nedostaju: hepatička oksidacija masnih kiselina (~85–90 % smanjenja masnoće jetre u fazi 2a kod MASLD-a), lipoliza masnog tkiva i termogena potrošnja energije.
Više od dvanaest ispitivanja faze 3, tri odobrenja FDA-e, objavljeni CVOT na 13.165 pacijenata i zrela sigurnosna omotnica iz informacija o propisivanju. Danas referentna molekula za istraživanja GLP-1/GIP-a.
SURPASS-2 je u izravnoj usporedbi nadmašio semaglutid 1 mg po HbA1c; SURPASS-CVOT je jedino objavljeno ispitivanje kardiovaskularnih ishoda za bilo koju od dviju molekula. Dokazi o retatrutidu kod T2DM-a još su u fazi 2 (Rosenstock 2023.).
Tirzepatid, nedvojbeno. Više od dvanaest ispitivanja faze 3, tri odobrenja FDA-e i objavljeno ispitivanje kardiovaskularnih ishoda na 13.165 pacijenata 12. Retatrutid ima jedan vodeći nalaz iz faze 3 (TRIUMPH-4) i program faze 2 s otprilike šest recenziranih publikacija 1 5. Razmak će se kroz 2026. smanjivati kako budu izlazili rezultati TRIUMPH-1, TRIUMPH-2 i TRIUMPH-3.
Ne. Prema stanju u travnju 2026. nije objavljeno niti javno prijavljeno nijedno izravno randomizirano kontrolirano ispitivanje retatrutida i tirzepatida. Usporedni dokazi ograničeni su na dvije neizravne mrežne meta-analize, koje obje idu u smjeru retatrutida, ali ne mogu zamijeniti izravno usporedno ispitivanje 20 .
Naš izbor je retatrutid. Ne zato što ima više podataka iz ispitivanja — nema. Tirzepatidov program faze 3 dublji je za četiri godine, njegova tri odobrenja FDA-e pokrivaju dijabetes tipa 2, kronično upravljanje težinom i opstruktivnu apneju u snu, a njegovo objavljeno ispitivanje kardiovaskularnih ishoda na više od trinaest tisuća pacijenata činjenica je koju ne osporavamo 12 28. Za istraživačke protokole kojima je potrebna najdublja, najpomnije ispitana baza dokaza dostupna danas u klasi inkretina, tirzepatid je referentna molekula i to će ostati dok se ne dovrši program TRIUMPH.
No za istraživačke protokole koji teže najvišem terapijskom plafonu, brojke govore u prilog retatrutida. Njegov prvi nalaz iz faze 3 prijavio je oko 28,7 % smanjenja tjelesne težine pri 12 mg tijekom 68 tjedana 5— značajna prednost u plafonu od šest postotnih bodova nad vrhuncem tirzepatida iz studije SURMOUNT-1 od 22,5 % tijekom 72 tjedna 13. Mehanističko obrazloženje nije spekulativno: glukagonski receptor dodaje hepatičku oksidaciju masnih kiselina, lipolizu masnog tkiva i termogenu potrošnju energije koje dvostruki agonizam po dizajnu ne može aktivirati 27, a 85–90 % smanjenja masnoće jetre iz nalaza faze 2a kod MASLD-a izravan je potpis tog puta 3. Obje objavljene mrežne meta-analize govore u prilog retatrutida 20 21. Baza dokaza će sazrijevati; plafon, po dizajnu, neće se spustiti.
Za istraživačku granicu metaboličke peptidne terapije, retatrutid je pobjednik. Za protokole koji iznad svega cijene regulatornu dubinu, tirzepatid ostaje standard. To je jasnija podjela uloga nego što je nudi većina usporedbi tipa „X u odnosu na Y”, a iskrenost o toj podjeli korisnija je od prisilno proglašenog jedinog pobjednika.
Prisutan; ~85–90 % smanjenja masnoće jetre u fazi 2a MASLD 3
Po dizajnu odsutan
~144 h (~6 dana)
~120 h (~5 dana)
1 vodeći nalaz (TRIUMPH-4); TRIUMPH-1/2/3 u tijeku 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Nijedno (CVOT nije pokrenut)
SURPASS-CVOT (n=13.165; NEJM, prosinac 2025.) 12
Nijedno (nema odobrene deklaracije)
MTC C-stanice štitnjače (glodavci, ljudska relevantnost neutvrđena) 28
Nije objavljeno
Nije objavljeno
Jednom tjedno, supkutano
Jednom tjedno, supkutano
SAD: najranije kraj 2027. (NDA najranije Q4 2026.) 22
Već odobren (SAD: 2022./2023./2024.; EU: 2022./2024.)
Liofiliziran; rekonstitucija s BAC vodom; 2–8 °C
Liofiliziran; rekonstitucija s BAC vodom; 2–8 °C
Viši plafon i širina glukagonskog receptora
Niži plafon; najbolje karakterizirana sigurnosna omotnica
Tirzepatid (LY3298176) dvostruki je agonist GLP-1R / GIPR — jedinstveni peptid od 39 ostataka ugođen tako da angažira oba inkretinska receptora s usporedivim afinitetom. Krak GLP-1R doprinosi istovjetnim ključnim mehanizmima poznatima iz prve generacije analoga GLP-1: o glukozi ovisno izlučivanje inzulina, supresija glukagona iz alfa-stanica, hipotalamička regulacija apetita i usporeno pražnjenje želuca 24.
Ono što tirzepatid izdvaja od čistih agonista GLP-1 jest dodano djelovanje na GIPR. Pretklinički, istodobna primjena GIP-a i GLP-1 daje aditivna, a u nekim mjerama i sinergistička smanjenja tjelesne težine i glukoze, veća nego što ih daje pojedinačno 25. Čini se da središnja aktivacija GIPR-a potencira anoreksiju izazvanu GLP-1 putem hipotalamičke POMC signalizacije; periferna aktivacija GIPR-a u bijelom masnom tkivu pojačava puferski kapacitet depoa i smanjuje potrebu za ektopičnim odlaganjem. Vidljiva posljedica jest najpotentniji profil sniženja težine i glukoze među svim molekulama odobrenim prije retatrutida: SURMOUNT-1 zabilježio je smanjenje tjelesne težine od približno 22,5 % pri dozi od 15 mg tijekom 72 tjedna 13, a SURMOUNT-5 u izravnoj je usporedbi nakon 72 tjedna pokazao tirzepatid superiornijim u odnosu na semaglutid 2,4 mg (−20,2 % u odnosu na −13,7 %) 18.
Krak glukagonskog receptora mehanistički je razlikovni element retatrutida. Pretklinički podaci i podaci faze 2 sugeriraju da se to odražava u učincima na lipide, smanjenju masnoće jetre i potrošnji energije koje tirzepatid po dizajnu nema. Hoće li se to prevesti u prednost u izravnoj usporedbi koju nagovještavaju mrežne meta-analize, ostat će otvoreno pitanje sve do objave izravnog usporednog ispitivanja — a takvo, prema stanju u travnju 2026., još nije najavljeno.
Dubina dokaza o tirzepatidu danas nema premca — dvanaest ispitivanja faze 3 u dvama programima bolesti, objavljeno ispitivanje kardiovaskularnih ishoda na više od trinaest tisuća pacijenata i tri odobrenja FDA-e na deklaraciji. Iako pojedinačan, dostupan rezultat retatrutida nadmašuje najbolji plafon tirzepatida iz faze 3, i to u kraćem prozoru promatranja. Riječ je o signalu koji zaslužuje ozbiljnu pozornost dok TRIUMPH-1, TRIUMPH-2 i TRIUMPH-3 sazrijevaju kroz 2026. i 2027.
Zrela sigurnosna omotnica iz informacija o propisivanju, kroz Mounjaro i Zepbound. Uobičajene nuspojave odražavaju klasu GLP-1 i koncentriraju se pri titraciji doze; ozbiljni rizici obuhvaćeni su upozorenjem u okviru i nizom upozorenja i mjera opreza usavršenih kroz postmarketinški nadzor (analiza FAERS 2024. i farmakovigilancija EMA-e).
Ovaj članak urednička je usporedba pripremljena za čitatelje u istraživačkom kontekstu. Ni retatrutid ni tirzepatid ne nude se niti se preporučuju za samostalnu primjenu u ljudi putem ove stranice. Tamo gdje se tirzepatid propisuje, dostupan je isključivo pod nadzorom liječnika u jurisdikcijama u kojima je odobren (Mounjaro za T2DM; Zepbound za kronično upravljanje težinom i opstruktivnu apneju u snu). Retatrutid je prema stanju u travnju 2026. u cijelom svijetu istraživački te ga treba rukovati isključivo unutar prikladnih istraživačkih protokola.
Ovdje sažeti sigurnosni podaci odražavaju objavljene skupove podataka iz faze 2 i faze 3 te trenutne informacije o propisivanju. Novi signali mogu se pojaviti u svakom trenutku; datum lastUpdated na ovoj stranici označava granicu naše procjene. Ništa na ovoj stranici ne predstavlja medicinski savjet niti zamjenu za savjetovanje s kvalificiranim liječnikom.
Tirzepatid je odobren pod dva zaštitna naziva: Mounjaro za dijabetes tipa 2 (FDA, svibanj 2022.) i Zepbound za kronično upravljanje težinom (studeni 2023.) i umjerenu do tešku opstruktivnu apneju u snu uz pretilost (prosinac 2024.) 28. Retatrutid je posvuda istraživački; prema stanju u travnju 2026. NDA još nije podnesen 22.
Retatrutid, prema dostupnim podacima. TRIUMPH-4 zabilježio je ~−28,7 % pri 12 mg tijekom 68 tjedana 5; najbolji rezultat tirzepatida iz faze 3 kod pretilosti, SURMOUNT-1 pri 15 mg tijekom 72 tjedna, iznosio je ~−22,5 % 13. Obje objavljene mrežne meta-analize svrstavaju retatrutid više po smanjenju tjelesne težine 20 21.
Na razini klase obje molekule imaju profil s prevladavajućim probavnim nuspojavama (mučnina, povraćanje, proljev) koje se koncentriraju pri titraciji doze. Mrežna meta-analiza iz listopada 2025. zabilježila je viši relativni rizik nepoželjnih događaja za retatrutid (RR 4,10) nego za tirzepatid (RR 2,78), u skladu s većim probavnim opterećenjem pri najvišim dozama 20. Tirzepatid nosi upozorenje u okviru za MTC i karakteriziran profil pankreatitisa, oboljenja žučnog mjehura i preosjetljivosti 28 29; analogna dugoročna sigurnosna omotnica za retatrutid još nije utvrđena.
Objavljena ispitivanja faze 2 i faze 3 za obje molekule uključuju ispitanike u monoterapiji (sa ili bez prateće terapije T2DM-a poput metformina ili inzulina). Ne postoje objavljeni dokazi o kombiniranju s drugim istraživačkim peptidima. Bilo koji kombinacijski protokol strogo je istraživački i izvan baze dokaza koja je sažeta u ovom članku.
Retatrutidovo poluvrijeme od ~144 sata i tirzepatidovo poluvrijeme od ~120 sati podržavaju jednu tjednu supkutanu dozu, što je raspored upotrijebljen u svakom registracijskom ispitivanju. Nešto duže poluvrijeme retatrutida pruža skroman međuprostor uz varijabilnost propuštene doze, ali ne mijenja temeljni jednokratni tjedni ritam.
Da. Retatrutid i tirzepatid navedeni su za istraživačku upotrebu u EU i SAD kanalu. Dostupnost, veličine bočica i cijene specifične za pojedini kanal prikazane su na pojedinačnoj stranici proizvoda.
Prema Lillyjevim smjernicama tijekom 2026. očekuju se nalazi TRIUMPH-1 (pretilost bez T2DM-a), TRIUMPH-2 (pretilost s T2DM-om) i TRIUMPH-3 (pretilost s utvrđenom kardiovaskularnom bolešću) 4. Svaki od njih bitno će proširiti bazu dokaza o retatrutidu; zajedno će odrediti hoće li se plafon iz TRIUMPH-4 generalizirati po populacijama i hoće li se podnošenje NDA-e pomaknuti ranije od trenutačno najranijeg prozora Q4 2026.
Retatrutid pobjeđuje na dimenzijama koje su najvažnije za istraživanja na granici područja: viši izmjereni plafon u TRIUMPH-4, širina mehanizma trostrukog agonista i dosljedan smjer u objema objavljenim mrežnim meta-analizama. Tirzepatid ostaje referentna molekula za protokole kojima je potrebna najdublja danas objavljena baza dokaza.