Retatrutide: Was die Forschung zeigt
Dr. Sieglinde Klaus
Tudományos szerkesztés · Bergdorf Bioscience

Tartalomjegyzék
- 01Was ist Retatrutide und wie unterscheidet es sich von Semaglutid?
- 02Wie wirkt der Triple-Agonismus?
- 03Was zeigt die Phase-2-Studie zum Gewichtsverlust?
- 04Welche Ergebnisse gibt es bei Typ-2-Diabetes?
- 05Was zeigt die Forschung zur Fettleber (MASLD)?
- 06Wie verändert sich die Körperzusammensetzung?
- 07Welche Dosierungen wurden klinisch getestet?
- 08Häufig gestellte Fragen (FAQ)
- Ist Retatrutide für den therapeutischen Einsatz zugelassen?
- Worin unterscheidet sich Retatrutide von Tirzepatid?
- Wie wird Retatrutide korrekt gelagert?
- Welche Phase-3-Studien laufen aktuell zu Retatrutide?
- 09Haftungsausschluss
- 10Quellen und Attribution
Retatrutide (LY3437943) ist der erste Triple-Agonist, der gleichzeitig GIP-, GLP-1- und Glucagon-Rezeptoren aktiviert. In der zentralen Phase-2-Studie, publiziert im New England Journal of Medicine (2023), erreichten Teilnehmende unter der höchsten Dosis einen mittleren Gewichtsverlust von −24,2 % nach 48 Wochen — das stärkste bisher in einer randomisierten, kontrollierten Studie publizierte Ergebnis für ein einzelnes Molekül. Damit übertrifft Retatrutide sowohl Semaglutid (Wegovy®, circa 15 %) als auch Tirzepatid (Mounjaro®, circa 22 %). Der folgende Leitfaden fasst sechs klinische Studien zusammen, verlinkt jede Aussage auf die zugehörige PubMed-Quelle und ordnet die Ergebnisse in den aktuellen Forschungsstand ein. Alle Angaben beziehen sich ausschließlich auf die präklinische und klinische Forschungsliteratur; Retatrutide ist derzeit nicht für den therapeutischen Einsatz am Menschen zugelassen und wird ausschließlich als Forschungssubstanz angeboten.
Was ist Retatrutide und wie unterscheidet es sich von Semaglutid?
Retatrutide (LY3437943) ist ein von Eli Lilly entwickeltes Peptid, das als einziges Molekül drei Inkretinrezeptoren gleichzeitig anspricht: den glukoseabhängigen insulinotropen Polypeptid-Rezeptor (GIPR), den Glucagon-like-Peptide-1-Rezeptor (GLP-1R) und den Glucagon-Rezeptor (GCGR). Semaglutid — bekannt unter den Handelsnamen Ozempic® und Wegovy® — ist ein reiner GLP-1-Rezeptoragonist und erzielt in Phase-3-Studien einen mittleren Gewichtsverlust von etwa 15 %. Tirzepatid (Mounjaro®/Zepbound®) kombiniert GLP-1- und GIP-Agonismus und erreicht rund 22 %. Retatrutide ergänzt diese beiden Mechanismen um den Glucagon-Rezeptor, was in präklinischen Modellen eine gesteigerte Thermogenese und eine beschleunigte hepatische Lipidoxidation bewirkte. Die erste Humanstudie von Urva et al. (2022) bestätigte die Sicherheit und dosisabhängige Wirksamkeit bei übergewichtigen Erwachsenen mit einem günstigen pharmakokinetischen Profil (Lancet 2022; DOI: 10.1016/S0140-6736(22)02033-5).
Wie wirkt der Triple-Agonismus?
Der therapeutische Vorteil von Retatrutide beruht auf dem synergistischen Zusammenspiel dreier Signalwege. Die GIP-Komponente stimuliert die Insulinsekretion in Abhängigkeit vom Blutglukosespiegel und fördert über Adipozyten-Rezeptoren den Fettabbau im weißen Fettgewebe. Die GIP-vermittelte Insulinfreisetzung ist glukoseabhängig, wodurch das Hypoglykämie-Risiko minimiert wird. Der GLP-1-Agonismus verlangsamt die Magenentleerung, verstärkt das zentrale Sättigungssignal im Hypothalamus und verbessert die postprandiale Glukoseregulation — Mechanismen, die von reinen GLP-1-Rezeptoragonisten wie Semaglutid bereits umfassend charakterisiert sind. Die entscheidende dritte Komponente — der Glucagon-Rezeptoragonismus — erhöht den Grundumsatz über hepatische Thermogenese und steigert die Fettsäure-β-Oxidation in der Leber signifikant. In präklinischen Modellen reduzierte die Glucagon-Aktivierung den Leberfettgehalt um mehr als 80 %. Dieses dreifache Zusammenspiel erklärt, warum Retatrutide in klinischen Studien sowohl den Gewichtsverlust als auch die metabolischen Begleitparameter deutlich stärker verbessert als Mono- oder Dualagonisten allein.

Was zeigt die Phase-2-Studie zum Gewichtsverlust?
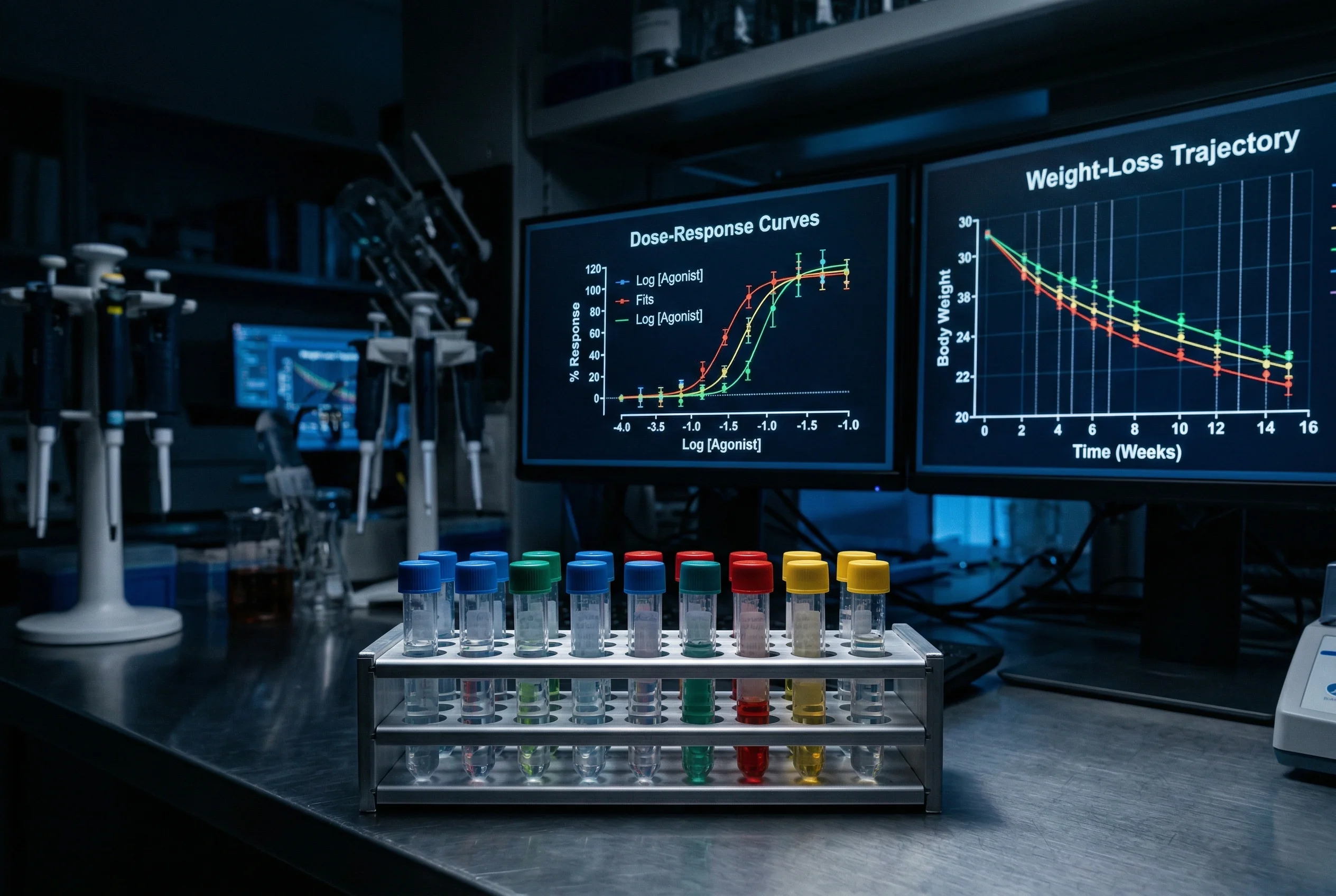
Die zentrale Wirksamkeitsstudie wurde von Jastreboff et al. (2023) im New England Journal of Medicine veröffentlicht. An der randomisierten, doppelblinden, placebokontrollierten Studie nahmen 338 Erwachsene mit Adipositas (BMI ≥ 30) oder Übergewicht (BMI ≥ 27 mit mindestens einer gewichtsassoziierten Komorbidität) teil. Die Teilnehmenden erhielten über 48 Wochen Retatrutide in Dosierungen von 1 mg bis 12 mg einmal wöchentlich als subkutane Injektion oder ein entsprechendes Placebo. In der höchsten Dosisgruppe (12 mg) betrug der mittlere Gewichtsverlust −24,2 % gegenüber Baseline; bereits nach 24 Wochen lag dieser Wert bei beeindruckenden −17,5 %. Besonders bemerkenswert: 72 % der Teilnehmenden mit Prädiabetes erreichten eine Normoglykämie. Die Abbruchrate war niedrig, und gastrointestinale Nebenwirkungen — vorwiegend Übelkeit und Durchfall — waren überwiegend mild bis moderat und vorübergehend (NEJM 2023; DOI: 10.1056/NEJMoa2301972).
Welche Ergebnisse gibt es bei Typ-2-Diabetes?
Parallel zur Adipositas-Studie untersuchten Rosenstock et al. (2023) die Wirksamkeit und Sicherheit von Retatrutide bei 281 Erwachsenen mit Typ-2-Diabetes mellitus in einer separaten randomisierten Phase-2-Studie. Die Ergebnisse, publiziert in The Lancet, zeigten eine dosisabhängige Reduktion des HbA1c-Wertes: In der 12-mg-Gruppe sank der HbA1c um durchschnittlich 2,02 Prozentpunkte gegenüber Baseline, wobei ein Großteil der Teilnehmenden den klinisch relevanten Zielwert von unter 7,0 % erreichte. Gleichzeitig wurde ein substantieller Gewichtsverlust von bis zu −16,9 % beobachtet — ein Wert, der bei Patientinnen und Patienten mit Typ-2-Diabetes typischerweise geringer ausfällt als bei nicht-diabetischer Adipositas. Das Sicherheitsprofil entsprach dem bekannter GLP-1-Rezeptoragonisten; schwerwiegende Hypoglykämien traten nicht auf. Diese vielversprechenden Ergebnisse positionieren Retatrutide als Kandidaten für die gleichzeitige Behandlung von Adipositas und Typ-2-Diabetes (Lancet 2023; DOI: 10.1016/S0140-6736(23)01053-X).
Was zeigt die Forschung zur Fettleber (MASLD)?
Die metabolisch assoziierte steatotische Lebererkrankung (MASLD, früher als NAFLD bezeichnet) betrifft geschätzt 30 % der Weltbevölkerung und stellt einen unabhängigen kardiovaskulären Risikofaktor dar. Hartman et al. (2024) untersuchten in einer präspezifizierten Sub-Studie mit 98 Teilnehmenden die Wirkung von Retatrutide auf den Leberfettgehalt, gemessen mittels MRT-basierter Protonendichte-Fettfraktion (MRI-PDFF). Nach 48 Wochen reduzierte die 12-mg-Dosis den Leberfettgehalt um beeindruckende −82,4 % relativ zur Baseline. 86 % der Teilnehmenden in dieser Dosisgruppe erreichten eine vollständige Normalisierung des Leberfettgehalts auf unter 5 %. Diese herausragende Wirkung wird maßgeblich der Glucagon-Rezeptor-Komponente zugeschrieben, die die hepatische Lipidoxidation direkt und potent stimuliert. Kein anderer Inkretinagonist hat bisher eine vergleichbare Reduktion des Leberfetts in einer kontrollierten klinischen Studie gezeigt (Nature Medicine 2024; DOI: 10.1038/s41591-024-03018-2).
Wie verändert sich die Körperzusammensetzung?
Ein häufiger Kritikpunkt an pharmakologisch induziertem Gewichtsverlust ist der potenzielle Verlust von fettfreier Masse (Lean Mass), der langfristig zu Sarkopenie und metabolischer Verschlechterung führen kann. Um diese zentrale Frage zu adressieren, wurden in einer Substudie DXA-Ganzkörperscans (Dual-Energy-X-Ray-Absorptiometrie) durchgeführt. Die Ergebnisse, veröffentlicht in The Lancet Diabetes & Endocrinology (2025), zeigten unter der höchsten Retatrutide-Dosis eine Reduktion der Gesamtfettmasse um −26,1 %. Die fettfreie Masse nahm zwar absolut ab, blieb jedoch proportional zum Gesamtgewichtsverlust erhalten — ein Verhältnis, das mit dem bei bariatrischen chirurgischen Eingriffen beobachteten Muster vergleichbar ist. Der prozentuale Anteil der fettfreien Masse am Gesamtkörpergewicht stieg somit relativ an. Diese Daten legen nahe, dass der Gewichtsverlust unter Retatrutide überwiegend aus Fettgewebe stammt, was das metabolische Gesamtprofil der Substanz zusätzlich aufwertet (Lancet D&E 2025; DOI: 10.1016/S2213-8587(25)00092-0).
Welche Dosierungen wurden klinisch getestet?
In der Phase-1b-Studie von Urva et al. (2022) wurden Einzeldosen von 0,5 mg bis 12 mg sowie Mehrfachdosen bis 12 mg wöchentlich geprüft. Die terminale Plasmahalbwertszeit beträgt etwa sechs Tage, was eine einmal wöchentliche subkutane Injektion ermöglicht und die Therapieadhärenz fördert. In den Phase-2-Studien erfolgte eine schrittweise Dosissteigerung (Dose Escalation) über 12 bis 24 Wochen, um gastrointestinale Nebenwirkungen systematisch zu minimieren. Diese traten bei 35–63 % der Teilnehmenden auf, waren jedoch überwiegend mild bis moderat ausgeprägt und dosisabhängig. Übelkeit war das häufigste berichtete Symptom, gefolgt von Durchfall und gelegentlichem Erbrechen. Eine aktuelle systematische Meta-Analyse (2025), die die Sicherheitsdaten aus allen bisherigen Studien zusammenfasst, bestätigt das günstige Nutzen-Risiko-Profil von Retatrutide über alle untersuchten Dosierungen hinweg (Expert Rev Clin Pharmacol 2025; DOI: 10.1080/17512433.2025.2450254). Für Forschungszwecke ist Retatrutide in Dosierungen von 5 mg bis 60 mg als lyophilisiertes Pulver mit einer Reinheit von ≥ 99 % (HPLC-geprüft) erhältlich — jetzt Retatrutide im Shop ansehen.
Häufig gestellte Fragen (FAQ)
Ist Retatrutide für den therapeutischen Einsatz zugelassen?
Nein. Retatrutide (LY3437943) befindet sich derzeit in der klinischen Phase-3-Entwicklung bei Eli Lilly. Es liegt keine Zulassung durch die FDA, die EMA oder eine andere Regulierungsbehörde vor. Die Substanz wird ausschließlich für die in-vitro-Forschung angeboten und ist nicht für den Einsatz am Menschen bestimmt. Alle in diesem Leitfaden zitierten Ergebnisse stammen aus kontrollierten klinischen Studien unter ärztlicher Aufsicht.
Worin unterscheidet sich Retatrutide von Tirzepatid?
Tirzepatid (Mounjaro®/Zepbound®) ist ein dualer GIP/GLP-1-Agonist, während Retatrutide zusätzlich den Glucagon-Rezeptor aktiviert. Dieser dritte Mechanismus steigert die hepatische Thermogenese und Fettoxidation, was in klinischen Studien zu einem höheren Gewichtsverlust (−24,2 % gegenüber circa 22 %) und einer deutlich stärkeren Reduktion des Leberfettgehalts (−82,4 %) führte. Beide Substanzen werden von Eli Lilly entwickelt und jeweils einmal wöchentlich subkutan injiziert.
Wie wird Retatrutide korrekt gelagert?
Als lyophilisiertes Pulver sollte Retatrutide bei 2–8 °C (Kühlschrank) gelagert werden, geschützt vor Licht und Feuchtigkeit. Nach Rekonstitution mit bakteriostatischem Wasser empfiehlt sich eine Verwendung innerhalb von 28 Tagen bei durchgehender Kühlung. Die Reinheit beträgt ≥ 99 % (HPLC-geprüft). Alle Chargen werden mit einem detaillierten Analysezertifikat (Certificate of Analysis, CoA) geliefert.
Welche Phase-3-Studien laufen aktuell zu Retatrutide?
Eli Lilly führt mehrere Phase-3-Studien unter dem Programmnamen TRIUMPH durch. Diese umfassen Studien zur Adipositas (TRIUMPH-1 bis TRIUMPH-4), zu Typ-2-Diabetes (TRIUMPH-5) sowie zur MASLD/MASH (metabolisch assoziierte Steatohepatitis). Erste Phase-3-Ergebnisse werden für Ende 2025 beziehungsweise Anfang 2026 erwartet. Sämtliche Studien sind unter ClinicalTrials.gov registriert. Aktuelle Informationen finden Sie auf der ClinicalTrials.gov-Übersicht zu Retatrutide.
Haftungsausschluss
Wichtiger Hinweis: Retatrutide ist ein Forschungspeptid und nicht für den therapeutischen Einsatz am Menschen zugelassen. Alle in diesem Leitfaden genannten Ergebnisse stammen aus publizierten, begutachteten klinischen Studien und dienen ausschließlich der wissenschaftlichen Information. Die hier bereitgestellten Inhalte ersetzen keine ärztliche Beratung, Diagnose oder Behandlung. BergdorfBio übernimmt keine Haftung für Anwendungen außerhalb der Forschung. Vor jeder Verwendung in experimentellen Protokollen konsultieren Sie bitte die jeweils geltenden regulatorischen Anforderungen Ihres Landes sowie die institutionellen Ethikrichtlinien.
Quellen und Attribution
Dieser Leitfaden wurde am 22. März 2026 durch die wissenschaftliche Redaktion von BergdorfBio erstellt und basiert auf sechs begutachteten Originalarbeiten (Peer-Reviewed). Alle Referenzen sind mit DOI-Links zu den Originalpublikationen versehen:
- Urva et al. (2022) — Lancet; DOI: 10.1016/S0140-6736(22)02033-5
- Jastreboff et al. (2023) — NEJM; DOI: 10.1056/NEJMoa2301972
- Rosenstock et al. (2023) — Lancet; DOI: 10.1016/S0140-6736(23)01053-X
- Hartman et al. (2024) — Nature Medicine; DOI: 10.1038/s41591-024-03018-2
- DXA-Substudie (2025) — Lancet Diabetes & Endocrinology; DOI: 10.1016/S2213-8587(25)00092-0
- Meta-Analyse (2025) — Expert Rev Clin Pharmacol; DOI: 10.1080/17512433.2025.2450254
Letzte Aktualisierung: 22. März 2026. Bei Fragen oder Anmerkungen wenden Sie sich bitte an unser wissenschaftliches Team unter info@bergdorf.bio.
Hivatkozások
- Urva S., et al. LY3437943, a novel triple GIP, GLP-1, and glucagon receptor agonist in people with type 2 diabetes: a phase 1b, multicentre, double-blind, placebo-controlled, randomised, multiple-ascending dose trial. The Lancet. 2022.DOI
- Jastreboff A., et al. Triple–Hormone-Receptor Agonist Retatrutide for Obesity — A Phase 2 Trial. New England Journal of Medicine. 2023.DOI
- Rosenstock J., et al. Retatrutide, a GIP, GLP-1 and glucagon receptor agonist, for people with type 2 diabetes: a randomised, double-blind, placebo and active-controlled, parallel-group, phase 2 trial conducted in the USA. The Lancet. 2023.DOI
- Sanyal A., et al. Triple hormone receptor agonist retatrutide for metabolic dysfunction-associated steatotic liver disease: a randomized phase 2a trial. Nature Medicine. 2024.DOI
- Tewari J., et al. Efficacy and safety of triple hormone receptor agonist retatrutide for the management of obesity: a systematic review and meta-analysis. Expert Review of Clinical Pharmacology. 2025.
