

Trippelagonisten som satte et nytt tak, mot dobbeltagonisten som bygget kategorien. En sammenligning for forskningsprotokoller som vil forstå hvilket molekyl som representerer fronten, hvilket som er standarden, og hvorfor skillet er av betydning.

Tirzepatide (Eli Lillys Mounjaro/Zepbound) er en dobbel GLP-1/GIP-reseptoragonist med fire års fase 3-data, tre FDA-godkjenninger og en publisert kardiovaskulær endepunktsstudie. Retatrutide, Lillys oppfølgermolekyl, er en trippelagonist som legger glukagonreseptoren til samme dobbeltskjelett, og som i sin første fase 3-avlesning ga den dypeste vektreduksjonen som noensinne er rapportert i en registreringsstudie for fedme: omtrent 28,7 % ved 68 uker 5 mot tirzepatides SURMOUNT-1-topp på rundt 22,5 % ved 72 uker 13.
Evidensgrunnlagene er ikke symmetriske. Tirzepatide har den modne, fagfellevurderte saken. Retatrutide har det høyere observerte taket, en mekanistisk bredere målprofil og to nettverksmetaanalyser som peker i dets retning 20 21. For forskningsprotokoller som prioriterer maksimalt terapeutisk tak og mekanistisk bredde, er vårt redaksjonelle valg retatrutide. For protokoller som verdsetter regulatorisk dybde i evidensgrunnlaget og en avklart sikkerhetsmerking, forblir tirzepatide referansemolekylet.
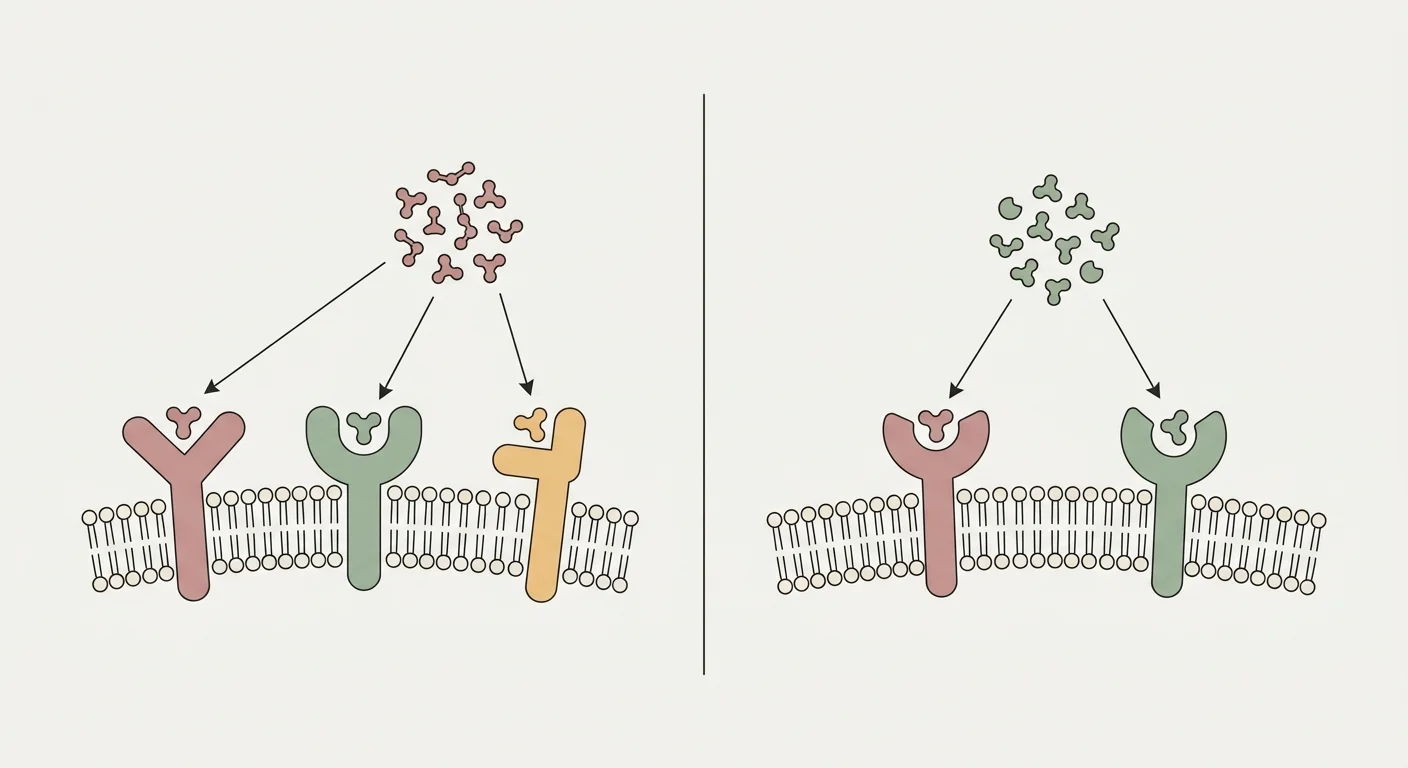
Retatrutide (LY3437943) er et enkelt peptid konstruert for å aktivere tre reseptorer i inkretinfamilien samtidig: glukagonlignende peptid-1-reseptoren (GLP-1R), den glukoseavhengige insulinotrope polypeptidreseptoren (GIPR) og glukagonreseptoren (GCGR) 26. GLP-1R-armen driver den sentrale appetittdempingen, forsinket ventrikkeltømming og glukoseavhengig insulinsekresjon som er kjent fra semaglutide og tirzepatide 24. GIPR-armen tilfører synergistisk insulinotrop aktivitet og styrker, i fettvev, sunn lipidbuffring som reduserer ektopisk fettavleiring i lever og muskulatur 25.
Den særegne armen er GCGR. Glukagon framstilles vanligvis som det motregulerende hormonet som hever blodglukosen; i konteksten av en balansert trippelagonist motvirkes dets klassiske effekt på hepatisk glukoseproduksjon av den samtidige insulinotrope GLP-1R/GIPR-virkningen, mens de metabolske effektene peptiddesignere faktisk ønsker fra GCGR, beholdes: økt energiomsetning via termogenese i brunt fettvev og oksidasjon i skjelettmuskulatur, lipolyse i fettvev med frigjøring av frie fettsyrer for betaoksidasjon, og hepatisk fettsyreoksidasjon som klarerer triglyserider fra leveren 27. I fase 2a-data fra MASLD ga retatrutide rundt 85–90 % reduksjon i leverfett ved høyeste dose; om lag 90 % av deltakerne på 12 mg nådde leverfett under 5 % ved 48 uker, en størrelse som dobbeltagonisme ikke har vist 3.
Ingen direkte randomisert kontrollert studie av retatrutide mot tirzepatide er publisert eller varslet per april 2026. En registreringsstudie head-to-head (NCT06662383) er synlig i Lillys pipeline-oversikt, men ingen avlesning er rapportert. Enhver komparativ påstand i denne artikkelen bærer derfor et forbehold: den er enten en indirekte sammenligning på tvers av studier med ulike populasjoner, doseringsregimer og endepunkter, eller en mekanistisk ekstrapolasjon fra prekliniske og fase 2-data. Det er ikke en grunn til å overse signalet — det er en grunn til å nyansere det.
To nettverksmetaanalyser har forsøkt å plassere molekylene på samme skala. Analysen fra oktober 2025 publisert i Journal of the Endocrine Society (sammendrag SUN-659, med fullt fagfellevurdert artikkel hos PMC12544991) rapporterte retatrutide ved en gjennomsnittlig absolutt reduksjon på −16,34 kg og −23,77 % kroppsvekt mot −11,82 kg og −16,79 % for tirzepatide, en indirekte fordel i retatrutides favør 20. Den samme analysen flagget en høyere relativ risiko for bivirkninger ved retatrutide (RR 4,10 mot 2,78), i samsvar med en høyere gastrointestinal byrde ved høyeste doser. En bredere nettverksmetaanalyse av syv preparater publisert i Metabolism (2024) rangerte molekylene for vekttap som retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, med konsistente rangeringer for midjeomkrets, HbA1c og fastende plasmaglukose 21.
Begge nettverksmetaanalyser favoriserer retatrutide tallmessig og retningsmessig, men fraværet av direkte RCT-evidens innebærer at enhver komparativ påstand må bære et forbehold. For forskningsformål er dette en grunn til videre undersøkelser, ikke en grunn til å avvise signalet.
Sikkerhetsprofilen i fase 2 er i samsvar med GLP-1-reseptoragonistklassen, dominert av doseavhengige gastrointestinale bivirkninger som konsentreres i de første en til to ukene av hver opptrappingstrinn. Fase 3-sikkerhet (TRIUMPH-4) foreligger kun som toppresultat fra pressemelding per april 2026 og er ennå ikke fagfellevurdert i full datasettoppløsning.
TRIUMPH-4-toppresultatet rapporterer ~28,7 % reduksjon ved 68 uker og overgår tirzepatides SURMOUNT-1-topp ved 72 uker med rundt seks prosentpoeng. Begge publiserte nettverksmetaanalyser peker i samme retning.
GCGR-armen tilfører signalveier som tirzepatide mangler: hepatisk fettsyreoksidasjon (~85–90 % reduksjon i leverfett i fase 2a MASLD), lipolyse i fettvev og termogen energiomsetning.
Tolv pluss fase 3-studier, tre FDA-godkjenninger, en publisert CVOT med 13 165 pasienter og en moden sikkerhetsmerking i preparatomtalen. Referansemolekylet for GLP-1/GIP-forskning i dag.
SURPASS-2 slo semaglutide 1 mg head-to-head på HbA1c; SURPASS-CVOT er den eneste publiserte kardiovaskulære endepunktsstudien for noen av molekylene. Retatrutides T2D-evidens forblir på fase 2-nivå (Rosenstock 2023).
Tirzepatide, utvetydig. Tolv pluss fase 3-studier, tre FDA-godkjenninger og en publisert kardiovaskulær endepunktsstudie i 13 165 pasienter 12. Retatrutide har ett fase 3-toppresultat (TRIUMPH-4) og et fase 2-program på rundt seks fagfellevurderte publikasjoner 1 5. Gapet vil snevre inn gjennom 2026 etter hvert som TRIUMPH-1, TRIUMPH-2 og TRIUMPH-3 leses ut.
Retatrutide er vårt valg. Ikke fordi det har mer studiedata — det har det ikke. Tirzepatides fase 3-program er fire år dypere, dets tre FDA-godkjenninger spenner over type 2-diabetes, kronisk vektkontroll og obstruktiv søvnapné, og dets publiserte kardiovaskulære endepunktsstudie i over tretten tusen pasienter er et faktum vi ikke bestrider 12 28. For forskningsprotokoller som trenger det dypeste, mest gjennomgranskede evidensgrunnlaget i inkretinklassen i dag, er tirzepatide referansemolekylet og vil forbli det inntil TRIUMPH-programmet er fullført.
Men for forskningsprotokoller som forfølger det høyeste terapeutiske taket, favoriserer tallene retatrutide. Den første fase 3-avlesningen rapporterte rundt 28,7 % vektreduksjon ved 12 mg over 68 uker 5— en betydningsfull takfordel på seks prosentpoeng over tirzepatides SURMOUNT-1-topp på 22,5 % over 72 uker 13. Den mekanistiske forklaringen er ikke spekulativ: glukagonreseptoren tilfører hepatisk fettsyreoksidasjon, lipolyse i fettvev og termogen energiomsetning som dobbeltagonisme ved konstruksjon ikke kan engasjere 27, og fase 2a MASLD-avlesningens leverfettreduksjon på 85–90 % er en direkte signatur av den signalveien 3. Begge publiserte nettverksmetaanalyser peker i retatrutides retning 20 21. Evidensgrunnlaget vil modnes; taket, ved konstruksjon, vil ikke flytte seg nedover.
For forskningsfronten innen metabolsk peptidterapi er retatrutide vinneren. For protokoller som verdsetter regulatorisk dybde over alt annet, forblir tirzepatide standarden. Det er en klarere rolledeling enn de fleste «X mot Y»-sammenligninger kan tilby, og ærlighet om delingen er mer nyttig enn én tvungen vinner.
Retatrutide vinner på dimensjonene som betyr mest for forskning på fronten: høyere observert tak i TRIUMPH-4, mekanistisk bredde fra trippelagonisme og konsistent retning på tvers av begge publiserte nettverksmetaanalyser. Tirzepatide forblir referansemolekylet for protokoller som trenger det dypeste publiserte evidensgrunnlaget i dag.
Til stede; ~85–90 % reduksjon i leverfett i fase 2a MASLD 3
Fraværende ved konstruksjon
~144 t (~6 dager)
~120 t (~5 dager)
1 toppresultat (TRIUMPH-4); TRIUMPH-1/2/3 utestående 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Ingen (ingen CVOT igangsatt)
SURPASS-CVOT (n=13 165; NEJM des. 2025) 12
Ingen (ingen godkjent merking)
MTC-skjoldbrusk-C-celler (gnager, human relevans ikke etablert) 28
Ingen publisert
Ingen publisert
Én gang ukentlig, subkutant
Én gang ukentlig, subkutant
USA: tidligst sent 2027 (NDA tidligst Q4 2026) 22
Allerede godkjent (USA: 2022/2023/2024; EU: 2022/2024)
Lyofilisert; rekonstituering med BAC-vann; 2–8 °C
Lyofilisert; rekonstituering med BAC-vann; 2–8 °C
Høyere tak + glukagonreseptor-bredde
Lavere tak; best karakteriserte sikkerhetsprofil
Tirzepatide (LY3298176) er en dobbel GLP-1R/GIPR-agonist — et enkelt 39-resters peptid avstemt for å engasjere begge inkretinreseptorer med sammenlignbar potens. GLP-1R-armen bidrar med den samme kjernemekanismen som er kjent fra første generasjon GLP-1-analoger: glukoseavhengig insulinsekresjon, hemming av glukagon fra alfaceller, hypothalamisk appetittregulering og forsinket ventrikkeltømming 24.
Det som skiller tirzepatide fra rene GLP-1-agonister, er den tilførte GIPR-aktiviteten. Prekliniske studier viser at samtidig administrasjon av GIP og GLP-1 gir additive og i enkelte mål synergistiske reduksjoner i kroppsvekt og glukose, mer enn hver for seg 25. Sentral GIPR-aktivering ser ut til å potensere GLP-1-indusert anoreksi via hypothalamisk POMC-signalering; perifer GIPR-aktivering i hvitt fettvev øker depotets bufferkapasitet og reduserer behovet for ektopisk avleiring. Den observerbare konsekvensen er den mest potente vekt- og glukosesenkende profilen til noe molekyl godkjent før retatrutide: SURMOUNT-1 rapporterte rundt 22,5 % vektreduksjon ved 15 mg-dosen over 72 uker 13, og SURMOUNT-5 viste tirzepatide som overlegen semaglutide 2,4 mg i direkte sammenligning ved 72 uker (−20,2 % mot −13,7 %) 18.
Glukagonreseptor-armen er retatrutides mekanistiske differensierende egenskap. Prekliniske og fase 2-data antyder at dette omsettes i lipidsenkende, leverfettreduserende og energiomsetningsfremmende effekter som tirzepatide, ved konstruksjon, mangler. Hvorvidt dette oversettes til den direkte sammenligningsfordelen som nettverksmetaanalysene antyder, vil forbli åpent inntil en head-to-head-RCT leses ut — og per april 2026 er ingen slik varslet.
Tirzepatides evidensdybde er uten sidestykke i dag — tolv fase 3-studier på tvers av to sykdomsprogrammer, en publisert kardiovaskulær endepunktsstudie i over tretten tusen pasienter, og tre FDA-godkjenninger på etiketten. Retatrutides foreliggende avlesning er enestående og overgår tirzepatides beste fase 3-tak ved et kortere observasjonsvindu. Det er et signal som fortjener seriøs oppmerksomhet etter hvert som TRIUMPH-1, TRIUMPH-2 og TRIUMPH-3 modnes gjennom 2026 og 2027.
Moden sikkerhetsmerking i preparatomtalen for både Mounjaro og Zepbound. Vanlige bivirkninger speiler GLP-1-klassen og konsentreres ved doseopptrapping; alvorlige risikoer er fanget i en innrammet advarsel og et sett av advarsler og forsiktighetsregler som er finjustert gjennom legemiddelovervåking etter markedsføring (FAERS-analyse 2024 og EMAs farmakovigilans).
Denne artikkelen er en redaksjonell sammenligning utarbeidet for lesere i forskningskontekst. Hverken retatrutide eller tirzepatide tilbys eller anbefales for selvadministrasjon hos mennesker via dette nettstedet. Der tirzepatide er forskrevet, er det kun tilgjengelig under tilsyn av lege i jurisdiksjoner der det er godkjent (Mounjaro for T2D; Zepbound for kronisk vektkontroll og obstruktiv søvnapné). Retatrutide er utprøvende globalt per april 2026 og bør kun håndteres innenfor egnede forskningsprotokoller.
Sikkerhetsdata oppsummert her gjenspeiler publiserte fase 2- og fase 3-datasett samt gjeldende preparatomtaler. Nye signaler kan oppstå når som helst; lastUpdated-datoen på denne siden angir skjæringsdatoen for vår gjennomgang. Ingenting på denne siden utgjør medisinsk rådgivning eller en erstatning for konsultasjon med kvalifisert helsepersonell.
På klassenivå har begge en GI-dominert profil (kvalme, brekninger, diaré) som konsentreres ved doseopptrapping. Nettverksmetaanalysen fra oktober 2025 rapporterte en høyere relativ risiko for bivirkninger ved retatrutide (RR 4,10) enn ved tirzepatide (RR 2,78), i samsvar med høyere GI-byrde ved høyeste doser 20. Tirzepatide bærer en innrammet MTC-advarsel og en karakterisert pankreatitt-/galleblære-/hypersensitivitetsprofil 28 29; retatrutides analoge langtidssikkerhetsprofil er ikke etablert.
Publiserte fase 2- og fase 3-studier for begge molekyler inkluderer som monoterapi (med eller uten bakgrunnsbehandling for T2D, slik som metformin eller insulin). Det finnes ingen publisert evidens på stabling med andre forskningspeptider. Enhver kombinasjonsprotokoll er strengt utprøvende og utenfor evidensgrunnlaget oppsummert i denne artikkelen.
Retatrutides halveringstid på ~144 timer og tirzepatides på ~120 timer støtter begge en enkelt subkutan ukedose, regimet brukt i hver registreringsstudie. Den noe lengre halveringstiden til retatrutide gir en beskjeden buffer mot variasjon ved glemte doser, men endrer ikke det grunnleggende ukentlige rytme.
Ja. Både retatrutide og tirzepatide er listet for forskningsbruk i både EU- og US-kanalene. Tilgjengelighet, hetteglasstørrelser og kanalspesifikke priser vises på hvert produkts detaljside.
Avlesningene av TRIUMPH-1 (fedme uten T2D), TRIUMPH-2 (fedme med T2D) og TRIUMPH-3 (fedme med etablert kardiovaskulær sykdom) ventes gjennom 2026 i henhold til Lillys veiledning 4. Hver vil materielt utvide retatrutides evidensgrunnlag; samlet vil de avgjøre om TRIUMPH-4-taket generaliseres på tvers av populasjoner, og om en NDA-innsending fremskyndes fra det nåværende vinduet med tidligst Q4 2026.