

Trojitý agonista, ktorý posunul nový strop, oproti duálnemu agonistovi, ktorý vybudoval celú kategóriu. Porovnanie pre výskumné protokoly, ktoré chcú pochopiť, ktorá molekula predstavuje hranicu, ktorá štandard, a prečo na tomto rozdiele záleží.

Tirzepatid (Mounjaro/Zepbound od spoločnosti Eli Lilly) je duálny agonista receptorov GLP-1/GIP so štyrmi rokmi dát z fázy 3, tromi schváleniami FDA a publikovanou kardiovaskulárnou outcomes štúdiou. Retatrutid, následná molekula spoločnosti Lilly, je trojitý agonista, ktorý k tomu istému duálnemu základu pridáva glukagónový receptor a vo svojom prvom čítaní fázy 3 dosiahol najhlbšie zníženie hmotnosti, aké kedy bolo zaznamenané v registračnej štúdii obezity: približne 28,7 % po 68 týždňoch 5 oproti vrcholu tirzepatidu v štúdii SURMOUNT-1, ktorý činil zhruba 22,5 % po 72 týždňoch 13.
Dôkazové základne nie sú symetrické. Tirzepatid má vyzretý, recenzovaný prípad. Retatrutid má vyšší pozorovaný strop, mechanisticky širší cieľový profil a dve sieťové meta-analýzy, ktoré ukazujú v jeho prospech 20 21. Pre výskumné protokoly, ktoré uprednostňujú maximálny terapeutický strop a šírku mechanizmu, je našou redakčnou voľbou retatrutid. Pre protokoly, ktoré cenia hĺbku dôkazov regulačnej úrovne a ustálený bezpečnostný profil, zostáva referenčnou molekulou tirzepatid.
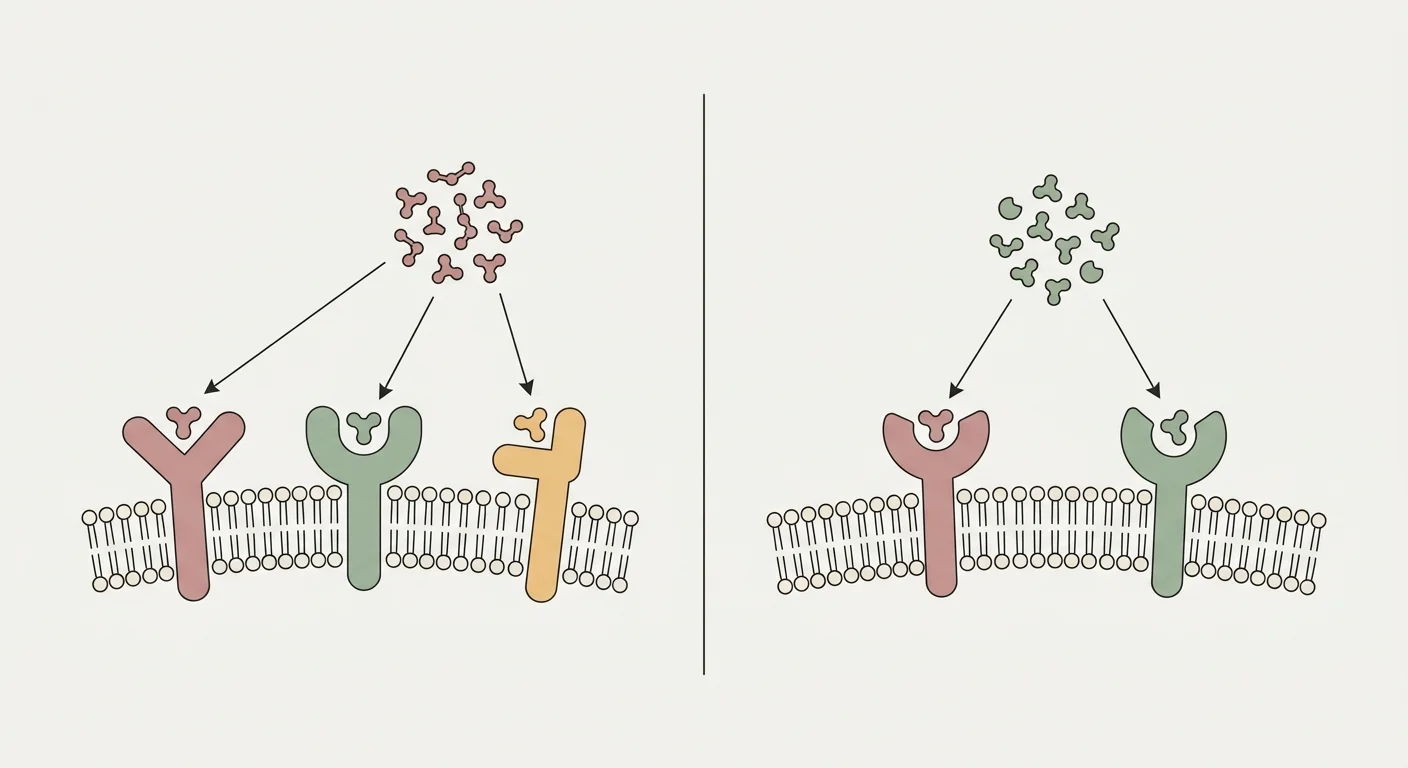
Retatrutid (LY3437943) je jediný peptid navrhnutý tak, aby súčasne pôsobil ako agonista na troch receptoroch z rodiny inkretínov: receptor pre glukagónu podobný peptid 1 (GLP-1R), receptor pre glukózodependentný inzulinotropný polypeptid (GIPR) a glukagónový receptor (GCGR) 26. Rameno GLP-1R poháňa centrálne potlačenie chuti do jedla, oneskorenie vyprázdňovania žalúdka a glukózodependentnú sekréciu inzulínu, ktorá je známa zo semaglutidu a tirzepatidu 24. Rameno GIPR pridáva synergickú inzulinotropnú aktivitu a v tukovom tkanive zlepšuje zdravé ukladanie lipidov, čím znižuje ektopické ukladanie tuku v pečeni a svaloch 25.
Rozlišujúcim ramenom je GCGR. Glukagón sa zvyčajne vníma ako kontraregulačný hormón, ktorý zvyšuje hladinu glukózy v krvi; v kontexte vyváženého trojitého agonistu je jeho klasický účinok na hepatálnu produkciu glukózy kompenzovaný súčasným inzulinotropným pôsobením GLP-1R/GIPR, zatiaľ čo sa zachovávajú metabolické účinky, ktoré dizajnéri peptidov od GCGR skutočne chcú: zvýšený energetický výdaj prostredníctvom termogenézy v hnedom tukovom tkanive a oxidácie v kostrovom svale, lipolýza tukového tkaniva s uvoľňovaním voľných mastných kyselín pre beta-oxidáciu a hepatálna oxidácia mastných kyselín, ktorá z pečene odstraňuje triglyceridy 27. V dátach fázy 2a MASLD retatrutid pri najvyššej dávke spôsobil zhruba 85–90 % zníženie pečeňového tuku; približne 90 % účastníkov s 12 mg dosiahlo po 48 týždňoch hladinu pečeňového tuku pod 5 %, čo je rozsah, ktorý duálny agonizmus nepreukázal 3.
K aprílu 2026 nebola publikovaná ani oznámená žiadna priama randomizovaná kontrolovaná štúdia retatrutid versus tirzepatid. Registračná head-to-head štúdia (NCT06662383) je viditeľná v pipeline trackeri spoločnosti Lilly, ale neboli oznámené žiadne výsledky. Každé komparatívne tvrdenie v tomto článku preto nesie výhradu: ide buď o nepriame porovnanie naprieč štúdiami s rôznymi populáciami, dávkovacími schémami a koncovými ukazovateľmi, alebo o mechanistickú extrapoláciu z predklinických dát a dát z fázy 2. To nie je dôvod ignorovať tento signál — je to dôvod kvalifikovať ho.
Dve sieťové meta-analýzy sa pokúsili umiestniť molekuly na rovnakú stupnicu. Analýza z októbra 2025 publikovaná v Journal of the Endocrine Society (abstrakt SUN-659, s úplným recenzovaným článkom v PMC12544991) zaznamenala u retatrutidu priemerné absolútne zníženie −16,34 kg a −23,77 % telesnej hmotnosti oproti −11,82 kg a −16,79 % u tirzepatidu, čo je nepriama výhoda v prospech retatrutidu 20. Tá istá analýza upozornila na vyššie relatívne riziko nežiaducich účinkov pre retatrutid (RR 4,10 vs 2,78), čo je v súlade s vyššou gastrointestinálnou záťažou pri najvyšších dávkach. Širšia sieťová meta-analýza siedmich látok publikovaná v Metabolism (2024) zoradila molekuly pre úbytok hmotnosti ako retatrutid 12 mg > retatrutid 8 mg > tirzepatid 15 mg, s konzistentným poradím naprieč obvodom pása, HbA1c a glukózou nalačno 21.
Obe sieťové meta-analýzy uprednostňujú retatrutid číselne i smerovo, ale absencia priamych RCT dôkazov znamená, že akékoľvek komparatívne tvrdenie musí niesť výhradu. Pre výskumné účely je to dôvod na ďalšie skúmanie, nie dôvod tento signál odmietnuť.
Bezpečnostný profil fázy 2 je v súlade s triedou agonistov receptora GLP-1, prevažujú dávkovo závislé gastrointestinálne nežiaduce účinky, ktoré sa koncentrujú v prvom až druhom týždni každého eskalačného kroku. Bezpečnosť fázy 3 (TRIUMPH-4) je k aprílu 2026 dostupná len ako top-line z tlačovej správy a ešte nebola recenzovaná v rozlíšení úplného súboru dát.
Top-line z TRIUMPH-4 hlási ~28,7 % zníženie po 68 týždňoch, čo prekračuje vrchol tirzepatidu zo SURMOUNT-1 po 72 týždňoch zhruba o šesť percentuálnych bodov. Obe publikované sieťové meta-analýzy ukazujú rovnakým smerom.
Rameno GCGR pridáva dráhy, ktoré tirzepatidu chýbajú: hepatálnu oxidáciu mastných kyselín (~85–90 % zníženie pečeňového tuku vo fáze 2a MASLD), lipolýzu tukového tkaniva a termogénny energetický výdaj.
Dvanásť+ štúdií fázy 3, tri schválenia FDA, publikovaná CVOT na 13 165 pacientoch a vyzretá bezpečnostná obálka v predpisovacích informáciách. Dnešná referenčná molekula pre výskum GLP-1/GIP.
SURPASS-2 v priamom porovnaní porazil semaglutid 1 mg na HbA1c; SURPASS-CVOT je jediná publikovaná kardiovaskulárna outcomes štúdia naprieč oboma molekulami. Dôkazy retatrutidu pre T2D zostávajú vo fáze 2 (Rosenstock 2023).
Tirzepatid, jednoznačne. Dvanásť+ štúdií fázy 3, tri schválenia FDA a publikovaná kardiovaskulárna outcomes štúdia na 13 165 pacientoch 12. Retatrutid má jeden top-line z fázy 3 (TRIUMPH-4) a program fázy 2 zhruba so šiestimi recenzovanými publikáciami 1 5. Tento rozdiel sa v priebehu roka 2026 zúži, keď sa zverejnia výsledky TRIUMPH-1, TRIUMPH-2 a TRIUMPH-3.
Retatrutid je našou voľbou. Nie preto, že má viac dát zo štúdií — nemá. Program fázy 3 tirzepatidu je o štyri roky hlbší, jeho tri schválenia FDA pokrývajú diabetes 2. typu, chronický manažment hmotnosti a obštrukčné spánkové apnoe a jeho publikovaná kardiovaskulárna outcomes štúdia s viac než trinástimi tisícmi pacientov je fakt, ktorý nespochybňujeme 12 28. Pre výskumné protokoly, ktoré potrebujú najhlbšiu, najlepšie preverenú dôkazovú základňu dostupnú dnes v triede inkretínov, je tirzepatid referenčnou molekulou a zostane ňou, kým sa nedokončí program TRIUMPH.
Pre výskumné protokoly sledujúce najvyšší terapeutický strop však čísla uprednostňujú retatrutid. Jeho prvé čítanie z fázy 3 zaznamenalo zhruba 28,7 % zníženie hmotnosti pri 12 mg počas 68 týždňov 5— významnú šesťpercentuálnu výhodu v strope oproti vrcholu tirzepatidu zo SURMOUNT-1 vo výške 22,5 % počas 72 týždňov 13. Mechanistické vysvetlenie nie je špekulatívne: glukagónový receptor pridáva hepatálnu oxidáciu mastných kyselín, lipolýzu tukového tkaniva a termogénny energetický výdaj, ktorý duálny agonizmus konštrukčne nemôže aktivovať 27, a 85–90 % zníženie pečeňového tuku v čítaní fázy 2a MASLD je priamym podpisom tejto dráhy 3. Obe publikované sieťové meta-analýzy ukazujú v smere retatrutidu 20 21. Dôkazová základňa dozreje; strop sa konštrukčne neposunie nadol.
Pre výskumnú hranicu metabolickej peptidovej terapie je víťazom retatrutid. Pre protokoly, ktoré nadovšetko cenia hĺbku regulačnej úrovne, zostáva tirzepatid štandardom. Toto je jasnejšie rozdelenie rolí, než aké dokáže ponúknuť väčšina porovnaní typu „X vs Y“, a úprimnosť ohľadom tohto rozdelenia je užitočnejšia než vynútený jediný víťaz.
Retatrutid víťazí v dimenziách, na ktorých pre hraničný výskum najviac záleží: vyšší pozorovaný strop v TRIUMPH-4, šírka mechanizmu trojitého agonistu a konzistentné smerovanie naprieč oboma publikovanými sieťovými meta-analýzami. Tirzepatid zostáva referenčnou molekulou pre protokoly, ktoré dnes potrebujú najhlbšiu publikovanú dôkazovú základňu.
Prítomné; ~85–90 % zníženie pečeňového tuku vo fáze 2a MASLD 3
Konštrukčne neprítomné
~144 h (~6 dní)
~120 h (~5 dní)
1 top-line (TRIUMPH-4); TRIUMPH-1/2/3 čakajú 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Žiadna (CVOT nezahájená)
SURPASS-CVOT (n=13 165; NEJM dec. 2025) 12
Žiadne (žiadne schválené označenie)
MTC tyroidné C-bunky (hlodavce, relevancia pre ľudí nepreukázaná) 28
Žiadna nepublikovaná
Žiadna nepublikovaná
Raz týždenne, subkutánne
Raz týždenne, subkutánne
USA: najskôr koncom 2027 (NDA najskôr Q4 2026) 22
Už schválený (USA: 2022/2023/2024; EÚ: 2022/2024)
Lyofilizovaný; rekonštitúcia BAC vodou; 2–8 °C
Lyofilizovaný; rekonštitúcia BAC vodou; 2–8 °C
Vyšší strop + šírka glukagónového receptora
Nižší strop; najlepšie charakterizovaná bezpečnostná obálka
Tirzepatid (LY3298176) je duálny agonista GLP-1R / GIPR — jediný 39-aminokyselinový peptid vyladený na to, aby s porovnateľnou účinnosťou interagoval s oboma inkretínovými receptormi. Rameno GLP-1R prispieva tým istým základným mechanizmom známym z prvej generácie analógov GLP-1: glukózodependentná sekrécia inzulínu, supresia glukagónu z alfa-buniek, hypotalamická regulácia chuti do jedla a spomalené vyprázdňovanie žalúdka 24.
Čo odlišuje tirzepatid od čistých GLP-1 agonistov, je pridaná aktivita GIPR. V predklinických podmienkach spoločné podávanie GIP s GLP-1 produkuje aditívne a v niektorých meraniach synergické zníženia telesnej hmotnosti a glukózy, viac než ktorýkoľvek z nich samostatne 25. Zdá sa, že centrálna aktivácia GIPR potencuje anorexiu vyvolanú GLP-1 prostredníctvom hypotalamického signalizovania POMC; periférna aktivácia GIPR v bielom tukovom tkanive zlepšuje tlmivú kapacitu zásobníka a znižuje potrebu ektopického ukladania. Pozorovateľným dôsledkom je najúčinnejší profil znižovania hmotnosti a glukózy spomedzi všetkých molekúl schválených pred retatrutidom: SURMOUNT-1 zaznamenal pri dávke 15 mg po 72 týždňoch zhruba 22,5 % zníženie hmotnosti 13a SURMOUNT-5 ukázal, že tirzepatid je v priamom porovnaní po 72 týždňoch lepší ako semaglutid 2,4 mg (−20,2 % vs −13,7 %) 18.
Rameno glukagónového receptora je mechanistickým diferenciátorom retatrutidu. Predklinické dáta a dáta z fázy 2 naznačujú, že sa to premieta do účinkov znižovania lipidov, redukcie pečeňového tuku a energetického výdaja, ktoré tirzepatid svojou konštrukciou nemá. Či sa to premietne do výhody pri priamom porovnaní, ktorú naznačujú sieťové meta-analýzy, zostane otvorené, kým sa nezverejnia výsledky head-to-head RCT — čo, k aprílu 2026, ešte nebolo oznámené.
Hĺbka dôkazov tirzepatidu je dnes neprekonateľná — dvanásť štúdií fázy 3 naprieč dvomi ochoreniami, publikovaná kardiovaskulárna outcomes štúdia s viac než trinástimi tisícmi pacientov a tri schválenia FDA na označení. Dostupný výsledok retatrutidu, hoci jediný, prekonáva najlepší strop tirzepatidu z fázy 3 pri kratšom pozorovacom okne. Toto je signál, ktorý si zaslúži vážnu pozornosť, keď budú v priebehu rokov 2026 a 2027 dozrievať TRIUMPH-1, TRIUMPH-2 a TRIUMPH-3.
Vyzretá bezpečnostná obálka v predpisovacích informáciách pre Mounjaro a Zepbound. Bežné NÚ odzrkadľujú triedu GLP-1 a koncentrujú sa pri eskalácii dávky; závažné riziká sú zachytené v rámčekovom varovaní a v sade varovaní a opatrení spresnených prostredníctvom postmarketingového dohľadu (analýza FAERS 2024 a farmakovigilancia EMA).
Tento článok je redakčné porovnanie pripravené pre čitateľov vo výskumnom kontexte. Ani retatrutid, ani tirzepatid nie je prostredníctvom tejto stránky ponúkaný ani odporúčaný na ľudské samopodávanie. Tam, kde je tirzepatid predpisovaný, je dostupný iba pod dohľadom lekára v jurisdikciách, kde bol schválený (Mounjaro pre T2D; Zepbound pre chronický manažment hmotnosti a obštrukčné spánkové apnoe). Retatrutid je k aprílu 2026 globálne v skúšaní a má sa s ním manipulovať iba v rámci primeraných výskumných protokolov.
Bezpečnostné údaje tu zhrnuté odrážajú publikované súbory dát fázy 2 a fázy 3 a aktuálne predpisovacie informácie. Nové signály sa môžu objaviť kedykoľvek; dátum lastUpdated na tejto stránke označuje hraničný termín nášho prehľadu. Nič na tejto stránke nepredstavuje lekársku radu ani náhradu za konzultáciu s kvalifikovaným klinickým odborníkom.
Tirzepatid je schválený pod dvomi obchodnými názvami: Mounjaro pre diabetes 2. typu (FDA, máj 2022) a Zepbound pre chronický manažment hmotnosti (november 2023) a stredne závažné až závažné obštrukčné spánkové apnoe s obezitou (december 2024) 28. Retatrutid je všade v skúšaní; k aprílu 2026 nebola podaná žiadna NDA 22.
Retatrutid, na základe dostupných dát. TRIUMPH-4 zaznamenal ~−28,7 % pri 12 mg počas 68 týždňov 5; najlepší výsledok obezity z fázy 3 tirzepatidu, SURMOUNT-1 pri 15 mg počas 72 týždňov, bol ~−22,5 % 13. Obe publikované sieťové meta-analýzy hodnotia retatrutid vyššie pri redukcii telesnej hmotnosti 20 21.
Na úrovni triedy majú obe profil dominovaný gastrointestinálnymi účinkami (nevoľnosť, vracanie, hnačka), ktoré sa koncentrujú pri eskalácii dávky. Sieťová meta-analýza z októbra 2025 zaznamenala vyššie relatívne riziko nežiaducich účinkov pre retatrutid (RR 4,10) než pre tirzepatid (RR 2,78), čo je v súlade s vyššou gastrointestinálnou záťažou pri najvyšších dávkach 20. Tirzepatid nesie rámčekové varovanie pre MTC a charakterizovaný profil pankreatitídy / žlčníka / hypersenzitivity 28 29; analogická dlhodobá bezpečnostná obálka retatrutidu nebola stanovená.
Publikované štúdie fázy 2 a fázy 3 pre obe molekuly zaraďujú účastníkov ako monoterapiu (s existujúcou liečbou T2D, ako je metformín alebo inzulín, alebo bez nej). Neexistujú publikované dôkazy o kombinovaní niektorej z nich s inými výskumnými peptidmi. Akýkoľvek kombinačný protokol je prísne v skúšaní a mimo dôkazovej základne zhrnutej v tomto článku.
Polčas retatrutidu ~144 hodín a polčas tirzepatidu ~120 hodín obidva podporujú jednotnú týždennú subkutánnu dávku, čo je rozvrh použitý v každej registračnej štúdii. Mierne dlhší polčas retatrutidu poskytuje miernu rezervu proti variabilite vynechaných dávok, ale nemení základnú týždennú kadenciu.
Áno. Retatrutid aj tirzepatid sú uvedené pre výskumné použitie v kanáloch EÚ aj USA. Dostupnosť, veľkosti liekoviek a ceny špecifické pre kanál sú zobrazené na detailnej stránke každého produktu.
Výsledky TRIUMPH-1 (obezita bez T2D), TRIUMPH-2 (obezita s T2D) a TRIUMPH-3 (obezita so zavedeným kardiovaskulárnym ochorením) sa očakávajú v priebehu roka 2026 podľa usmernení spoločnosti Lilly 4. Každý z nich materiálne rozšíri dôkazovú základňu retatrutidu; spoločne určia, či sa strop TRIUMPH-4 zovšeobecní naprieč populáciami a či sa podanie NDA posunie z aktuálneho najskoršieho okna Q4 2026.