

Der Triple-Agonist, der eine neue Obergrenze gesetzt hat, gegen den Dual-Agonist, der die Kategorie aufgebaut hat. Ein Vergleich für Forschungsprotokolle, die verstehen wollen, welches Molekül die Spitze ist, welches der Standard, und warum diese Unterscheidung zählt.

Tirzepatid (Eli Lillys Mounjaro/Zepbound) ist ein dualer GLP-1/GIP-Rezeptoragonist mit vier Jahren Phase-3-Daten, drei FDA-Zulassungen und einer publizierten kardiovaskulären Outcome-Studie. Retatrutid, Lillys Nachfolgemolekül, ist ein Triple-Agonist, der den Glukagonrezeptor zu derselben dualen Grundstruktur hinzufügt und in seiner ersten Phase-3-Auswertung die tiefste je in einer zulassungsrelevanten Adipositas-Studie berichtete Gewichtsreduktion erzielte: etwa 28,7% nach 68 Wochen 5 gegenüber dem SURMOUNT-1-Höchstwert von Tirzepatid von rund 22,5% nach 72 Wochen 13.
Die Evidenzbasen sind nicht symmetrisch. Tirzepatid hat den ausgereiften, peer-reviewten Datensatz. Retatrutid hat die höhere beobachtete Obergrenze, ein mechanistisch breiteres Zielprofil und zwei Netzwerk-Metaanalysen, die in seine Richtung weisen 20 21. Für Forschungsprotokolle, die maximale therapeutische Obergrenze und Mechanismusbreite priorisieren, ist unsere redaktionelle Empfehlung Retatrutid. Für Protokolle, die regulatorisch belastbare Evidenztiefe und ein etabliertes Sicherheitslabel schätzen, bleibt Tirzepatid das Referenzmolekül.
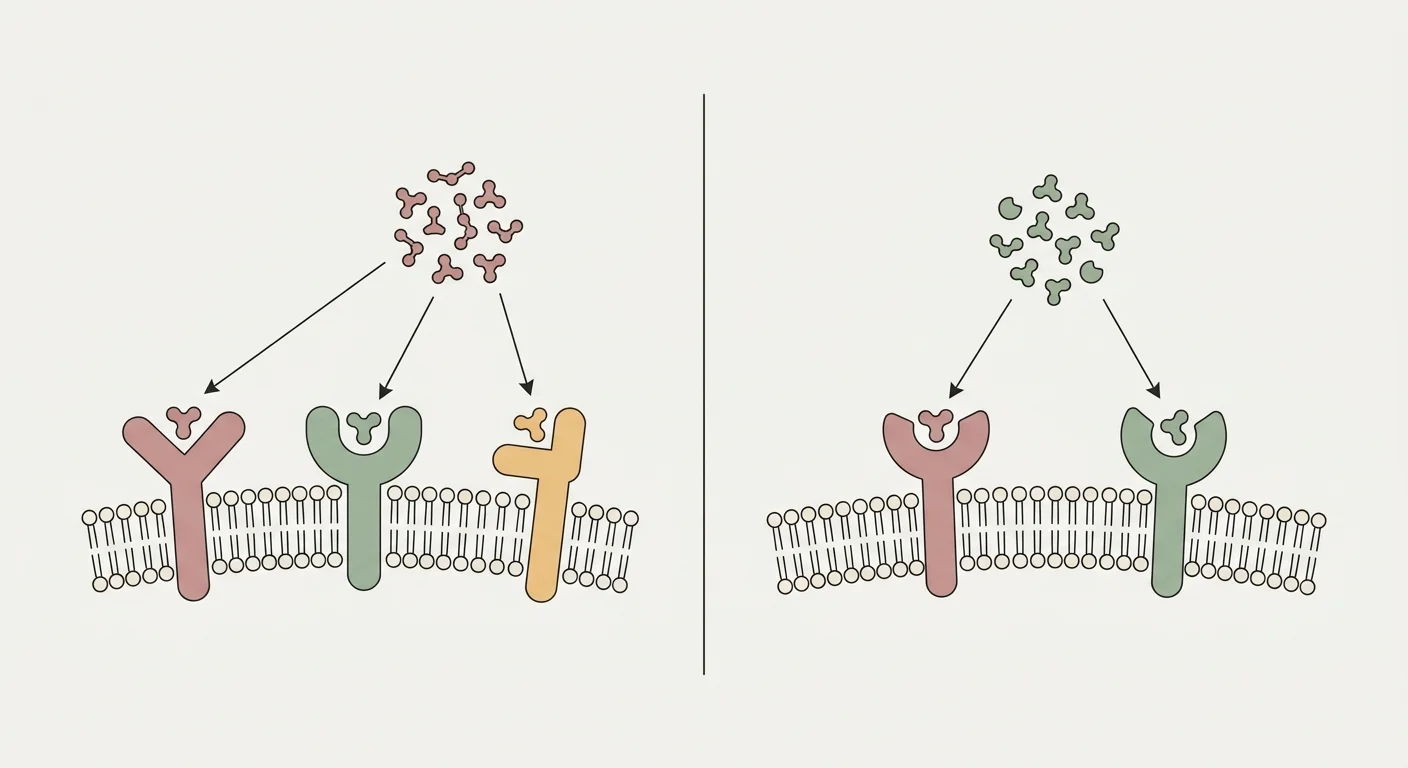
Retatrutid (LY3437943) ist ein einzelnes Peptid, das so konstruiert wurde, dass es drei Rezeptoren der Inkretin-Familie gleichzeitig agonisiert: den Glucagon-like-Peptide-1-Rezeptor (GLP-1R), den Glucose-dependent-Insulinotropic-Polypeptide-Rezeptor (GIPR) und den Glukagonrezeptor (GCGR) 26. Der GLP-1R-Arm steuert die zentrale Appetitsuppression, die verzögerte Magenentleerung und die glukoseabhängige Insulinsekretion, die von Semaglutid und Tirzepatid bekannt sind 24. Der GIPR-Arm fügt synergistische insulinotrope Aktivität hinzu und verbessert im Fettgewebe die gesunde Lipidpufferung, wodurch ektope Fettablagerungen in Leber und Muskulatur reduziert werden 25.
Der unterscheidende Arm ist GCGR. Glukagon wird üblicherweise als gegenregulatorisches Hormon verstanden, das den Blutzucker erhöht; im Kontext eines balancierten Triple-Agonisten wird seine klassische Wirkung auf die hepatische Glukoseproduktion durch die simultane GLP-1R/GIPR-vermittelte Insulinotropie aufgewogen, während die metabolischen Effekte, die Peptid-Designer von GCGR tatsächlich nutzen wollen, erhalten bleiben: gesteigerter Energieumsatz durch Thermogenese im braunen Fettgewebe und Oxidation in der Skelettmuskulatur, Lipolyse im Fettgewebe mit Freisetzung freier Fettsäuren für die Beta-Oxidation sowie hepatische Fettsäureoxidation, die Triglyzeride aus der Leber entfernt 27. In Phase-2a-MASLD-Daten erzielte Retatrutid bei der höchsten Dosis eine Leberfettreduktion von etwa 85–90%; rund 90% der Teilnehmenden unter 12 mg erreichten nach 48 Wochen einen Leberfettanteil unter 5%, eine Größenordnung, die der Dual-Agonismus nicht gezeigt hat 3.
Bis April 2026 wurde keine direkte randomisierte kontrollierte Studie zwischen Retatrutid und Tirzepatid publiziert oder angekündigt. Eine zulassungsrelevante Head-to-Head-Studie (NCT06662383) ist im Pipeline-Tracker von Lilly sichtbar, eine Auswertung wurde jedoch nicht berichtet. Jede vergleichende Aussage in diesem Artikel trägt daher einen Vorbehalt: Sie ist entweder ein indirekter Vergleich über Studien mit unterschiedlichen Populationen, Dosierungsschemata und Endpunkten oder eine mechanistische Extrapolation aus präklinischen und Phase-2-Daten. Das ist kein Grund, das Signal zu ignorieren, sondern ein Grund, es einzuordnen.
Zwei Netzwerk-Metaanalysen haben versucht, die Moleküle auf dieselbe Skala zu stellen. Die im Oktober 2025 im Journal of the Endocrine Society publizierte Analyse (Abstract SUN-659, mit vollständigem peer-reviewten Artikel unter PMC12544991) berichtete für Retatrutid eine mittlere absolute Reduktion von −16,34 kg und −23,77% Körpergewicht gegenüber −11,82 kg und −16,79% für Tirzepatid, ein indirekter Vorteil zugunsten von Retatrutid 20. Dieselbe Analyse markierte ein höheres relatives Risiko für unerwünschte Ereignisse für Retatrutid (RR 4,10 vs. 2,78), konsistent mit einer höheren gastrointestinalen Belastung in den Hochdosen. Eine breitere Sieben-Wirkstoff-Netzwerk-Metaanalyse, publiziert in Metabolism (2024), reihte die Moleküle für Gewichtsverlust wie folgt: Retatrutid 12 mg > Retatrutid 8 mg > Tirzepatid 15 mg, mit konsistenten Rangfolgen über Taillenumfang, HbA1c und Nüchternplasmaglukose hinweg 21.
Beide Netzwerk-Metaanalysen begünstigen Retatrutid numerisch und richtungsweisend, doch das Fehlen direkter RCT-Evidenz bedeutet, dass jede vergleichende Aussage einen Vorbehalt tragen muss. Für Forschungszwecke ist dies ein Anlass für weitere Untersuchung, kein Grund, das Signal zu verwerfen.
Das Phase-2-Sicherheitsprofil entspricht der GLP-1-Rezeptoragonisten-Klasse und wird von dosisabhängigen gastrointestinalen unerwünschten Ereignissen dominiert, die sich auf die ersten ein bis zwei Wochen jedes Eskalationsschritts konzentrieren. Die Phase-3-Sicherheit (TRIUMPH-4) liegt bis April 2026 nur als Top-line aus Pressemitteilungen vor und wurde noch nicht auf Ebene des vollständigen Datensatzes peer-reviewt.
TRIUMPH-4 Top-line berichtet ~28,7% Reduktion nach 68 Wochen und übertrifft den SURMOUNT-1-Höchstwert von Tirzepatid nach 72 Wochen um rund sechs Prozentpunkte. Beide publizierten Netzwerk-Metaanalysen weisen in dieselbe Richtung.
Der GCGR-Arm fügt Pfade hinzu, die Tirzepatid fehlen: hepatische Fettsäureoxidation (~85–90% Leberfettreduktion in Phase 2a MASLD), Lipolyse im Fettgewebe und thermogener Energieumsatz.
Zwölf+ Phase-3-Studien, drei FDA-Zulassungen, ein publiziertes CVOT mit 13.165 Patienten und ein ausgereiftes Sicherheitsprofil aus der Fachinformation. Das Referenzmolekül für die GLP-1/GIP-Forschung von heute.
SURPASS-2 schlug Semaglutid 1 mg im direkten Vergleich beim HbA1c; SURPASS-CVOT ist die einzige publizierte kardiovaskuläre Outcome-Studie für eines der beiden Moleküle. Die T2D-Evidenz für Retatrutid bleibt in Phase 2 (Rosenstock 2023).
Tirzepatid ist ein dualer Agonist an GLP-1R und GIPR; Retatrutid fügt den Glukagonrezeptor (GCGR) als drittes Ziel hinzu 26. Der GCGR-Arm trägt zur hepatischen Fettsäureoxidation, Lipolyse im Fettgewebe und zum thermogenen Energieumsatz bei, die der Dual-Agonismus konstruktionsbedingt nicht aktiviert 27.
Tirzepatid, eindeutig. Zwölf+ Phase-3-Studien, drei FDA-Zulassungen und eine publizierte kardiovaskuläre Outcome-Studie mit 13.165 Patienten 12. Retatrutid hat eine Phase-3-Top-line (TRIUMPH-4) und ein Phase-2-Programm mit rund sechs peer-reviewten Publikationen 1 5. Die Lücke wird sich im Verlauf von 2026 verringern, sobald TRIUMPH-1, TRIUMPH-2 und TRIUMPH-3 ihre Auswertungen vorlegen.
Nein. Bis April 2026 wurde keine direkte RCT zwischen Retatrutid und Tirzepatid publiziert oder öffentlich berichtet. Die vergleichende Evidenz beschränkt sich auf zwei indirekte Netzwerk-Metaanalysen, die beide in Richtung Retatrutid weisen, aber eine Head-to-Head-Studie nicht ersetzen können 20 .
Retatrutid ist unsere Empfehlung. Nicht weil es mehr Studiendaten hat, das hat es nicht. Das Phase-3-Programm von Tirzepatid ist vier Jahre tiefer, seine drei FDA-Zulassungen umfassen Typ-2-Diabetes, chronisches Gewichtsmanagement und obstruktive Schlafapnoe, und seine publizierte kardiovaskuläre Outcome-Studie mit mehr als dreizehntausend Patienten ist ein Faktum, das wir nicht bestreiten 12 28. Für Forschungsprotokolle, die die heute tiefste, am gründlichsten geprüfte Evidenzbasis der Inkretin-Klasse benötigen, ist Tirzepatid das Referenzmolekül und wird es bleiben, bis das TRIUMPH-Programm abgeschlossen ist.
Doch für Forschungsprotokolle, die die höchste therapeutische Obergrenze anstreben, sprechen die Zahlen für Retatrutid. Seine erste Phase-3-Auswertung berichtete eine Gewichtsreduktion von rund 28,7% bei 12 mg über 68 Wochen 5, ein bedeutsamer Sechs-Prozentpunkte-Vorsprung gegenüber dem SURMOUNT-1-Höchstwert von Tirzepatid von 22,5% über 72 Wochen 13. Die mechanistische Erklärung ist nicht spekulativ: Der Glukagonrezeptor fügt hepatische Fettsäureoxidation, Lipolyse im Fettgewebe und thermogenen Energieumsatz hinzu, die der Dual-Agonismus konstruktionsbedingt nicht aktivieren kann 27, und die Leberfettreduktion von 85–90% in der Phase-2a-MASLD-Auswertung ist eine unmittelbare Signatur dieses Pfads 3. Beide publizierten Netzwerk-Metaanalysen weisen in Richtung Retatrutid 20 21. Die Evidenzbasis wird reifen; die Obergrenze wird sich konstruktionsbedingt nicht nach unten bewegen.
Für die Forschungsspitze der metabolischen Peptidtherapie ist Retatrutid der Sieger. Für Protokolle, die regulatorisch belastbare Tiefe über alles stellen, bleibt Tirzepatid der Standard. Das ist eine klarere Rollenverteilung, als die meisten „X vs. Y”-Vergleiche bieten können, und Ehrlichkeit über diese Aufteilung ist nützlicher als ein erzwungener Einzelsieger.
Vorhanden; ~85–90% Leberfettreduktion in Phase 2a MASLD 3
Konstruktionsbedingt nicht vorhanden
~144 h (~6 Tage)
~120 h (~5 Tage)
1 Top-line (TRIUMPH-4); TRIUMPH-1/2/3 ausstehend 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Keine (kein CVOT initiiert)
SURPASS-CVOT (n=13.165; NEJM Dez. 2025) 12
Keine (kein zugelassenes Label)
MTC-Schilddrüsen-C-Zellen (Nager, humane Relevanz nicht etabliert) 28
Keine publiziert
Keine publiziert
Einmal wöchentlich, subkutan
Einmal wöchentlich, subkutan
USA: frühestens Ende 2027 (NDA frühestens Q4 2026) 22
Bereits zugelassen (USA: 2022/2023/2024; EU: 2022/2024)
Lyophilisiert; Rekonstitution mit BAC-Wasser; 2–8 °C
Lyophilisiert; Rekonstitution mit BAC-Wasser; 2–8 °C
Höhere Obergrenze + Glukagonrezeptor-Breite
Niedrigere Obergrenze; bestcharakterisiertes Sicherheitsprofil
Tirzepatid (LY3298176) ist ein dualer GLP-1R/GIPR-Agonist, ein einzelnes 39-Aminosäuren-Peptid, das so abgestimmt wurde, dass es beide Inkretinrezeptoren mit vergleichbarer Potenz aktiviert. Der GLP-1R-Arm trägt denselben Kernmechanismus bei, den die erste Generation der GLP-1-Analoga bekannt gemacht hat: glukoseabhängige Insulinsekretion, Suppression der Glukagonausschüttung aus Alpha-Zellen, hypothalamische Appetitregulation und verlangsamte Magenentleerung 24.
Was Tirzepatid von reinen GLP-1-Agonisten unterscheidet, ist die zusätzliche GIPR-Aktivität. Präklinisch erzeugt die Koadministration von GIP mit GLP-1 additive und in einigen Endpunkten synergistische Reduktionen von Körpergewicht und Glukose, mehr als jeder Agonist allein 25. Die zentrale GIPR-Aktivierung scheint die GLP-1-induzierte Anorexie über hypothalamisches POMC-Signalling zu potenzieren; die periphere GIPR-Aktivierung im weißen Fettgewebe steigert die Pufferkapazität des Depots und verringert den Bedarf an ektoper Fettablagerung. Die beobachtbare Konsequenz ist das potenteste Gewichts- und Glukose-senkende Profil aller vor Retatrutid zugelassenen Moleküle: SURMOUNT-1 berichtete unter 15 mg über 72 Wochen eine Gewichtsreduktion von rund 22,5% 13, und SURMOUNT-5 zeigte Tirzepatid im direkten Vergleich nach 72 Wochen Semaglutid 2,4 mg überlegen (−20,2% vs. −13,7%) 18.
Der Glukagonrezeptor-Arm ist das mechanistische Differenzierungsmerkmal von Retatrutid. Präklinische und Phase-2-Daten legen nahe, dass dies in lipidsenkende, leberfettreduzierende und energieumsatzsteigernde Effekte übersetzt wird, die Tirzepatid konstruktionsbedingt nicht aufweist. Ob daraus der direkte Vergleichsvorteil entsteht, den Netzwerk-Metaanalysen suggerieren, bleibt offen, bis eine Head-to-Head-RCT vorliegt; bis April 2026 wurde keine angekündigt.
Die Evidenztiefe von Tirzepatid ist heute unerreicht: zwölf Phase-3-Studien über zwei Krankheitsprogramme, eine publizierte kardiovaskuläre Outcome-Studie mit mehr als dreizehntausend Patienten und drei FDA-Zulassungen im Label. Die verfügbare Auswertung von Retatrutid übertrifft, obwohl singulär, die beste Phase-3-Obergrenze von Tirzepatid bei einem kürzeren Beobachtungsfenster. Das ist ein Signal, das ernsthafte Aufmerksamkeit verdient, während TRIUMPH-1, TRIUMPH-2 und TRIUMPH-3 im Verlauf von 2026 und 2027 reifen.
Ausgereiftes Sicherheitsprofil aus der Fachinformation für Mounjaro und Zepbound. Häufige UE entsprechen der GLP-1-Klasse und konzentrieren sich auf die Dosiseskalation; ernsthafte Risiken sind in einer Boxed Warning sowie in einer Reihe von Warnhinweisen und Vorsichtsmaßnahmen erfasst, die durch die Postmarketing-Überwachung verfeinert wurden (FAERS-Analyse 2024 und EMA-Pharmakovigilanz).
Dieser Artikel ist ein redaktioneller Vergleich, der für Leserinnen und Leser im Forschungskontext erstellt wurde. Weder Retatrutid noch Tirzepatid wird über diese Seite zur Selbstanwendung am Menschen angeboten oder empfohlen. Wo Tirzepatid verschrieben wird, ist es ausschließlich unter ärztlicher Aufsicht in Rechtsräumen erhältlich, in denen es zugelassen ist (Mounjaro für T2D; Zepbound für chronisches Gewichtsmanagement und obstruktive Schlafapnoe). Retatrutid ist Stand April 2026 weltweit in der Prüfphase und sollte ausschließlich innerhalb geeigneter Forschungsprotokolle gehandhabt werden.
Die hier zusammengefassten Sicherheitsdaten spiegeln publizierte Phase-2- und Phase-3-Datensätze sowie aktuelle Fachinformationen wider. Neue Signale können jederzeit auftreten; das Datum lastUpdated auf dieser Seite kennzeichnet den Stichtag unserer Auswertung. Nichts auf dieser Seite stellt eine medizinische Beratung oder einen Ersatz für die Konsultation einer qualifizierten Klinikerin oder eines qualifizierten Klinikers dar.
Tirzepatid ist unter zwei Markennamen zugelassen: Mounjaro für Typ-2-Diabetes (FDA Mai 2022) und Zepbound für chronisches Gewichtsmanagement (November 2023) sowie für mittelschwere bis schwere obstruktive Schlafapnoe mit Adipositas (Dezember 2024) 28. Retatrutid ist überall in der Prüfphase; bis April 2026 wurde keine NDA eingereicht 22.
Retatrutid, basierend auf den verfügbaren Daten. TRIUMPH-4 berichtete ~−28,7% bei 12 mg über 68 Wochen 5; die beste Phase-3-Adipositas-Auswertung von Tirzepatid, SURMOUNT-1 bei 15 mg über 72 Wochen, betrug ~−22,5% 13. Beide publizierten Netzwerk-Metaanalysen reihen Retatrutid bei der Gewichtsreduktion höher ein 20 21.
Auf Klassenebene haben beide ein GI-dominantes Profil (Übelkeit, Erbrechen, Diarrhoe), das sich auf die Dosiseskalation konzentriert. Die Netzwerk-Metaanalyse vom Oktober 2025 berichtete ein höheres relatives Risiko für unerwünschte Ereignisse für Retatrutid (RR 4,10) als für Tirzepatid (RR 2,78), konsistent mit höherer GI-Belastung in den Hochdosen 20. Tirzepatid trägt eine MTC-Boxed-Warning sowie ein charakterisiertes Pankreatitis-, Gallenblasen- und Überempfindlichkeitsprofil 28 29; das analoge Langzeit-Sicherheitsprofil von Retatrutid ist nicht etabliert.
Die publizierten Phase-2- und Phase-3-Studien für beide Moleküle rekrutieren als Monotherapie (mit oder ohne T2D-Begleittherapie wie Metformin oder Insulin). Es gibt keine publizierte Evidenz zum Stacking mit anderen Forschungspeptiden. Jedes Kombinationsprotokoll ist strikt prüfungsorientiert und außerhalb der in diesem Artikel zusammengefassten Evidenzbasis.
Die Halbwertszeit von Retatrutid (~144 Stunden) und die von Tirzepatid (~120 Stunden) stützen beide eine einzelne wöchentliche subkutane Dosis, das Schema, das in jeder zulassungsrelevanten Studie verwendet wurde. Die etwas längere Halbwertszeit von Retatrutid bietet einen geringen Puffer gegen die Variabilität ausgelassener Dosen, ändert aber nichts am grundsätzlich wöchentlichen Rhythmus.
Ja. Sowohl Retatrutid als auch Tirzepatid sind in den EU- und US-Kanälen für die Forschungsanwendung gelistet. Verfügbarkeit, Vialgrößen und kanalspezifische Preise werden auf der Detailseite des jeweiligen Produkts angezeigt.
Die Auswertungen von TRIUMPH-1 (Adipositas ohne T2D), TRIUMPH-2 (Adipositas mit T2D) und TRIUMPH-3 (Adipositas mit etablierter kardiovaskulärer Erkrankung) werden gemäß den Angaben von Lilly im Verlauf von 2026 erwartet 4. Jede wird die Evidenzbasis von Retatrutid wesentlich erweitern; gemeinsam werden sie bestimmen, ob die TRIUMPH-4-Obergrenze über Populationen hinweg generalisiert und ob eine NDA-Einreichung gegenüber dem aktuellen frühestmöglichen Fenster Q4 2026 vorgezogen werden kann.
Retatrutid gewinnt in den Dimensionen, die für die Spitzenforschung am wichtigsten sind: höhere beobachtete Obergrenze in TRIUMPH-4, Mechanismusbreite des Triple-Agonisten und konsistente Richtung beider publizierten Netzwerk-Metaanalysen. Tirzepatid bleibt das Referenzmolekül für Protokolle, die heute die tiefste publizierte Evidenzbasis benötigen.