

A hármas agonista, amely új plafont állított fel, szemben a kettős agonistával, amely megalapozta a kategóriát. Összehasonlítás olyan kutatási protokollokhoz, amelyek pontosan tudni akarják, melyik molekula a frontvonal, melyik a sztenderd, és miért számít ez a különbség.

A tirzepatid (az Eli Lilly Mounjaro/Zepbound készítménye) kettős GLP-1/GIP receptor agonista, amely mögött négy év III. fázisú adat, három FDA-engedély és egy publikált kardiovaszkuláris kimeneti vizsgálat áll. A retatrutid, a Lilly következő molekulája, hármas agonista, amely ugyanahhoz a kettős gerinchez hozzáadja a glukagon receptort, és első III. fázisú eredményében a regisztrációs obesitás vizsgálatok történetében valaha jelentett legmélyebb testsúlycsökkenést produkálta: körülbelül 28,7% 68 hét alatt 5 szemben a tirzepatid SURMOUNT-1 csúcsával, amely körülbelül 22,5% volt 72 hét alatt 13.
A bizonyítékbázisok nem szimmetrikusak. A tirzepatid mögött kiérlelt, peer-reviewed dokumentáció áll. A retatrutidnak magasabb a megfigyelt plafonja, mechanisztikusan szélesebb a célprofilja, és két hálózati metaanalízis is az ő irányába mutat 20 21. Olyan kutatási protokollokhoz, amelyek a maximális terápiás plafont és a mechanisztikus szélességet helyezik előtérbe, szerkesztőségi választásunk a retatrutid. Olyan protokollokhoz, amelyek a regisztrációs szintű bizonyítékmélységet és a kiforrott biztonsági címkét értékelik, a tirzepatid marad a referenciamolekula.
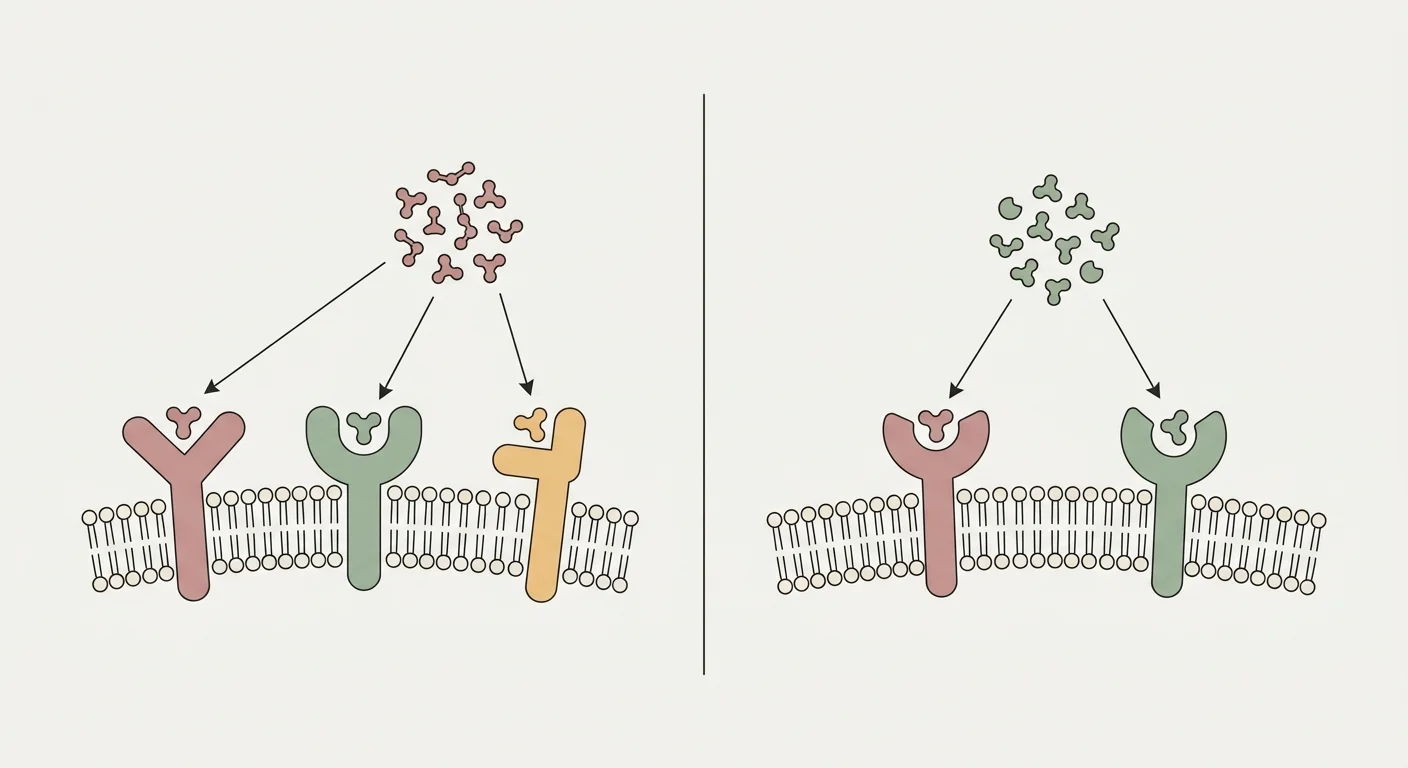
A retatrutid (LY3437943) egyetlen peptid, amelyet úgy terveztek, hogy egyszerre három inkretin-családbeli receptort agonizáljon: a glukagon-szerű peptid-1 receptort (GLP-1R), a glükóz-függő inzulinotrop polipeptid receptort (GIPR) és a glukagon receptort (GCGR) 26. A GLP-1R kar hozza a központi étvágycsökkenést, a lassított gyomorürülést és a glükóz-függő inzulinszekréciót, amit már a szemaglutidtól és a tirzepatidtól ismerünk 24. A GIPR kar szinergisztikus inzulinotrop aktivitást ad hozzá, és a zsírszövetben fokozza az egészséges lipidpufferelést, csökkentve a májban és az izomban a heterotopikus zsírlerakódást 25.
A megkülönböztető kar a GCGR. A glukagont általában úgy szokás bemutatni, mint a vércukorszintet emelő ellenregulációs hormont; egy kiegyensúlyozott hármas agonista kontextusában a hepatikus glükóztermelésre gyakorolt klasszikus hatását ellensúlyozza a párhuzamos GLP-1R/GIPR inzulinotrop hatás, miközben megmaradnak azok a metabolikus hatások, amelyeket a peptidtervezők valójában kívánnak a GCGR-től: megnövekedett energiakiadás a barna zsír termogenezise és a vázizom-oxidáció révén, a zsírszövet lipolízise szabad zsírsav-felszabadulással a béta-oxidáció számára, valamint a hepatikus zsírsav-oxidáció, amely tisztítja a májat a trigliceridtől 27. A 2a fázisú MASLD adatokban a retatrutid a felső dózisnál körülbelül 85–90%-os májzsír-csökkenést produkált; a 12 mg-os résztvevők mintegy 90%-a 48 hét alatt 5% alatti májzsír-szintet ért el, ami olyan nagyságrend, amit a kettős agonizmus nem mutatott 3.
2026 áprilisáig nem publikáltak, és nem is jelentettek be közvetlen, retatrutid-vs-tirzepatid randomizált, kontrollált vizsgálatot. A Lilly pipeline trackerében szerepel egy regisztrációs head-to-head vizsgálat (NCT06662383), de eredményt eddig nem közöltek. Minden összehasonlító állítás ebben a cikkben tehát fenntartással kísért: vagy különböző populációkon, dozírozási ütemezésekkel és végpontokkal végzett vizsgálatok közötti indirekt összehasonlítás, vagy mechanisztikus extrapoláció preklinikai és II. fázisú adatokból. Ez nem ok arra, hogy figyelmen kívül hagyjuk a szignált — arra ok, hogy árnyaltan kezeljük.
Két hálózati metaanalízis próbálta a két molekulát ugyanarra a skálára helyezni. A 2025 októberi, Journal of the Endocrine Society lapban publikált elemzés (SUN-659 absztrakt, a teljes peer-reviewed cikk PMC12544991 azonosítóval) a retatrutidnál −16,34 kg és −23,77% átlagos abszolút testsúlycsökkenést jelzett, szemben a tirzepatid −11,82 kg és −16,79% értékével — indirekt előny a retatrutid javára 20. Ugyanez az elemzés magasabb mellékhatás-relatív kockázatot jelzett a retatrutidra (RR 4,10 vs 2,78), ami konzisztens a felső dózisokon észlelt nagyobb gasztrointesztinális teherrel. Egy szélesebb, hét hatóanyagra kiterjedő hálózati metaanalízis a Metabolism folyóiratban (2024) a testsúlycsökkenés szempontjából a következő rangsort állította fel: retatrutid 12 mg > retatrutid 8 mg > tirzepatid 15 mg, konzisztens rangsorral haskörfogatra, HbA1c-re és éhgyomri plazma glükózra 21.
Mindkét hálózati metaanalízis számszerűen és irányában is a retatrutidot támogatja, de a közvetlen RCT bizonyíték hiánya miatt minden összehasonlító állítást fenntartással kell kezelni. Kutatási célból ez ok a további vizsgálódásra, nem pedig arra, hogy a szignált elvessük.
A II. fázisú biztonsági profil konzisztens a GLP-1 receptor agonista osztállyal: a dózisfüggő gasztrointesztinális mellékhatások dominálnak, amelyek minden eszkalációs lépcső első egy-két hetére koncentrálódnak. A III. fázisú biztonság (TRIUMPH-4) 2026 áprilisáig csak press-release top-line-ként elérhető, és teljes adatszintű peer-review még nem készült róla.
A TRIUMPH-4 top-line ~28,7% csökkenést jelent 68 hét alatt, ami körülbelül hat százalékponttal meghaladja a tirzepatid SURMOUNT-1 csúcsát 72 hét alatt. Mindkét publikált hálózati metaanalízis ugyanebbe az irányba mutat.
A GCGR kar olyan útvonalakat ad hozzá, amelyek a tirzepatidnál hiányoznak: hepatikus zsírsav-oxidáció (~85–90% májzsír-csökkenés a 2a fázisú MASLD vizsgálatban), a zsírszövet lipolízise és termogenikus energiakiadás.
Tizenkettőnél több III. fázisú vizsgálat, három FDA-engedély, egy publikált CVOT 13 165 betegen, és kiforrott prescribing-information biztonsági burok. Ma a GLP-1/GIP kutatás referenciamolekulája.
A SURPASS-2 head-to-head verte az 1 mg szemaglutidot HbA1c-ben; a SURPASS-CVOT az egyetlen publikált kardiovaszkuláris kimeneti vizsgálat a két molekula között. A retatrutid T2D-bizonyítéka II. fázisú szinten áll (Rosenstock 2023).
Egyértelműen a tirzepatidhoz. Tizenkettőnél több III. fázisú vizsgálat, három FDA-engedély és egy publikált kardiovaszkuláris kimeneti vizsgálat 13 165 betegen 12. A retatrutidnak egy III. fázisú top-line eredménye van (TRIUMPH-4) és egy II. fázisú program nagyjából hat peer-reviewed publikációval 1 5. A különbség 2026 folyamán szűkülni fog, ahogy a TRIUMPH-1, TRIUMPH-2 és TRIUMPH-3 eredményt közöl.
Nincs. 2026 áprilisáig nem publikáltak, és nem is jelentettek be nyilvánosan közvetlen, retatrutid-vs-tirzepatid RCT-t. Az összehasonlító bizonyíték két indirekt hálózati metaanalízisre korlátozódik, amelyek mindkettő a retatrutid irányába mutat, de nem helyettesítheti a head-to-head vizsgálatot 20 .
A retatrutid a választásunk. Nem azért, mert mögötte több vizsgálati adat áll — nem így van. A tirzepatid III. fázisú programja négy évvel mélyebb, három FDA-engedélye átfogja a 2-es típusú diabéteszt, a krónikus testsúly-menedzsmentet és az obstruktív alvási apnoét, a több mint tizenháromezer betegen futott publikált kardiovaszkuláris kimeneti vizsgálata pedig olyan tény, amelyet nem vitatunk 12 28. Olyan kutatási protokollokhoz, amelyek a ma az inkretin-osztályban elérhető legmélyebb, legalaposabban átvizsgált bizonyítékbázist igénylik, a tirzepatid a referenciamolekula, és az is marad, amíg a TRIUMPH program le nem zárul.
Olyan kutatási protokollokhoz azonban, amelyek a legmagasabb terápiás plafont keresik, a számok a retatrutidnak kedveznek. Első III. fázisú eredménye 12 mg-nál 68 hét alatt körülbelül 28,7%-os testsúlycsökkenést jelentett 5— érdemi, hat százalékpontos plafonelőny a tirzepatid SURMOUNT-1 csúcsával szemben, amely 72 hét alatt 22,5% volt 13. A mechanisztikus magyarázat nem spekulatív: a glukagon receptor olyan hepatikus zsírsav-oxidációt, zsírszöveti lipolízist és termogenikus energiakiadást ad hozzá, amelyeket a kettős agonizmus tervezésénél fogva nem érint 27, és a 2a fázisú MASLD eredmény 85–90%-os májzsír-csökkenése ennek az útvonalnak közvetlen ujjlenyomata 3. Mindkét publikált hálózati metaanalízis a retatrutid irányába mutat 20 21. A bizonyítékbázis kiérik; a plafon, tervezésénél fogva, nem fog lejjebb mozdulni.
A metabolikus peptidterápia kutatási frontvonalán a retatrutid a győztes. Olyan protokollokhoz, amelyek a regisztrációs szintű mélységet mindenek fölé helyezik, a tirzepatid marad a sztenderd. Ez tisztább szereposztás, mint amit a legtöbb „X vs Y” összehasonlítás kínálni tud, és az őszinteség a megosztásról hasznosabb, mint egy erőltetett egyetlen győztes.
Jelen van; ~85–90% májzsír-csökkenés a 2a fázisú MASLD vizsgálatban 3
Tervezésből hiányzik
~144 ó (~6 nap)
~120 ó (~5 nap)
1 top-line eredmény (TRIUMPH-4); TRIUMPH-1/2/3 folyamatban 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Nincs (CVOT-ot nem indítottak)
SURPASS-CVOT (n=13 165; NEJM 2025. dec.) 12
Nincs (nincs engedélyezett címke)
MTC pajzsmirigy C-sejt (rágcsáló, humán relevancia nincs igazolva) 28
Nincs publikálva
Nincs publikálva
Heti egyszer, szubkután
Heti egyszer, szubkután
USA: legkorábban 2027 vége (NDA legkorábban 2026 Q4) 22
Már engedélyezett (USA: 2022/2023/2024; EU: 2022/2024)
Liofilizált; BAC-vízzel rekonstituálva; 2–8 °C
Liofilizált; BAC-vízzel rekonstituálva; 2–8 °C
Magasabb plafon + glukagon-receptor szélesség
Alacsonyabb plafon; legjobban jellemzett biztonsági burok
A tirzepatid (LY3298176) kettős GLP-1R / GIPR agonista — egyetlen 39 aminosavból álló peptid, amelyet úgy hangoltak, hogy mindkét inkretin receptorhoz hasonló potenciával kötődjön. A GLP-1R kar ugyanazt az alapmechanizmust adja, amit a GLP-1 analógok első generációjából már ismerünk: glükóz-függő inzulinszekréció, alfa-sejtes glukagon-szuppresszió, hipotalamikus étvágyszabályozás és lassított gyomorürülés 24.
Ami a tirzepatidot a tiszta GLP-1 agonistáktól megkülönbözteti, az a hozzáadott GIPR aktivitás. Preklinikai vizsgálatokban a GIP és a GLP-1 együttes adagolása additív, sőt egyes mérésekben szinergisztikus testsúly- és vércukor-csökkenést eredményez, amely meghaladja bármelyik komponens önállóan elérhető hatását 25. A központi GIPR-aktiváció láthatólag fokozza a GLP-1 által kiváltott anorexiát a hipotalamikus POMC-jelátvitelen keresztül; a fehér zsírszövetben zajló perifériás GIPR-aktiváció pedig javítja a depó pufferelési képességét, és csökkenti a heterotopikus lerakódás szükségességét. Ennek megfigyelhető következménye a retatrutid előtt engedélyezett bármely molekula legpotensebb testsúly- és vércukor-csökkentő profilja: a SURMOUNT-1 a 15 mg-os dózisnál 72 hét alatt körülbelül 22,5%-os testsúlycsökkenést jelentett 13, a SURMOUNT-5 pedig 72 hét alatt head-to-head összehasonlításban a tirzepatidot a 2,4 mg-os szemaglutiddal szemben felülmúlónak találta (−20,2% vs −13,7%) 18.
A glukagon-receptor kar a retatrutid mechanisztikus megkülönböztetője. A preklinikai és II. fázisú adatok arra utalnak, hogy ez lipidcsökkentő, májzsírt redukáló és energiakiadást fokozó hatásokra fordítódik le, amelyek a tirzepatidnál tervezésüknél fogva hiányoznak. Hogy ez lefordítható-e a hálózati metaanalízisek által sugalmazott közvetlen összehasonlítási előnnyé, addig nyitott kérdés marad, amíg egy head-to-head RCT eredményt nem közöl — ami 2026 áprilisáig még nem hangzott el.
A tirzepatid bizonyítékmélysége ma páratlan — tizenkét III. fázisú vizsgálat két betegségprogram keretében, egy publikált kardiovaszkuláris kimeneti vizsgálat több mint tizenháromezer betegen, és három FDA-engedély a címkén. A retatrutid jelenleg elérhető eredménye, bár egyedülálló, rövidebb megfigyelési ablakon belül felülmúlja a tirzepatid legjobb III. fázisú plafonját. Ez olyan szignál, amely komoly figyelmet érdemel, miközben a TRIUMPH-1, TRIUMPH-2 és TRIUMPH-3 vizsgálatok 2026 és 2027 során beérnek.
Kiforrott prescribing-information biztonsági burok a Mounjaro és Zepbound között. A gyakori mellékhatások a GLP-1 osztályét tükrözik, és a dóziseszkaláció során koncentrálódnak; a súlyos kockázatokat boxed warning és figyelmeztetések, óvintézkedések rögzítik, amelyeket forgalombahozatal utáni felügyelet finomított (FAERS 2024-es elemzés és EMA farmakovigilancia).
Ez a cikk szerkesztőségi összehasonlítás, amely kutatási kontextusban olvasó közönségnek készült. Sem a retatrutidot, sem a tirzepatidot nem ajánljuk és nem kínáljuk humán öngyógyszerelésre ezen az oldalon keresztül. Ahol a tirzepatid felírható, ott csak orvosi felügyelet mellett érhető el azokban a joghatóságokban, ahol engedélyezték (Mounjaro T2D-re; Zepbound krónikus testsúly-menedzsmentre és obstruktív alvási apnoéra). A retatrutid 2026 áprilisáig globálisan vizsgálati készítmény, és csak megfelelő kutatási protokollok keretein belül kezelhető.
Az itt összefoglalt biztonsági adatok a publikált II. és III. fázisú adatkészleteket és a jelenlegi prescribing information dokumentumokat tükrözik. Új szignálok bármikor felmerülhetnek; az oldal lastUpdated dátuma jelzi az áttekintés zárónapját. Ezen az oldalon semmi nem minősül orvosi tanácsnak vagy minősített klinikus konzultációjának helyettesítőjének.
A tirzepatid két márkanév alatt engedélyezett: a Mounjaro 2-es típusú diabéteszre (FDA, 2022. május) és a Zepbound krónikus testsúly-menedzsmentre (2023. november), valamint közepes-súlyos obstruktív alvási apnoéra obesitással (2024. december) 28. A retatrutid mindenhol vizsgálati készítmény; 2026 áprilisáig nem nyújtottak be NDA-t 22.
A retatrutidé, az elérhető adatok alapján. A TRIUMPH-4 ~−28,7%-ot jelent 12 mg-nál 68 hét alatt 5; a tirzepatid legjobb III. fázisú obesitás-eredménye, a SURMOUNT-1 15 mg-nál 72 hét alatt, ~−22,5% volt 13. Mindkét publikált hálózati metaanalízis a retatrutidot rangsorolja előrébb a testsúlycsökkenés szempontjából 20 21.
Osztályszinten mindkettő GI-domináns profilú (hányinger, hányás, hasmenés), amely a dóziseszkaláció során koncentrálódik. A 2025 októberi hálózati metaanalízis magasabb mellékhatás-relatív kockázatot jelzett a retatrutidra (RR 4,10), mint a tirzepatidra (RR 2,78), ami konzisztens a felső dózisokon észlelt nagyobb GI-teherrel 20. A tirzepatid boxed MTC-figyelmeztetést és jellemzett pankreatitisz / epehólyag / túlérzékenységi profilt visel 28 29; a retatrutid analóg, hosszú távú biztonsági burka még nem alakult ki.
A két molekula publikált II. és III. fázisú vizsgálatai monoterápiaként (T2D háttérterápiával, például metforminnal vagy inzulinnal vagy anélkül) toborozzák a résztvevőket. Nincs publikált bizonyíték arról, hogy bármelyiket más kutatási peptidekkel együtt alkalmaznák. Bármilyen kombinációs protokoll szigorúan vizsgálati jellegű, és kívül esik az ebben a cikkben összefoglalt bizonyítékbázison.
A retatrutid ~144 órás és a tirzepatid ~120 órás felezési ideje egyaránt támogatja a heti egyszeri szubkután adagolást, ami minden regisztrációs vizsgálat ütemezése volt. A retatrutid valamivel hosszabb felezési ideje szerény pufferolást ad a kihagyott dózisok variabilitása ellen, de nem változtat a heti egyszeri alapritmuson.
Igen. Mind a retatrutid, mind a tirzepatid kutatási célra fel van listázva mind az EU, mind az US csatornán. Az elérhetőség, üvegcseméretek és csatorna-specifikus árazás minden termék részletes oldalán látható.
A TRIUMPH-1 (obesitás T2D nélkül), TRIUMPH-2 (obesitás T2D-vel) és TRIUMPH-3 (obesitás megalapozott kardiovaszkuláris betegséggel) eredményei a Lilly iránymutatása szerint 2026 folyamán várhatók 4. Mindegyik érdemben kibővíti a retatrutid bizonyítékbázisát; együttesen eldöntik, hogy a TRIUMPH-4 plafonja általánosítható-e populációkon át, és hogy az NDA-benyújtás előbbre kerül-e a jelenlegi, legkorábbi 2026 Q4-es ablakból.
A retatrutid a frontvonal-kutatás szempontjából legfontosabb dimenziókban győz: magasabb megfigyelt plafon a TRIUMPH-4-ben, hármas agonista mechanisztikus szélesség, és konzisztens irány mindkét publikált hálózati metaanalízisben. A tirzepatid marad a referenciamolekula olyan protokollokhoz, amelyek a ma elérhető legmélyebb publikált bizonyítékbázist igénylik.