

Trójagonista, który wyznaczył nowy pułap, kontra dwuagonista, który zbudował całą kategorię. Porównanie dla protokołów badawczych, w których chce się rozumieć, która cząsteczka stanowi granicę możliwości, która jest standardem i dlaczego to rozróżnienie ma znaczenie.

Tyrzepatyd (Mounjaro/Zepbound firmy Eli Lilly) jest dwuagonistą receptorów GLP-1 i GIP, opartym na czterech latach danych z badań fazy 3, mającym trzy rejestracje FDA oraz opublikowane badanie nad punktami końcowymi sercowo-naczyniowymi. Retatrutyd, kolejna cząsteczka Lilly’ego, to trójagonista, który dodaje receptor glukagonu do tego samego dualnego rdzenia i w pierwszym odczycie fazy 3 osiągnął najgłębszą redukcję masy ciała kiedykolwiek raportowaną w rejestracyjnym badaniu nad otyłością: około 28,7% w 68. tygodniu 5 w porównaniu z maksymalną wartością tyrzepatydu w SURMOUNT-1 wynoszącą około 22,5% w 72. tygodniu 13.
Bazy dowodowe nie są symetryczne. Tyrzepatyd dysponuje dojrzałym, recenzowanym dossier. Retatrutyd ma wyższy obserwowany pułap, mechanistycznie szerszy profil punktu uchwytu oraz dwie sieciowe metaanalizy, które wskazują na jego korzyść 20 21. Dla protokołów badawczych priorytetyzujących maksymalny pułap terapeutyczny i szerokość mechanizmu naszym redakcyjnym wyborem jest retatrutyd. Dla protokołów ceniących głębię dowodów na poziomie regulacyjnym oraz ustabilizowaną etykietę bezpieczeństwa tyrzepatyd pozostaje cząsteczką referencyjną.
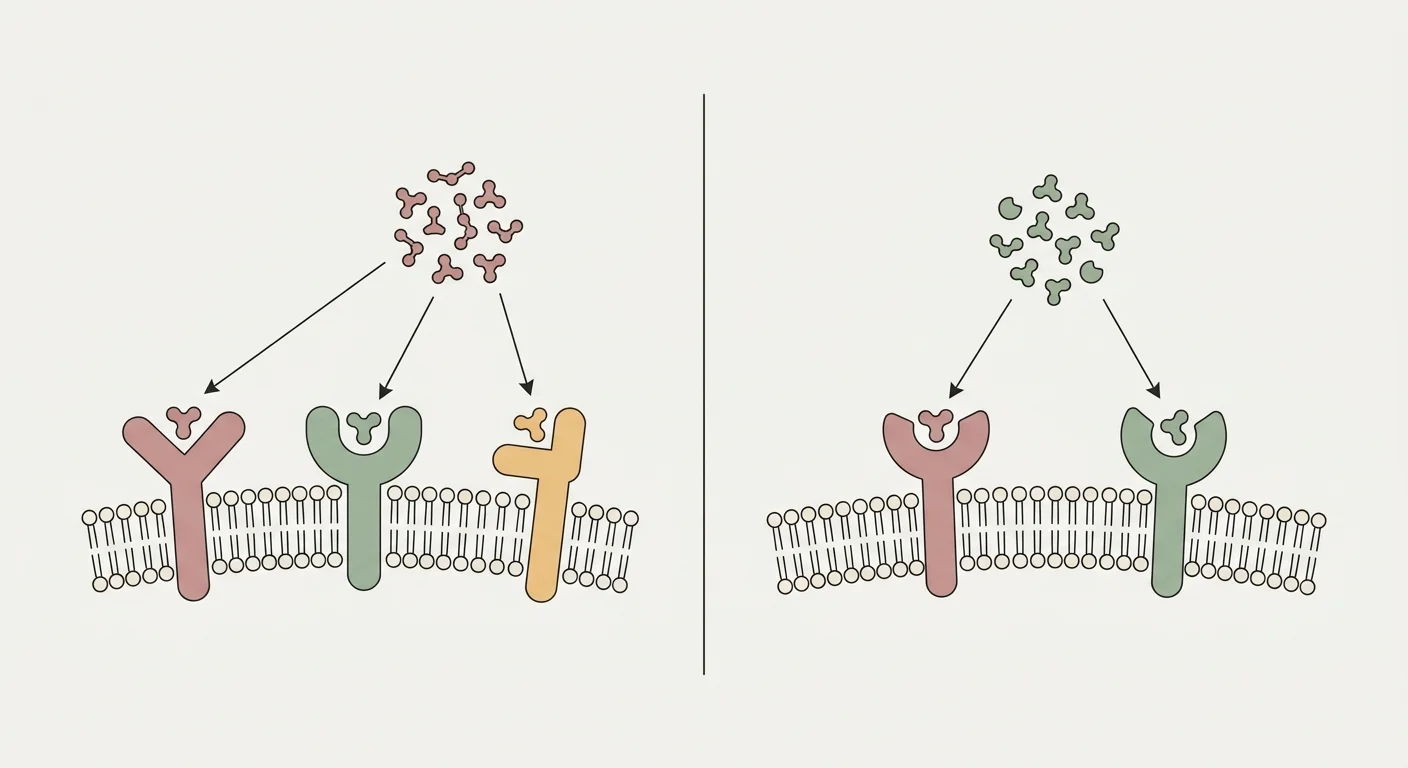
Retatrutyd (LY3437943) jest pojedynczym peptydem zaprojektowanym tak, aby równocześnie agonizować trzy receptory z rodziny inkretynowej: receptor peptydu glukagonopodobnego-1 (GLP-1R), receptor żołądkowego peptydu insulinotropowego (GIPR) oraz receptor glukagonu (GCGR) 26. Ramię GLP-1R odpowiada za centralne hamowanie apetytu, opóźnienie opróżniania żołądka i zależne od glukozy wydzielanie insuliny, znane z semaglutydu i tyrzepatydu 24. Ramię GIPR dodaje synergistyczną aktywność insulinotropową, a w tkance tłuszczowej wzmaga zdrowe buforowanie lipidów, ograniczając ektopowe odkładanie tłuszczu w wątrobie i mięśniach 25.
Wyróżniającym ramieniem jest GCGR. Glukagon przedstawia się zwykle jako hormon kontrregulacyjny podnoszący poziom glukozy we krwi; w kontekście zrównoważonego trójagonisty jego klasyczny wpływ na wątrobową produkcję glukozy jest równoważony przez równoczesne działanie insulinotropowe GLP-1R/GIPR, podczas gdy zachowane zostają te efekty metaboliczne, które konstruktorzy peptydów rzeczywiście chcą uzyskać z GCGR: zwiększony wydatek energetyczny przez termogenezę brunatnej tkanki tłuszczowej i utlenianie w mięśniach szkieletowych, lipoliza tkanki tłuszczowej z uwalnianiem wolnych kwasów tłuszczowych dla beta-oksydacji oraz wątrobowe utlenianie kwasów tłuszczowych usuwające triglicerydy z wątroby 27. W danych z fazy 2a w MASLD retatrutyd wywołał około 85–90% redukcję tłuszczu wątrobowego przy najwyższej dawce; około 90% uczestników otrzymujących 12 mg uzyskało zawartość tłuszczu w wątrobie poniżej 5% w 48. tygodniu, czego skali agonizm podwójny nie wykazał 3.
Według stanu na kwiecień 2026 r. nie opublikowano ani nie ogłoszono żadnego bezpośredniego, randomizowanego badania kontrolowanego porównującego retatrutyd z tyrzepatydem. Rejestracyjne badanie head-to-head (NCT06662383) jest widoczne w pipeline’ie firmy Lilly, lecz odczytu nie przedstawiono. Każde stwierdzenie porównawcze w niniejszym artykule wiąże się zatem z zastrzeżeniem: jest to albo porównanie pośrednie pomiędzy badaniami o różnych populacjach, schematach dawkowania i punktach końcowych, albo ekstrapolacja mechanistyczna z danych przedklinicznych i fazy 2. To nie powód, aby ignorować sygnał — to powód, aby go opatrzyć kwalifikacją.
Dwie sieciowe metaanalizy podjęły próbę umieszczenia tych cząsteczek na tej samej skali. Analiza z października 2025 r. opublikowana w Journal of the Endocrine Society (abstrakt SUN-659, z pełnym recenzowanym artykułem dostępnym w PMC12544991) raportowała dla retatrutydu średnią bezwzględną redukcję −16,34 kg i −23,77% masy ciała wobec −11,82 kg i −16,79% dla tyrzepatydu, czyli pośrednią przewagę na korzyść retatrutydu 20. Ta sama analiza odnotowała wyższe ryzyko względne zdarzeń niepożądanych dla retatrutydu (RR 4,10 vs 2,78), spójne z wyższym obciążeniem ze strony przewodu pokarmowego przy najwyższych dawkach. Szersza, siedmioskładnikowa sieciowa metaanaliza opublikowana w czasopiśmie Metabolism (2024) uszeregowała cząsteczki pod względem utraty masy ciała następująco: retatrutyd 12 mg > retatrutyd 8 mg > tyrzepatyd 15 mg, ze spójnymi rankingami w odniesieniu do obwodu talii, HbA1c i glukozy w osoczu na czczo 21.
Obie sieciowe metaanalizy faworyzują retatrutyd liczbowo i kierunkowo, lecz brak bezpośrednich dowodów z RCT oznacza, że każde stwierdzenie porównawcze musi być opatrzone zastrzeżeniem. Z perspektywy badawczej jest to powód do dalszych dociekań, a nie do odrzucenia sygnału.
Profil bezpieczeństwa fazy 2 jest spójny z klasą agonistów receptora GLP-1, zdominowany przez zależne od dawki zdarzenia niepożądane ze strony przewodu pokarmowego, które koncentrują się w pierwszym lub drugim tygodniu każdego kroku eskalacji. Bezpieczeństwo fazy 3 (TRIUMPH-4) dostępne jest na kwiecień 2026 r. wyłącznie w postaci wstępnego komunikatu prasowego i nie zostało jeszcze poddane recenzji w pełnej rozdzielczości zbioru danych.
Wstępny odczyt TRIUMPH-4 raportuje ~28,7% redukcję w 68. tygodniu, przewyższając maksymalną wartość tyrzepatydu w SURMOUNT-1 w 72. tygodniu o około sześć punktów procentowych. Obie opublikowane sieciowe metaanalizy wskazują w tym samym kierunku.
Ramię GCGR dodaje ścieżki, których brak tyrzepatydowi: wątrobowe utlenianie kwasów tłuszczowych (~85–90% redukcji tłuszczu wątrobowego w fazie 2a w MASLD), lipolizę tkanki tłuszczowej oraz termogeniczny wydatek energetyczny.
Dwanaście+ badań fazy 3, trzy rejestracje FDA, opublikowane CVOT z udziałem 13 165 pacjentów oraz dojrzała koperta bezpieczeństwa wynikająca z informacji o produkcie. Cząsteczka referencyjna dla badań nad GLP-1/GIP w dniu dzisiejszym.
SURPASS-2 pokonało semaglutyd 1 mg w bezpośrednim porównaniu pod względem HbA1c; SURPASS-CVOT jest jedynym opublikowanym badaniem nad punktami końcowymi sercowo-naczyniowymi dla obu cząsteczek. Dowody T2D dla retatrutydu pozostają na poziomie fazy 2 (Rosenstock 2023).
Tyrzepatyd jest dwuagonistą receptorów GLP-1R i GIPR; retatrutyd dodaje receptor glukagonu (GCGR) jako trzeci punkt uchwytu 26. Ramię GCGR dorzuca wątrobowe utlenianie kwasów tłuszczowych, lipolizę tkanki tłuszczowej oraz termogeniczny wydatek energetyczny, których agonizm podwójny z założenia nie angażuje 27.
Tyrzepatyd, jednoznacznie. Dwanaście+ badań fazy 3, trzy rejestracje FDA oraz opublikowane badanie nad punktami końcowymi sercowo-naczyniowymi z udziałem 13 165 pacjentów 12. Retatrutyd ma jeden odczyt wstępny z fazy 3 (TRIUMPH-4) oraz program fazy 2 obejmujący około sześciu recenzowanych publikacji 1 5. Luka będzie się zmniejszać w 2026 r. wraz z odczytami TRIUMPH-1, TRIUMPH-2 i TRIUMPH-3.
Nie. Według stanu na kwiecień 2026 r. nie opublikowano ani publicznie nie ogłoszono żadnego bezpośredniego badania RCT retatrutyd vs tyrzepatyd. Dowody porównawcze ograniczają się do dwóch pośrednich sieciowych metaanaliz, z których obie wskazują w kierunku retatrutydu, ale nie mogą zastąpić badania head-to-head .
Retatrutyd jest naszym wyborem. Nie dlatego, że ma więcej danych z badań — nie ma. Program fazy 3 dla tyrzepatydu jest o cztery lata dojrzalszy, jego trzy rejestracje FDA obejmują cukrzycę typu 2, przewlekłe leczenie nadwagi i obturacyjny bezdech senny, a jego opublikowane badanie nad punktami końcowymi sercowo-naczyniowymi z udziałem ponad trzynastu tysięcy pacjentów to fakt, którego nie kwestionujemy 12 28. Dla protokołów badawczych potrzebujących najgłębszej, najdokładniej zweryfikowanej bazy dowodowej dostępnej dziś w klasie inkretyn tyrzepatyd jest cząsteczką referencyjną i pozostanie nią do czasu zakończenia programu TRIUMPH.
Jednak dla protokołów badawczych dążących do najwyższego pułapu terapeutycznego liczby przemawiają za retatrutydem. Jego pierwszy odczyt fazy 3 raportował około 28,7% redukcji masy ciała przy 12 mg w 68 tygodniach 5— istotną przewagę pułapu o sześć punktów procentowych nad maksymalną wartością tyrzepatydu w SURMOUNT-1 wynoszącą 22,5% w 72 tygodniach 13. Wyjaśnienie mechanistyczne nie jest spekulatywne: receptor glukagonu dodaje wątrobowe utlenianie kwasów tłuszczowych, lipolizę tkanki tłuszczowej i termogeniczny wydatek energetyczny, których agonizm podwójny z założenia nie może zaangażować 27, a 85–90% redukcja tłuszczu wątrobowego z odczytu fazy 2a w MASLD jest bezpośrednim podpisem tej ścieżki 3. Obie opublikowane sieciowe metaanalizy wskazują w kierunku retatrutydu 20 21. Baza dowodowa będzie dojrzewać; pułap, z założenia, nie obniży się.
Dla granicy badań nad terapią peptydami metabolicznymi zwycięzcą jest retatrutyd. Dla protokołów ceniących głębię na poziomie regulacyjnym ponad wszystko tyrzepatyd pozostaje standardem. To wyraźniejszy podział ról niż w większości porównań typu „X vs Y”, a uczciwość w sprawie tego podziału jest bardziej użyteczna niż wymuszenie jednego zwycięzcy.
Obecne; ~85–90% redukcji tłuszczu wątrobowego w fazie 2a w MASLD 3
Z założenia nieobecne
~144 h (~6 dni)
~120 h (~5 dni)
1 odczyt wstępny (TRIUMPH-4); TRIUMPH-1/2/3 w toku 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Brak (nie zainicjowano CVOT)
SURPASS-CVOT (n=13 165; NEJM grudzień 2025) 12
Brak (brak zatwierdzonej etykiety)
MTC, komórki C tarczycy (gryzonie; znaczenie dla ludzi nieustalone) 28
Nieopublikowane
Nieopublikowane
Raz w tygodniu, podskórnie
Raz w tygodniu, podskórnie
USA: najwcześniej koniec 2027 r. (NDA najszybciej IV kw. 2026) 22
Już zatwierdzony (USA: 2022/2023/2024; UE: 2022/2024)
Liofilizat; rekonstytucja wodą bakteriostatyczną; 2–8 °C
Liofilizat; rekonstytucja wodą bakteriostatyczną; 2–8 °C
Wyższy pułap + zakres ramienia receptora glukagonu
Niższy pułap; najlepiej scharakteryzowana koperta bezpieczeństwa
Tyrzepatyd (LY3298176) jest dwuagonistą GLP-1R/GIPR — pojedynczym 39-resztowym peptydem dostrojonym do angażowania obu receptorów inkretynowych z porównywalną mocą. Ramię GLP-1R wnosi ten sam podstawowy mechanizm, znany z pierwszej generacji analogów GLP-1: zależne od glukozy wydzielanie insuliny, supresję glukagonu z komórek alfa, podwzgórzową regulację apetytu i spowolnione opróżnianie żołądka 24.
Tym, co odróżnia tyrzepatyd od czystych agonistów GLP-1, jest dodatkowa aktywność GIPR. W warunkach przedklinicznych jednoczesne podawanie GIP z GLP-1 prowadzi do addytywnych, a w niektórych pomiarach synergistycznych redukcji masy ciała i glukozy, większych niż każdy z nich osobno 25. Ośrodkowa aktywacja GIPR wydaje się potencjalizować anorektyczne działanie GLP-1 poprzez sygnalizację POMC w podwzgórzu; obwodowa aktywacja GIPR w białej tkance tłuszczowej zwiększa pojemność buforową depozytu i redukuje konieczność ektopowego odkładania. Obserwowalną konsekwencją jest najbardziej skuteczny profil obniżania masy ciała i glukozy spośród cząsteczek zatwierdzonych przed retatrutydem: SURMOUNT-1 raportowało około 22,5% redukcji masy ciała przy dawce 15 mg po 72 tygodniach 13, a SURMOUNT-5 wykazało wyższość tyrzepatydu nad semaglutydem 2,4 mg w bezpośrednim porównaniu po 72 tygodniach (−20,2% vs −13,7%) 18.
Ramię receptora glukagonu jest mechanistycznym wyróżnikiem retatrutydu. Dane przedkliniczne i z fazy 2 sugerują, że przekłada się to na efekty obniżające lipidy, redukujące tłuszcz wątrobowy oraz zwiększające wydatek energetyczny, których tyrzepatyd, z założenia konstrukcyjnego, nie posiada. To, czy przełoży się to na przewagę w bezpośrednim porównaniu sugerowaną przez sieciowe metaanalizy, pozostanie pytaniem otwartym do czasu odczytu badania head-to-head — którego, według stanu na kwiecień 2026 r., nie ogłoszono.
Głębia dowodów dla tyrzepatydu pozostaje dziś niedościgniona — dwanaście badań fazy 3 w ramach dwóch programów chorobowych, opublikowane badanie nad punktami końcowymi sercowo-naczyniowymi z udziałem ponad trzynastu tysięcy pacjentów oraz trzy rejestracje FDA na etykiecie. Dostępny dziś odczyt retatrutydu, choć pojedynczy, przewyższa najlepszy pułap tyrzepatydu z fazy 3 przy krótszym oknie obserwacyjnym. Jest to sygnał wart poważnej uwagi w miarę dojrzewania TRIUMPH-1, TRIUMPH-2 i TRIUMPH-3 w latach 2026 i 2027.
Dojrzała koperta bezpieczeństwa wynikająca z informacji o produkcie, obejmująca Mounjaro i Zepbound. Częste AE odpowiadają klasie GLP-1 i koncentrują się w fazie eskalacji dawki; poważne ryzyka są ujęte w ostrzeżeniu w ramce oraz zestawie ostrzeżeń i środków ostrożności doprecyzowanych przez nadzór po wprowadzeniu do obrotu (analiza FAERS z 2024 r. oraz pharmacovigilance EMA).
Niniejszy artykuł jest porównaniem redakcyjnym przygotowanym dla czytelników z kontekstu badawczego. Ani retatrutyd, ani tyrzepatyd nie są oferowane ani zalecane do samodzielnego stosowania u ludzi za pośrednictwem tej witryny. Tam, gdzie tyrzepatyd jest przepisywany, dostępny jest wyłącznie pod nadzorem lekarza w jurysdykcjach, w których został zatwierdzony (Mounjaro w T2D; Zepbound w przewlekłym leczeniu nadwagi i obturacyjnym bezdechu sennym). Retatrutyd jest na kwiecień 2026 r. globalnie cząsteczką badaną i powinien być obsługiwany wyłącznie w ramach odpowiednich protokołów badawczych.
Podsumowane tu dane dotyczące bezpieczeństwa odzwierciedlają opublikowane zbiory danych z faz 2 i 3 oraz aktualne informacje o produkcie. Nowe sygnały mogą pojawić się w dowolnym momencie; data lastUpdated na tej stronie wskazuje punkt graniczny naszego przeglądu. Żaden element tej strony nie stanowi porady medycznej ani substytutu konsultacji z wykwalifikowanym lekarzem.
Tyrzepatyd jest zatwierdzony pod dwiema nazwami handlowymi: Mounjaro w cukrzycy typu 2 (FDA, maj 2022) oraz Zepbound w przewlekłym leczeniu nadwagi (listopad 2023) i w umiarkowanym do ciężkiego obturacyjnym bezdechu sennym z otyłością (grudzień 2024) 28. Retatrutyd jest cząsteczką badaną wszędzie; według stanu na kwiecień 2026 r. nie złożono NDA 22.
Retatrutyd, na podstawie dostępnych danych. TRIUMPH-4 raportowało ~−28,7% przy 12 mg w 68 tygodniach 5; najlepszy odczyt fazy 3 dla tyrzepatydu w otyłości, SURMOUNT-1 przy 15 mg w 72 tygodniach, wynosił ~−22,5% 13. Obie opublikowane sieciowe metaanalizy plasują retatrutyd wyżej pod względem redukcji masy ciała 20 21.
Na poziomie klasy obie cząsteczki mają profil zdominowany przez objawy żołądkowo-jelitowe (nudności, wymioty, biegunka), które koncentrują się w fazie eskalacji dawki. Sieciowa metaanaliza z października 2025 r. raportowała wyższe ryzyko względne zdarzeń niepożądanych dla retatrutydu (RR 4,10) niż dla tyrzepatydu (RR 2,78), spójne z wyższym obciążeniem przewodu pokarmowego przy najwyższych dawkach 20. Tyrzepatyd zawiera ostrzeżenie w ramce dotyczące MTC oraz scharakteryzowany profil zapalenia trzustki, pęcherzyka żółciowego i nadwrażliwości 28 29; analogiczna długoterminowa koperta bezpieczeństwa retatrutydu nie została jeszcze ustalona.
Opublikowane badania fazy 2 i fazy 3 dla obu cząsteczek włączają je w monoterapii (z lub bez tła leczenia T2D, takiego jak metformina lub insulina). Brak opublikowanych dowodów dotyczących łączenia którejkolwiek z innymi peptydami badawczymi. Każdy protokół kombinowany jest stricte badawczy i wykracza poza bazę dowodową podsumowaną w niniejszym artykule.
Okres półtrwania retatrutydu wynoszący ~144 godziny i tyrzepatydu wynoszący ~120 godzin wspierają jednorazową cotygodniową dawkę podskórną, czyli schemat stosowany w każdym badaniu rejestracyjnym. Nieco dłuższy okres półtrwania retatrutydu zapewnia skromny bufor wobec zmienności wynikającej z pominiętych dawek, lecz nie zmienia fundamentalnej kadencji raz w tygodniu.
Tak. Zarówno retatrutyd, jak i tyrzepatyd są wystawione do zastosowań badawczych w obu kanałach — UE i USA. Dostępność, wielkości fiolek i ceny specyficzne dla kanału są pokazane na stronach szczegółowych każdego produktu.
Według wskazań Lilly w 2026 r. spodziewane są odczyty TRIUMPH-1 (otyłość bez T2D), TRIUMPH-2 (otyłość z T2D) i TRIUMPH-3 (otyłość z udokumentowaną chorobą sercowo-naczyniową) 4. Każdy z nich istotnie poszerzy bazę dowodową retatrutydu; łącznie zdecydują, czy pułap z TRIUMPH-4 generalizuje się na różne populacje i czy złożenie NDA przyspieszy w stosunku do obecnego najwcześniejszego okna IV kw. 2026.
Retatrutyd wygrywa w wymiarach, które najbardziej liczą się dla badań na granicy możliwości: wyższy obserwowany pułap w TRIUMPH-4, szerokość mechanizmu trójagonisty oraz spójny kierunek w obu opublikowanych sieciowych metaanalizach. Tyrzepatyd pozostaje cząsteczką referencyjną dla protokołów wymagających najgłębszej dostępnej dziś opublikowanej bazy dowodowej.