

O agonista triplo que estabeleceu um novo tecto contra o agonista duplo que construiu a categoria. Uma comparação para protocolos de investigação que querem perceber qual é a molécula da fronteira, qual é o padrão e por que essa distinção importa.

Tirzepatide (Mounjaro/Zepbound da Eli Lilly) é um agonista duplo dos receptores GLP-1/GIP com quatro anos de dados de Fase 3, três aprovações da FDA e um ensaio publicado de desfechos cardiovasculares. Retatrutide, a molécula seguinte da Lilly, é um agonista triplo que acrescenta o receptor do glucagon ao mesmo esqueleto duplo e, na sua primeira leitura de Fase 3, produziu a redução de peso mais profunda alguma vez registada num ensaio de obesidade com fins de registo: cerca de 28,7% às 68 semanas 5 contra o pico de tirzepatide no SURMOUNT-1 de aproximadamente 22,5% às 72 semanas 13.
As bases de evidência não são simétricas. Tirzepatide tem o caso maduro e revisto por pares. Retatrutide tem o tecto observado mais elevado, um perfil-alvo mecanicisticamente mais alargado e duas meta-análises em rede que apontam na sua direcção 20 21. Para protocolos de investigação que privilegiam o tecto terapêutico máximo e a amplitude do mecanismo, a nossa escolha editorial é retatrutide. Para protocolos que valorizam a profundidade da evidência de grau regulamentar e uma rotulagem de segurança consolidada, tirzepatide continua a ser a molécula de referência.
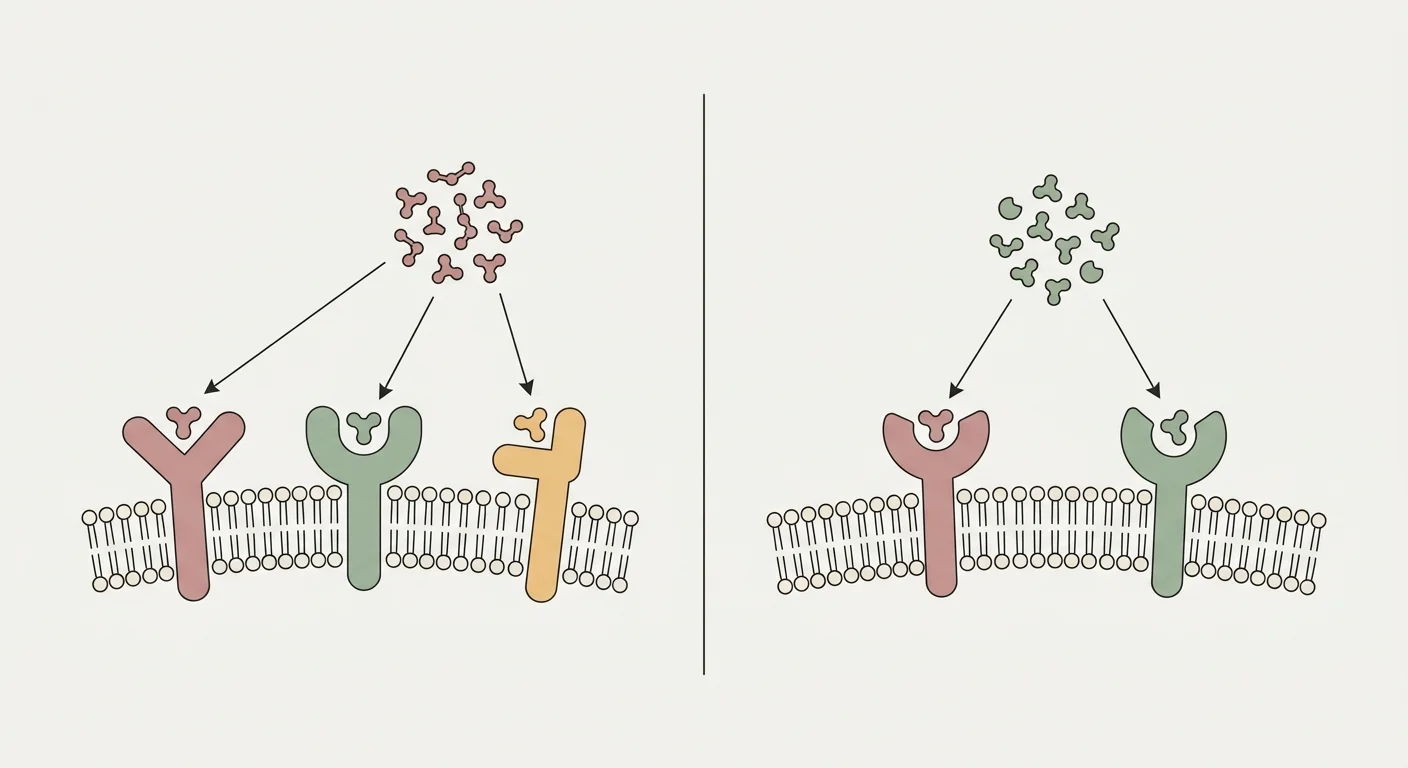
Retatrutide (LY3437943) é um único peptídeo concebido para activar simultaneamente três receptores da família das incretinas: o receptor do peptídeo-1 semelhante ao glucagon (GLP-1R), o receptor do peptídeo insulinotrópico dependente da glicose (GIPR) e o receptor do glucagon (GCGR) 26. O braço GLP-1R conduz a supressão central do apetite, o atraso do esvaziamento gástrico e a secreção de insulina dependente da glicose já familiares de semaglutide e tirzepatide 24. O braço GIPR acrescenta actividade insulinotrópica sinérgica e, no tecido adiposo, reforça a capacidade de tamponamento lipídico saudável, reduzindo a deposição ectópica de gordura no fígado e nos músculos 25.
O braço distintivo é o GCGR. O glucagon é normalmente apresentado como a hormona contra-reguladora que eleva a glicemia; no contexto de um agonista triplo equilibrado, o seu efeito clássico sobre a produção hepática de glicose é compensado pela acção insulinotrópica simultânea de GLP-1R/GIPR, retendo-se contudo os efeitos metabólicos que os concebedores de peptídeos efectivamente procuram no GCGR: aumento do gasto energético via termogénese no tecido adiposo castanho e oxidação no músculo esquelético, lipólise adiposa com libertação de ácidos gordos livres para beta-oxidação, e oxidação hepática de ácidos gordos que depura triglicéridos do fígado 27. Em dados de Fase 2a em MASLD, retatrutide produziu cerca de 85–90% de redução de gordura hepática na dose mais alta; perto de 90% dos participantes a 12 mg atingiram gordura hepática inferior a 5% às 48 semanas, magnitude que o agonismo duplo não demonstrou 3.
Não existe, à data de Abril de 2026, nenhum ensaio aleatorizado controlado directo de retatrutide contra tirzepatide publicado ou anunciado. Um ensaio cabeça-a-cabeça com fins de registo (NCT06662383) consta no rastreador de pipeline da Lilly, mas não foi reportada qualquer leitura. Toda a afirmação comparativa neste artigo carrega, por isso, uma ressalva: ou se trata de uma comparação indirecta entre ensaios com populações, esquemas de doses e desfechos diferentes, ou de uma extrapolação mecanicista a partir de dados pré-clínicos e de Fase 2. Não é razão para ignorar o sinal — é razão para o qualificar.
Duas meta-análises em rede tentaram colocar as moléculas na mesma escala. A análise de Outubro de 2025, publicada no Journal of the Endocrine Society (resumo SUN-659, com artigo completo revisto por pares em PMC12544991), reportou retatrutide com uma redução absoluta média de −16,34 kg e −23,77% de peso corporal contra −11,82 kg e −16,79% para tirzepatide, uma vantagem indirecta a favor de retatrutide 20. A mesma análise sinalizou um risco relativo de eventos adversos mais elevado para retatrutide (RR 4,10 vs 2,78), consistente com maior carga gastrointestinal nas doses mais altas. Uma meta-análise em rede mais ampla, com sete agentes, publicada em Metabolism (2024), classificou as moléculas para perda de peso como retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, com ordenações consistentes em circunferência da cintura, HbA1c e glicemia plasmática em jejum 21.
Ambas as meta-análises em rede favorecem retatrutide numérica e direccionalmente, mas a ausência de evidência directa de ensaio aleatorizado obriga a que qualquer afirmação comparativa carregue uma ressalva. Para fins de investigação, é razão para aprofundar o estudo, não para descartar o sinal.
O perfil de segurança de Fase 2 é consistente com a classe dos agonistas do receptor GLP-1, dominado por eventos adversos gastrointestinais dose-dependentes que se concentram na primeira ou segunda semana de cada fase de escalonamento. A segurança em Fase 3 (TRIUMPH-4) está disponível, à data de Abril de 2026, apenas como leitura preliminar em comunicado de imprensa, ainda não revista por pares com a granularidade do conjunto de dados completo.
O TRIUMPH-4, em leitura preliminar, reporta ~28,7% de redução às 68 semanas, ultrapassando o pico do SURMOUNT-1 de tirzepatide às 72 semanas em cerca de seis pontos percentuais. Ambas as meta-análises em rede publicadas apontam na mesma direcção.
O braço GCGR acrescenta vias que tirzepatide não tem: oxidação hepática de ácidos gordos (~85–90% de redução de gordura hepática em Fase 2a MASLD), lipólise adiposa e gasto energético termogénico.
Mais de doze ensaios de Fase 3, três aprovações da FDA, um CVOT publicado em 13.165 doentes e um envelope de segurança maduro na informação prescritora. A molécula de referência para investigação GLP-1/GIP nos dias de hoje.
O SURPASS-2 venceu semaglutide 1 mg em comparação directa em HbA1c; o SURPASS-CVOT é o único ensaio de desfechos cardiovasculares publicado para qualquer das moléculas. A evidência de retatrutide em T2D permanece em Fase 2 (Rosenstock 2023).
Tirzepatide, sem ambiguidades. Mais de doze ensaios de Fase 3, três aprovações da FDA e um ensaio publicado de desfechos cardiovasculares em 13.165 doentes 12. Retatrutide tem uma leitura preliminar de Fase 3 (TRIUMPH-4) e um programa de Fase 2 com aproximadamente seis publicações revistas por pares 1 5. A diferença irá estreitar-se ao longo de 2026, à medida que TRIUMPH-1, TRIUMPH-2 e TRIUMPH-3 reportarem resultados.
Não. Nenhum ensaio aleatorizado directo de retatrutide vs tirzepatide foi publicado ou divulgado publicamente, à data de Abril de 2026. A evidência comparativa limita-se a duas meta-análises em rede indirectas, ambas a apontar na direcção de retatrutide, mas que não substituem um ensaio cabeça-a-cabeça 20 .
Retatrutide é a nossa escolha. Não porque tenha mais dados de ensaio — não tem. O programa de Fase 3 de tirzepatide é quatro anos mais profundo, as suas três aprovações da FDA cobrem diabetes tipo 2, gestão crónica de peso e apneia obstrutiva do sono, e o seu ensaio publicado de desfechos cardiovasculares em mais de treze mil doentes é um facto que não disputamos 12 28. Para protocolos de investigação que precisam da base de evidência mais profunda e mais escrutinada disponível na classe das incretinas hoje, tirzepatide é a molécula de referência e assim continuará até que o programa TRIUMPH esteja concluído.
Mas para protocolos de investigação que perseguem o tecto terapêutico mais elevado, os números favorecem retatrutide. A sua primeira leitura de Fase 3 reportou cerca de 28,7% de redução de peso a 12 mg ao longo de 68 semanas 5— uma vantagem significativa de cerca de seis pontos percentuais sobre o pico do SURMOUNT-1 de tirzepatide, de 22,5% ao longo de 72 semanas 13. A explicação mecanicista não é especulativa: o receptor do glucagon acrescenta oxidação hepática de ácidos gordos, lipólise adiposa e gasto energético termogénico que o agonismo duplo não pode, por desenho, mobilizar 27, e a redução de 85–90% de gordura hepática observada na leitura de Fase 2a em MASLD é uma assinatura directa dessa via 3. Ambas as meta-análises em rede publicadas apontam na direcção de retatrutide 20 21. A base de evidência irá amadurecer; o tecto, por desenho, não irá baixar.
Para a fronteira da investigação em terapêutica peptídica metabólica, retatrutide é o vencedor. Para protocolos que valorizam acima de tudo a profundidade de grau regulamentar, tirzepatide mantém-se como o padrão. É uma divisão de papéis mais clara do que a maioria das comparações «X vs Y» consegue oferecer, e a honestidade quanto a essa divisão é mais útil do que um vencedor único forçado.
Presente; ~85–90% de redução de gordura hepática em Fase 2a MASLD 3
Ausente por desenho
~144 h (~6 dias)
~120 h (~5 dias)
1 leitura preliminar (TRIUMPH-4); TRIUMPH-1/2/3 pendentes 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Nenhum (sem CVOT iniciado)
SURPASS-CVOT (n=13.165; NEJM Dez. 2025) 12
Nenhum (sem rótulo aprovado)
Células C tiroideias (MTC) (roedor; relevância humana não estabelecida) 28
Nenhum publicado
Nenhum publicado
Uma vez por semana, subcutânea
Uma vez por semana, subcutânea
EUA: final de 2027 no mais cedo (NDA no 4.º trimestre de 2026 quando muito) 22
Já aprovado (EUA: 2022/2023/2024; UE: 2022/2024)
Liofilizado; reconstituição com água BAC; 2–8 °C
Liofilizado; reconstituição com água BAC; 2–8 °C
Tecto mais elevado + amplitude do receptor do glucagon
Tecto mais baixo; envelope de segurança mais bem caracterizado
Tirzepatide (LY3298176) é um agonista duplo de GLP-1R / GIPR — um único peptídeo de 39 resíduos afinado para se ligar a ambos os receptores incretínicos com potência comparável. O braço GLP-1R contribui com o mesmo mecanismo central já familiar da primeira geração de análogos de GLP-1: secreção de insulina dependente da glicose, supressão de glucagon nas células alfa, regulação hipotalâmica do apetite e desaceleração do esvaziamento gástrico 24.
O que distingue tirzepatide dos agonistas puros de GLP-1 é a actividade GIPR adicional. No plano pré-clínico, a co-administração de GIP com GLP-1 produz reduções aditivas e, em alguns indicadores, sinérgicas no peso corporal e na glicose, superiores a qualquer um isoladamente 25. A activação central de GIPR parece potenciar a anorexia induzida por GLP-1 através da sinalização POMC hipotalâmica; a activação periférica de GIPR no tecido adiposo branco aumenta a capacidade de tamponamento do depósito e reduz a necessidade de deposição ectópica. A consequência observável é o perfil mais potente de redução de peso e de glicose entre todas as moléculas aprovadas antes de retatrutide: o SURMOUNT-1 reportou cerca de 22,5% de redução de peso na dose de 15 mg ao longo de 72 semanas 13, e o SURMOUNT-5 mostrou tirzepatide superior a semaglutide 2,4 mg em comparação directa às 72 semanas (−20,2% vs −13,7%) 18.
O braço do receptor do glucagon é o factor de diferenciação mecanicista de retatrutide. Os dados pré-clínicos e de Fase 2 sugerem que isso se traduz em efeitos hipolipidemiantes, redutores da gordura hepática e aumentadores do gasto energético que tirzepatide, por desenho, não possui. Saber se isso se traduz na vantagem de comparação directa sugerida pelas meta-análises em rede permanecerá em aberto até que um ensaio aleatorizado cabeça-a-cabeça reporte resultados — e, à data de Abril de 2026, nenhum foi anunciado.
A profundidade de evidência de tirzepatide é hoje incomparável — doze ensaios de Fase 3 entre dois programas de doença, um ensaio publicado de desfechos cardiovasculares em mais de treze mil doentes e três aprovações da FDA. A leitura disponível de retatrutide, ainda que singular, supera o melhor tecto de Fase 3 de tirzepatide numa janela de observação mais curta. É um sinal merecedor de séria atenção, à medida que TRIUMPH-1, TRIUMPH-2 e TRIUMPH-3 amadurecem ao longo de 2026 e 2027.
Envelope de segurança maduro na informação prescritora de Mounjaro e Zepbound. Os efeitos adversos comuns reflectem a classe GLP-1 e concentram-se no escalonamento de dose; os riscos sérios estão capturados num aviso emoldurado e num conjunto de advertências e precauções refinado pela vigilância pós-comercialização (análise FAERS de 2024 e farmacovigilância da EMA).
Este artigo é uma comparação editorial preparada para leitores em contexto de investigação. Nem retatrutide nem tirzepatide são oferecidos ou recomendados para auto-administração humana através deste sítio. Quando tirzepatide é prescrito, está disponível apenas sob supervisão médica nas jurisdições onde foi aprovado (Mounjaro para T2D; Zepbound para gestão crónica de peso e apneia obstrutiva do sono). Retatrutide é, à data de Abril de 2026, investigacional a nível global e deve ser manuseado apenas no âmbito de protocolos de investigação adequados.
Os dados de segurança aqui resumidos reflectem conjuntos de dados publicados de Fase 2 e Fase 3 e a informação prescritora actual. Podem surgir novos sinais a qualquer momento; a data de lastUpdated nesta página indica o ponto de corte da nossa revisão. Nada nesta página constitui aconselhamento médico ou substitui a consulta com um clínico qualificado.
Tirzepatide está aprovada sob duas marcas: Mounjaro para diabetes tipo 2 (FDA, Maio de 2022) e Zepbound para gestão crónica de peso (Novembro de 2023) e para apneia obstrutiva do sono moderada-a-grave em obesidade (Dezembro de 2024) 28. Retatrutide é investigacional em todo o lado; nenhuma NDA foi submetida à data de Abril de 2026 22.
Retatrutide, com base nos dados disponíveis. O TRIUMPH-4 reportou ~−28,7% a 12 mg ao longo de 68 semanas 5; a melhor leitura de obesidade em Fase 3 de tirzepatide, o SURMOUNT-1 a 15 mg ao longo de 72 semanas, foi de ~−22,5% 13. Ambas as meta-análises em rede publicadas classificam retatrutide acima na redução de peso corporal 20 21.
Ao nível da classe, ambos têm um perfil de predomínio gastrointestinal (náuseas, vómitos, diarreia) que se concentra no escalonamento de dose. A meta-análise em rede de Outubro de 2025 reportou um risco relativo de eventos adversos mais elevado para retatrutide (RR 4,10) do que para tirzepatide (RR 2,78), consistente com maior carga gastrointestinal nas doses mais altas 20. Tirzepatide tem aviso emoldurado MTC e um perfil caracterizado de pancreatite / vesícula biliar / hipersensibilidade 28 29; o envelope análogo de segurança a longo prazo de retatrutide ainda não foi estabelecido.
Os ensaios de Fase 2 e Fase 3 publicados para ambas as moléculas recrutam em monoterapia (com ou sem terapia de fundo para T2D, como metformina ou insulina). Não há evidência publicada sobre combinação de qualquer uma com outros peptídeos de investigação. Qualquer protocolo de combinação é estritamente investigacional e fica fora da base de evidência resumida neste artigo.
A semivida de aproximadamente 144 horas de retatrutide e a semivida de aproximadamente 120 horas de tirzepatide suportam, ambas, uma única dose subcutânea semanal, o esquema usado em todos os ensaios com fins de registo. A semivida ligeiramente mais longa de retatrutide oferece uma margem modesta contra a variabilidade por doses falhadas, mas não altera a cadência fundamental semanal.
Sim. Tanto retatrutide como tirzepatide estão listados para uso de investigação nos canais UE e EUA. A disponibilidade, os tamanhos de frasco e o preço específico de cada canal são apresentados na página de detalhe de cada produto.
As leituras de TRIUMPH-1 (obesidade sem T2D), TRIUMPH-2 (obesidade com T2D) e TRIUMPH-3 (obesidade com doença cardiovascular estabelecida) estão previstas ao longo de 2026, segundo orientações da Lilly 4. Cada uma irá expandir materialmente a base de evidência de retatrutide; em conjunto, irão determinar se o tecto do TRIUMPH-4 se generaliza entre populações e se a submissão da NDA se antecipa relativamente à actual janela mais cedo de 4.º trimestre de 2026.
Retatrutide vence nas dimensões que mais importam para a investigação de fronteira: tecto observado mais elevado no TRIUMPH-4, amplitude do mecanismo de agonismo triplo e direcção consistente em ambas as meta-análises em rede publicadas. Tirzepatide mantém-se como a molécula de referência para protocolos que precisam da base de evidência publicada mais profunda hoje.