

Тройният агонист, който постави нов таван, срещу двойния агонист, изградил категорията. Сравнение за изследователски протоколи, които искат да разберат коя молекула е границата, коя е стандартът и защо това разграничение има значение.

Тирзепатид (Mounjaro/Zepbound на Eli Lilly) е двоен GLP-1/GIP рецепторен агонист с четири години данни от Фаза 3, три одобрения от FDA и публикувано проучване за сърдечно-съдови резултати. Ретатрутид, последващата молекула на Lilly, е троен агонист, който добавя глюкагоновия рецептор към същия двоен скелет и в първия си резултат от Фаза 3 произведе най-дълбокото намаляване на теглото, докладвано някога в регистрационно проучване за затлъстяване: около 28,7% на 68 седмици 5 срещу пика на тирзепатид в SURMOUNT-1 от приблизително 22,5% на 72 седмици 13.
Доказателствените бази не са симетрични. Тирзепатид има зрелия, рецензиран от експерти случай. Ретатрутид има по-високия наблюдаван таван, механистично по-широк профил на мишените и две мрежови мета-анализи, които сочат в негова посока 20 21. За изследователски протоколи, приоритизиращи максимален терапевтичен таван и широта на механизма, нашият редакторски избор е ретатрутид. За протоколи, които ценят дълбочина на доказателствата от регулаторен клас и установен профил на безопасност, тирзепатид остава референтната молекула.
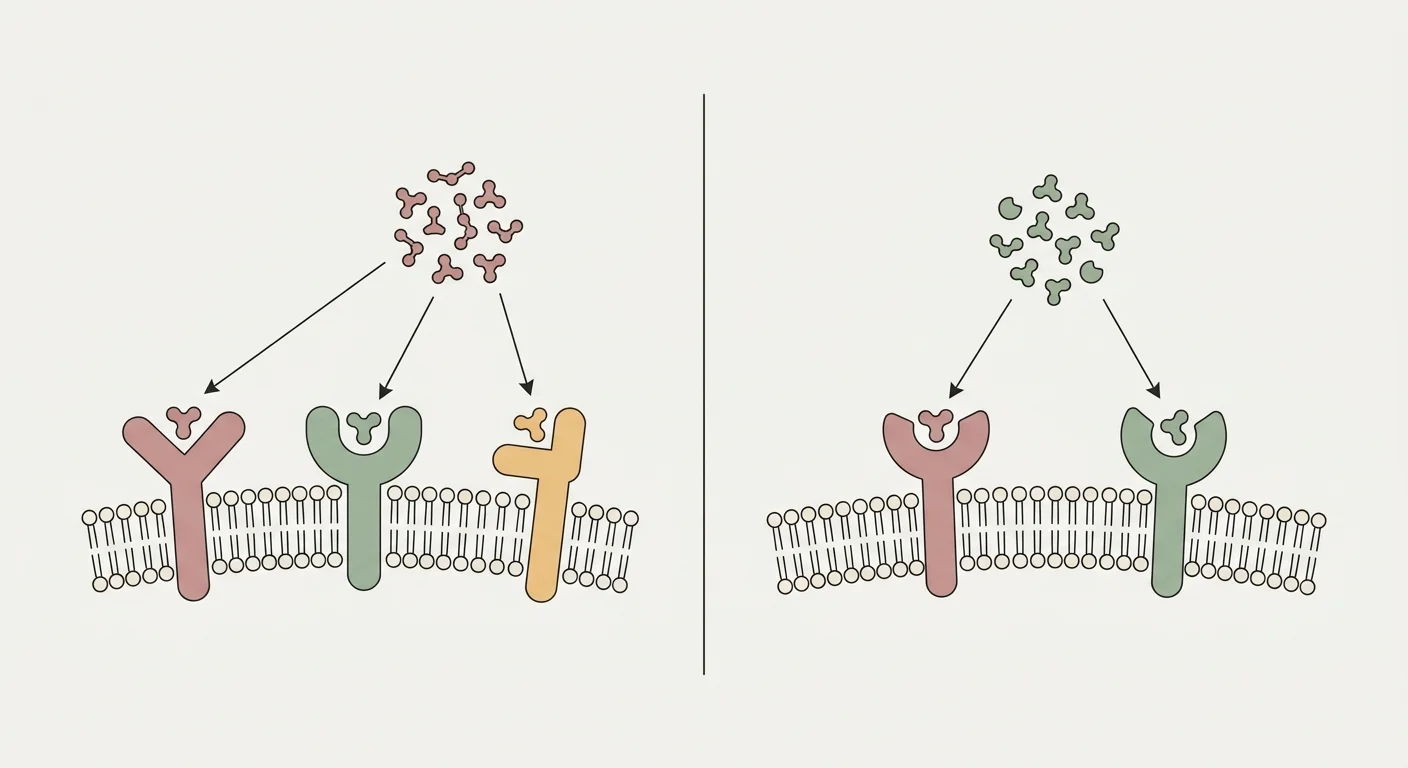
Ретатрутид (LY3437943) е единичен пептид, проектиран да агонизира едновременно три рецептора от инкретиновото семейство: рецептора на глюкагон-подобен пептид-1 (GLP-1R), рецептора на глюкозо-зависим инсулинотропен полипептид (GIPR) и глюкагоновия рецептор (GCGR) 26. Рамото GLP-1R задвижва централното потискане на апетита, забавеното изпразване на стомаха и глюкозо-зависимата инсулинова секреция, познати от семаглутид и тирзепатид 24. Рамото GIPR добавя синергична инсулинотропна активност и в мастната тъкан подобрява здравословното липидно буфериране, намалявайки ектопичното натрупване на мазнини в черния дроб и мускулите 25.
Отличителното рамо е GCGR. Глюкагонът обикновено се представя като контрарегулаторния хормон, който повишава кръвната захар; в контекста на балансиран троен агонист класическият му ефект върху чернодробната глюкозна продукция се компенсира от едновременното инсулинотропно действие на GLP-1R/GIPR, докато метаболитните ефекти, които дизайнерите на пептиди всъщност искат от GCGR, са запазени: повишен енергиен разход чрез термогенеза в кафявата мастна тъкан и окисление в скелетната мускулатура, мастна липолиза с освобождаване на свободни мастни киселини за бета-окисление и чернодробно окисление на мастни киселини, което изчиства триглицеридите от черния дроб 27. В данните от Фаза 2a при MASLD, ретатрутид произведе приблизително 85–90% намаляване на чернодробната мазнина при най-високата доза; около 90% от участниците на 12 mg достигнаха чернодробна мазнина под 5% на 48 седмици — величина, която двойното агонизиране не е демонстрирало 3.
Към април 2026 г. не е публикувано или обявено директно рандомизирано контролирано проучване ретатрутид срещу тирзепатид. Регистрационно проучване глава срещу глава (NCT06662383) е видимо в проследяващия инструмент за линията на Lilly, но не са докладвани резултати. Следователно всяко сравнително твърдение в тази статия носи уговорка: то е или непряко сравнение между проучвания с различни популации, дозиращи схеми и крайни точки, или е механистична екстраполация от предклинични данни и данни от Фаза 2. Това не е причина да се игнорира сигналът — това е причина да се квалифицира.
Два мрежови мета-анализа са се опитали да поставят молекулите в една и съща скала. Анализът от октомври 2025 г., публикуван в Journal of the Endocrine Society (резюме SUN-659, с пълна рецензирана статия в PMC12544991), докладва ретатрутид със средно абсолютно намаляване от −16,34 kg и −23,77% телесно тегло срещу −11,82 kg и −16,79% за тирзепатид — непряко предимство в полза на ретатрутид 20. Същият анализ отбеляза по-висок относителен риск от нежелани събития за ретатрутид (RR 4,10 срещу 2,78), съответстващ на по-голяма стомашно-чревна тежест при най-високите дози. По-широк мрежов мета-анализ на седем агента, публикуван в Metabolism (2024), класира молекулите за загуба на тегло като ретатрутид 12 mg > ретатрутид 8 mg > тирзепатид 15 mg, с последователни класирания по обиколка на талията, HbA1c и кръвна глюкоза на гладно 21.
Двата мрежови мета-анализа предпочитат ретатрутид числово и посоково, но липсата на директни RCT доказателства означава, че всяко сравнително твърдение трябва да носи уговорка. За изследователски цели това е причина за по-нататъшно проучване, а не причина да се отхвърля сигналът.
Профилът на безопасност от Фаза 2 е съвместим с класа на GLP-1 рецепторните агонисти, доминиран от дозо-зависими стомашно-чревни нежелани събития, които се концентрират в първата една до две седмици на всяка ескалационна стъпка. Безопасността от Фаза 3 (TRIUMPH-4) е налична само като предварителен резултат от прессъобщение към април 2026 г. и все още не е рецензирана при пълна резолюция на набора от данни.
Предварителният резултат на TRIUMPH-4 докладва ~28,7% намаляване на 68 седмици, надхвърляйки пика на тирзепатид в SURMOUNT-1 на 72 седмици с приблизително шест процентни пункта. И двата публикувани мрежови мета-анализа сочат в същата посока.
Рамото GCGR добавя пътища, които тирзепатид няма: чернодробно окисление на мастни киселини (~85–90% намаляване на чернодробната мазнина във Фаза 2a при MASLD), мастна липолиза и термогенен енергиен разход.
Дванадесет+ проучвания Фаза 3, три одобрения от FDA, публикувано CVOT при 13 165 пациенти и зрял профил на безопасност в информацията за предписване. Референтната молекула за GLP-1/GIP изследвания днес.
SURPASS-2 победи семаглутид 1 mg в директно сравнение по HbA1c; SURPASS-CVOT е единственото публикувано проучване за сърдечно-съдови резултати от която и да е от двете молекули. Доказателствата за ретатрутид при T2D остават във Фаза 2 (Rosenstock 2023).
Тирзепатид, недвусмислено. Дванадесет+ проучвания Фаза 3, три одобрения от FDA и публикувано проучване за сърдечно-съдови резултати при 13 165 пациенти 12. Ретатрутид има един предварителен резултат от Фаза 3 (TRIUMPH-4) и програма Фаза 2 от приблизително шест рецензирани публикации 1 5. Разликата ще се стесни през 2026 г., докато TRIUMPH-1, TRIUMPH-2 и TRIUMPH-3 отчитат резултати.
Не. Към април 2026 г. не е публикувано или публично докладвано директно RCT ретатрутид срещу тирзепатид. Сравнителните доказателства са ограничени до два непреки мрежови мета-анализа, и двата от които сочат в посока на ретатрутид, но не могат да заменят проучване глава срещу глава 20 .
Ретатрутид е нашият избор. Не защото има повече данни от проучвания — няма. Програмата на тирзепатид от Фаза 3 е с четири години по-дълбока, трите му одобрения от FDA обхващат диабет тип 2, хронично управление на теглото и обструктивна сънна апнея, а публикуваното му проучване за сърдечно-съдови резултати при повече от тринадесет хиляди пациенти е факт, който не оспорваме 12 28. За изследователски протоколи, които се нуждаят от най-дълбоката, най-внимателно изследваната доказателствена база, налична днес в инкретиновия клас, тирзепатид е референтната молекула и ще остане такава, докато програмата TRIUMPH не приключи.
Но за изследователски протоколи, преследващи най-високия терапевтичен таван, числата предпочитат ретатрутид. Първият му резултат от Фаза 3 докладва приблизително 28,7% намаляване на теглото при 12 mg за 68 седмици 5— значимо предимство от шест процентни пункта в тавана спрямо пика на тирзепатид в SURMOUNT-1 от 22,5% за 72 седмици 13. Механистичното обяснение не е спекулативно: глюкагоновият рецептор добавя чернодробно окисление на мастни киселини, мастна липолиза и термогенен енергиен разход, които двойното агонизиране не може да ангажира по дизайн 27, а резултатът от Фаза 2a при MASLD с 85–90% намаляване на чернодробната мазнина е директен подпис на този път 3. И двата публикувани мрежови мета-анализа сочат в посока на ретатрутид 20 21. Доказателствената база ще узрее; таванът, по дизайн, няма да се движи надолу.
За изследователската граница на метаболитната пептидна терапия ретатрутид е победителят. За протоколи, които ценят дълбочина от регулаторен клас над всичко, тирзепатид остава стандартът. Това е по-ясно разделение на ролите, отколкото повечето сравнения „X срещу Y” могат да предложат, и честността по отношение на разделението е по-полезна от насилствено избиране на единствен победител.
Налице; ~85–90% намаляване на чернодробната мазнина във Фаза 2a при MASLD 3
Отсъства по дизайн
~144 ч (~6 дни)
~120 ч (~5 дни)
1 предварителен резултат (TRIUMPH-4); TRIUMPH-1/2/3 предстоят 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Няма (не е инициирано CVOT)
SURPASS-CVOT (n=13 165; NEJM, декември 2025) 12
Няма (няма одобрен етикет)
MTC щитовидни C-клетки (гризачи, човешка значимост неустановена) 28
Няма публикувано
Няма публикувано
Веднъж седмично, подкожно
Веднъж седмично, подкожно
САЩ: най-рано края на 2027 г. (NDA не по-рано от Q4 2026) 22
Вече одобрен (САЩ: 2022/2023/2024; ЕС: 2022/2024)
Лиофилизиран; реконституиране с BAC вода; 2–8 °C
Лиофилизиран; реконституиране с BAC вода; 2–8 °C
По-висок таван + широта на глюкагоновия рецептор
По-нисък таван; най-добре охарактеризиран профил на безопасност
Тирзепатид (LY3298176) е двоен GLP-1R / GIPR агонист — единичен 39-аминокиселинен пептид, настроен да ангажира двата инкретинови рецептора със сравнима потентност. Рамото GLP-1R допринася за същия основен механизъм, познат от първото поколение GLP-1 аналози: глюкозо-зависима инсулинова секреция, потискане на алфа-клетъчния глюкагон, хипоталамична регулация на апетита и забавено изпразване на стомаха 24.
Това, което отличава тирзепатид от чистите GLP-1 агонисти, е добавената GIPR активност. Предклинично, едновременното прилагане на GIP с GLP-1 произвежда адитивни и в някои показатели синергични намаления на телесното тегло и глюкозата, повече отколкото всеки от тях самостоятелно 25. Централното GIPR активиране изглежда потенцира индуцираната от GLP-1 анорексия чрез хипоталамично POMC сигнализиране; периферното GIPR активиране в бялата мастна тъкан подобрява буферния капацитет на депото и намалява нуждата от ектопично отлагане. Наблюдаемата последица е най-потентният профил на намаляване на теглото и глюкозата от която и да е молекула, одобрена преди ретатрутид: SURMOUNT-1 докладва приблизително 22,5% намаляване на теглото при доза 15 mg за 72 седмици 13, а SURMOUNT-5 показа тирзепатид по-висок от семаглутид 2,4 mg в директно сравнение на 72 седмици (−20,2% срещу −13,7%) 18.
Глюкагон-рецепторното рамо е механистичният диференциатор на ретатрутид. Предклиничните данни и тези от Фаза 2 предполагат, че това се превръща в липидопонижаващи, чернодробно-мазнинно намаляващи и енергийно-разходни ефекти, които тирзепатид по дизайн няма. Дали това ще се превърне в директно сравнително предимство, подразбиращо се от мрежовите мета-анализи, ще остане отворено, докато не се отчете директно RCT — което, към април 2026 г., все още не е обявено.
Дълбочината на доказателствата за тирзепатид е несравнима днес — дванадесет проучвания Фаза 3 в две болестни програми, публикувано проучване за сърдечно-съдови резултати при повече от тринадесет хиляди пациенти и три одобрения от FDA на етикета. Наличният резултат за ретатрутид, макар и единичен, превъзхожда най-добрия таван от Фаза 3 на тирзепатид при по-кратък прозорец на наблюдение. Това е сигнал заслужаващ сериозно внимание, докато TRIUMPH-1, TRIUMPH-2 и TRIUMPH-3 узряват през 2026 и 2027 г.
Зрял профил на безопасност в информацията за предписване на Mounjaro и Zepbound. Често срещаните нежелани събития отразяват GLP-1 класа и се концентрират при ескалация на дозата; сериозните рискове са обхванати в предупреждение в рамка и набор от предупреждения и предпазни мерки, прецизирани чрез постмаркетингово наблюдение (анализ на FAERS 2024 и фармакобдителност на EMA).
Тази статия е редакторско сравнение, подготвено за читатели в изследователски контекст. Нито ретатрутид, нито тирзепатид се предлагат или препоръчват за самостоятелно прилагане при хора чрез този сайт. Когато тирзепатид е предписан, той е достъпен само под лекарско наблюдение в юрисдикции, където е одобрен (Mounjaro за T2D; Zepbound за хронично управление на теглото и обструктивна сънна апнея). Ретатрутид е изследователски в световен мащаб към април 2026 г. и трябва да се борави с него само в рамките на подходящи изследователски протоколи.
Обобщените тук данни за безопасност отразяват публикувани набори от данни от Фаза 2 и Фаза 3 и текущата информация за предписване. Нови сигнали могат да се появят по всяко време; датата lastUpdated на тази страница показва крайния срок за нашия преглед. Нищо на тази страница не представлява медицински съвет или заместител на консултация с квалифициран клиницист.
Тирзепатид е одобрен под две търговски марки: Mounjaro за диабет тип 2 (FDA, май 2022) и Zepbound за хронично управление на теглото (ноември 2023) и умерена до тежка обструктивна сънна апнея със затлъстяване (декември 2024) 28. Ретатрутид е изследователски навсякъде; към април 2026 г. не е подадена NDA 22.
Ретатрутид, въз основа на наличните данни. TRIUMPH-4 докладва ~−28,7% при 12 mg за 68 седмици 5; най-добрият резултат на тирзепатид от Фаза 3 при затлъстяване, SURMOUNT-1 при 15 mg за 72 седмици, беше ~−22,5% 13. И двата публикувани мрежови мета-анализа класират ретатрутид по-високо при намаляване на телесното тегло 20 21.
На ниво клас и двете имат GI-доминиран профил (гадене, повръщане, диария), който се концентрира при ескалация на дозата. Мрежовият мета-анализ от октомври 2025 г. докладва по-висок относителен риск от нежелани събития за ретатрутид (RR 4,10) от този за тирзепатид (RR 2,78), съвместим с по-голяма GI тежест при най-високите дози 20. Тирзепатид носи предупреждение в рамка за MTC и охарактеризиран профил на панкреатит / жлъчен мехур / свръхчувствителност 28 29; аналогичният дългосрочен профил на безопасност на ретатрутид не е установен.
Публикуваните проучвания Фаза 2 и Фаза 3 за двете молекули включват като монотерапия (със или без фонова терапия за T2D, като метформин или инсулин). Няма публикувани доказателства за комбиниране на двете с други изследователски пептиди. Всеки комбиниран протокол е строго изследователски и извън доказателствената база, обобщена в тази статия.
Полуживотът на ретатрутид от ~144 часа и този на тирзепатид от ~120 часа подкрепят една седмична подкожна доза — схемата, използвана във всяко регистрационно проучване. Малко по-дългият полуживот на ретатрутид осигурява скромен буфер срещу променливост при пропусната доза, но не променя фундаменталния веднъж-седмично ритъм.
Да. Както ретатрутид, така и тирзепатид са изброени за изследователска употреба в EU и US каналите. Наличността, размерите на флакони и специфичните за канала цени са показани на страницата с детайли за всеки продукт.
Резултатите от TRIUMPH-1 (затлъстяване без T2D), TRIUMPH-2 (затлъстяване с T2D) и TRIUMPH-3 (затлъстяване с установено сърдечно-съдово заболяване) се очакват през 2026 г. според насоките на Lilly 4. Всеки от тях ще разшири материално доказателствената база за ретатрутид; колективно те ще определят дали таванът на TRIUMPH-4 се обобщава за всички популации и дали подаването на NDA се измества напред от текущия най-ранен прозорец Q4 2026.
Ретатрутид печели по измеренията, които имат най-голямо значение за изследователска граница: по-висок наблюдаван таван в TRIUMPH-4, широта на тройно-агонистичния механизъм и съгласувана посока в двата публикувани мрежови мета-анализа. Тирзепатид остава референтната молекула за протоколи, които се нуждаят от най-дълбоката публикувана доказателствена база днес.