

Ο τριπλός αγωνιστής που έθεσε νέα οροφή απέναντι στον διπλό αγωνιστή που οικοδόμησε την κατηγορία. Μια σύγκριση για ερευνητικά πρωτόκολλα που θέλουν να κατανοήσουν ποιο μόριο είναι το μέτωπο, ποιο είναι το πρότυπο και γιατί η διάκριση έχει σημασία.

Το Tirzepatide (το Mounjaro/Zepbound της Eli Lilly) είναι διπλός αγωνιστής των υποδοχέων GLP-1/GIP με τέσσερα έτη δεδομένων Φάσης 3, τρεις εγκρίσεις FDA και δημοσιευμένη μελέτη καρδιαγγειακών εκβάσεων. Το Retatrutide, το διάδοχο μόριο της Lilly, είναι τριπλός αγωνιστής που προσθέτει τον υποδοχέα γλυκαγόνης στον ίδιο διπλό κορμό και, στην πρώτη του ανακοίνωση Φάσης 3, παρήγαγε τη βαθύτερη μείωση βάρους που έχει ποτέ αναφερθεί σε μελέτη παχυσαρκίας για έγκριση: περίπου 28,7% στις 68 εβδ. 5 έναντι της κορυφαίας τιμής του tirzepatide στη SURMOUNT-1 περίπου 22,5% στις 72 εβδ. 13.
Οι βάσεις τεκμηρίωσης δεν είναι συμμετρικές. Το tirzepatide διαθέτει την ώριμη, αξιολογημένη από ομοτίμους υπόθεση. Το retatrutide διαθέτει υψηλότερη παρατηρούμενη οροφή, μηχανιστικά ευρύτερο προφίλ στόχου και δύο μετα-αναλύσεις δικτύου που στρέφονται προς την κατεύθυνσή του 20 21. Για ερευνητικά πρωτόκολλα που δίνουν προτεραιότητα στη μέγιστη θεραπευτική οροφή και στην ευρύτητα του μηχανισμού, η συντακτική μας επιλογή είναι το retatrutide. Για πρωτόκολλα που εκτιμούν το βάθος τεκμηρίωσης σε επίπεδο ρυθμιστικής αρχής και ένα παγιωμένο προφίλ ασφαλείας, το tirzepatide παραμένει το μόριο αναφοράς.
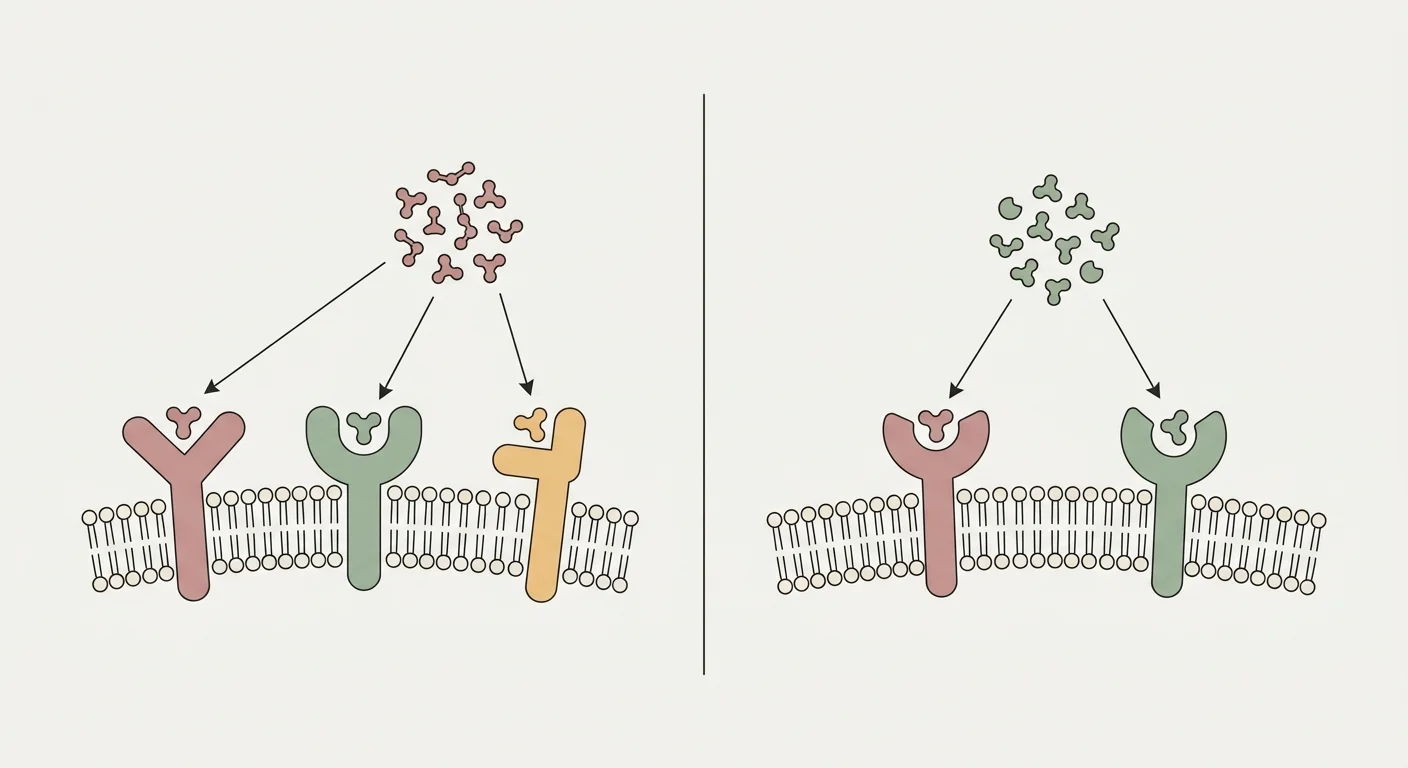
Το Retatrutide (LY3437943) είναι ένα ενιαίο πεπτίδιο σχεδιασμένο ώστε να αγωνίζεται ταυτοχρόνως τρεις υποδοχείς της οικογένειας ινκρετινών: τον υποδοχέα του γλυκαγονόμοιου πεπτιδίου-1 (GLP-1R), τον υποδοχέα του γλυκοζοεξαρτώμενου ινσουλινοτρόπου πολυπεπτιδίου (GIPR) και τον υποδοχέα της γλυκαγόνης (GCGR) 26. Το σκέλος GLP-1R καθοδηγεί την κεντρική καταστολή της όρεξης, την επιβραδυνόμενη γαστρική κένωση και την εξαρτώμενη από τη γλυκόζη έκκριση ινσουλίνης που μας είναι οικείες από το semaglutide και το tirzepatide 24. Το σκέλος GIPR προσθέτει συνεργιστική ινσουλινοτρόπο δραστηριότητα και, στον λιπώδη ιστό, ενισχύει την υγιή ρύθμιση των λιπιδίων, μειώνοντας την έκτοπη εναπόθεση λίπους στο ήπαρ και τους μυς 25.
Το διακριτικό σκέλος είναι αυτό του GCGR. Η γλυκαγόνη συνήθως πλαισιώνεται ως η αντι-ρυθμιστική ορμόνη που αυξάνει τη γλυκόζη του αίματος· στο πλαίσιο ενός ισορροπημένου τριπλού αγωνιστή, η κλασική της επίδραση στην ηπατική παραγωγή γλυκόζης αντισταθμίζεται από την ταυτόχρονη ινσουλινοτρόπο δράση των GLP-1R/GIPR, ενώ διατηρούνται οι μεταβολικές επιδράσεις που πραγματικά αναζητούν οι σχεδιαστές πεπτιδίων από τον GCGR: αυξημένη ενεργειακή δαπάνη μέσω θερμογένεσης του φαιού λιπώδους ιστού και οξείδωσης του σκελετικού μυός, λιπόλυση στον λιπώδη ιστό με απελευθέρωση ελεύθερων λιπαρών οξέων προς β-οξείδωση και ηπατική οξείδωση λιπαρών οξέων που αποβάλλει τα τριγλυκερίδια από το ήπαρ 27. Στα δεδομένα MASLD Φάσης 2a, το retatrutide παρήγαγε περίπου 85–90% μείωση του ηπατικού λίπους στην ανώτερη δόση· περίπου 90% των συμμετεχόντων στη δόση των 12 mg έφτασαν σε ηπατικό λίπος κάτω του 5% στις 48 εβδομάδες, μέγεθος που η διπλή αγωνιστική δράση δεν έχει επιδείξει .
Καμία άμεση τυχαιοποιημένη ελεγχόμενη μελέτη retatrutide έναντι tirzepatide δεν έχει δημοσιευτεί ή ανακοινωθεί έως τον Απρίλιο του 2026. Μια μελέτη απευθείας σύγκρισης για έγκριση (NCT06662383) είναι ορατή στον κατάλογο pipeline της Lilly, αλλά δεν έχει αναφερθεί κανένα αποτέλεσμα. Κάθε συγκριτικός ισχυρισμός σε αυτό το άρθρο φέρει επομένως μια επιφύλαξη: είναι είτε έμμεση σύγκριση μεταξύ μελετών με διαφορετικούς πληθυσμούς, σχήματα δοσολογίας και τελικά σημεία, είτε αποτελεί μηχανιστική προέκταση από προκλινικά δεδομένα και δεδομένα Φάσης 2. Αυτό δεν αποτελεί λόγο αγνόησης του σήματος — είναι λόγος για να το ποιοτικοποιήσουμε.
Δύο μετα-αναλύσεις δικτύου έχουν επιχειρήσει να τοποθετήσουν τα μόρια στην ίδια κλίμακα. Η ανάλυση του Οκτωβρίου 2025 που δημοσιεύτηκε στο Journal of the Endocrine Society (περίληψη SUN-659, με πλήρες αξιολογημένο από ομοτίμους άρθρο στο PMC12544991) ανέφερε για το retatrutide μέση απόλυτη μείωση −16,34 kg και −23,77% σωματικού βάρους έναντι −11,82 kg και −16,79% για το tirzepatide, ένα έμμεσο πλεονέκτημα υπέρ του retatrutide 20. Η ίδια ανάλυση επεσήμανε υψηλότερο σχετικό κίνδυνο ανεπιθύμητων ενεργειών για το retatrutide (RR 4,10 έναντι 2,78), συμβατό με υψηλότερο γαστρεντερικό φορτίο στις ανώτερες δόσεις. Μια ευρύτερη μετα-ανάλυση δικτύου επτά παραγόντων που δημοσιεύτηκε στο Metabolism (2024) κατέταξε τα μόρια ως προς την απώλεια βάρους ως retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, με συνεπείς κατατάξεις σε περιφέρεια μέσης, HbA1c και γλυκόζη πλάσματος νηστείας 21.
Και οι δύο μετα-αναλύσεις δικτύου ευνοούν το retatrutide αριθμητικά και κατευθυντικά, αλλά η απουσία άμεσων RCT μαρτυριών σημαίνει ότι κάθε συγκριτικός ισχυρισμός πρέπει να φέρει μια επιφύλαξη. Για ερευνητικούς σκοπούς, αυτός είναι λόγος για περαιτέρω διερεύνηση, όχι λόγος για να απορρίψουμε το σήμα.
Το προφίλ ασφάλειας Φάσης 2 είναι συμβατό με την κατηγορία αγωνιστών των υποδοχέων GLP-1, κυριαρχούμενο από εξαρτώμενα από τη δόση γαστρεντερικά ανεπιθύμητα συμβάντα που συγκεντρώνονται στις πρώτες μία έως δύο εβδομάδες κάθε σταδίου τιτλοποίησης. Η ασφάλεια Φάσης 3 (TRIUMPH-4) είναι διαθέσιμη μόνο ως πρώτη ανακοίνωση δελτίου τύπου τον Απρίλιο του 2026 και δεν έχει ακόμα αξιολογηθεί από ομοτίμους σε ανάλυση πλήρους συνόλου δεδομένων.
Η πρώτη ανακοίνωση της TRIUMPH-4 αναφέρει ~28,7% μείωση στις 68 εβδομάδες, ξεπερνώντας την κορυφαία τιμή της SURMOUNT-1 του tirzepatide στις 72 εβδομάδες κατά περίπου έξι ποσοστιαίες μονάδες. Και οι δύο δημοσιευμένες μετα-αναλύσεις δικτύου στρέφονται στην ίδια κατεύθυνση.
Το σκέλος GCGR προσθέτει οδούς που στερείται το tirzepatide: ηπατική οξείδωση λιπαρών οξέων (~85–90% μείωση ηπατικού λίπους σε MASLD Φάσης 2a), λιπόλυση στον λιπώδη ιστό και θερμογενετική ενεργειακή δαπάνη.
Δώδεκα και άνω μελέτες Φάσης 3, τρεις εγκρίσεις FDA, μια δημοσιευμένη CVOT σε 13.165 ασθενείς και ένα ώριμο φάκελο ασφαλείας στις πληροφορίες συνταγογράφησης. Το μόριο αναφοράς για έρευνα GLP-1/GIP σήμερα.
Η SURPASS-2 νίκησε το semaglutide 1 mg σε άμεση σύγκριση ως προς την HbA1c· η SURPASS-CVOT είναι η μοναδική δημοσιευμένη μελέτη καρδιαγγειακών εκβάσεων μεταξύ των δύο μορίων. Οι μαρτυρίες του retatrutide για T2D παραμένουν σε Φάση 2 (Rosenstock 2023).
Το tirzepatide είναι διπλός αγωνιστής στους GLP-1R και GIPR· το retatrutide προσθέτει τον υποδοχέα της γλυκαγόνης (GCGR) ως τρίτο στόχο 26. Το σκέλος GCGR συνεισφέρει ηπατική οξείδωση λιπαρών οξέων, λιπόλυση στον λιπώδη ιστό και θερμογενετική ενεργειακή δαπάνη που η διπλή αγωνιστική δράση δεν εμπλέκει εκ σχεδιασμού 27.
Το tirzepatide, αναμφισβήτητα. Δώδεκα και άνω μελέτες Φάσης 3, τρεις εγκρίσεις FDA και μια δημοσιευμένη μελέτη καρδιαγγειακών εκβάσεων σε 13.165 ασθενείς 12. Το retatrutide διαθέτει μία πρώτη ανακοίνωση Φάσης 3 (TRIUMPH-4) και ένα πρόγραμμα Φάσης 2 περίπου έξι αξιολογημένων από ομοτίμους δημοσιεύσεων 1 5. Το χάσμα θα στενέψει κατά τη διάρκεια του 2026 καθώς θα ανακοινωθούν τα αποτελέσματα των TRIUMPH-1, TRIUMPH-2 και TRIUMPH-3.
Όχι. Καμία άμεση RCT retatrutide έναντι tirzepatide δεν έχει δημοσιευτεί ή ανακοινωθεί δημόσια έως τον Απρίλιο του 2026. Οι συγκριτικές μαρτυρίες περιορίζονται σε δύο έμμεσες μετα-αναλύσεις δικτύου, που και οι δύο στρέφονται προς την κατεύθυνση του retatrutide αλλά δεν μπορούν να υποκαταστήσουν μια μελέτη άμεσης σύγκρισης .
Το retatrutide είναι η επιλογή μας. Όχι επειδή διαθέτει περισσότερα δεδομένα μελετών — δεν διαθέτει. Το πρόγραμμα Φάσης 3 του tirzepatide είναι κατά τέσσερα έτη βαθύτερο, οι τρεις εγκρίσεις του από τον FDA καλύπτουν τον διαβήτη τύπου 2, τη χρόνια διαχείριση βάρους και την αποφρακτική υπνική άπνοια, και η δημοσιευμένη του μελέτη καρδιαγγειακών εκβάσεων σε περισσότερους από δεκατρείς χιλιάδες ασθενείς είναι ένα γεγονός που δεν αμφισβητούμε 12 28. Για ερευνητικά πρωτόκολλα που χρειάζονται τη βαθύτερη, την πιο εξονυχιστικά εξεταζόμενη βάση τεκμηρίωσης που είναι σήμερα διαθέσιμη στην κατηγορία των ινκρετινών, το tirzepatide είναι το μόριο αναφοράς και θα παραμείνει έτσι μέχρι την ολοκλήρωση του προγράμματος TRIUMPH.
Για ερευνητικά πρωτόκολλα όμως που επιδιώκουν την υψηλότερη θεραπευτική οροφή, οι αριθμοί ευνοούν το retatrutide. Η πρώτη του ανακοίνωση Φάσης 3 ανέφερε περίπου 28,7% μείωση βάρους στα 12 mg σε 68 εβδομάδες 5— ένα ουσιαστικό πλεονέκτημα οροφής έξι ποσοστιαίων μονάδων έναντι της κορυφαίας τιμής 22,5% του tirzepatide στη SURMOUNT-1 σε 72 εβδομάδες 13. Η μηχανιστική εξήγηση δεν είναι θεωρητική: ο υποδοχέας γλυκαγόνης προσθέτει ηπατική οξείδωση λιπαρών οξέων, λιπόλυση στον λιπώδη ιστό και θερμογενετική ενεργειακή δαπάνη που η διπλή αγωνιστική δράση δεν μπορεί να εμπλέξει εκ σχεδιασμού 27, και η μείωση ηπατικού λίπους κατά 85–90% στην ανακοίνωση MASLD Φάσης 2a αποτελεί άμεση υπογραφή αυτής της οδού 3. Και οι δύο δημοσιευμένες μετα-αναλύσεις δικτύου στρέφονται προς την κατεύθυνση του retatrutide 20 21. Η βάση τεκμηρίωσης θα ωριμάσει· η οροφή, εκ σχεδιασμού, δεν θα μετακινηθεί προς τα κάτω.
Για το ερευνητικό μέτωπο της μεταβολικής πεπτιδικής θεραπείας, το retatrutide είναι ο νικητής. Για πρωτόκολλα που εκτιμούν το βάθος επιπέδου ρυθμιστικής αρχής πάνω απ' όλα, το tirzepatide παραμένει το πρότυπο. Αυτή είναι μια σαφέστερη κατανομή ρόλων από όση μπορούν να προσφέρουν οι περισσότερες συγκρίσεις «X έναντι Y», και η ειλικρίνεια ως προς αυτή την κατανομή είναι πιο χρήσιμη από έναν εξαναγκασμένο μοναδικό νικητή.
Παρόν· ~85–90% μείωση ηπατικού λίπους σε MASLD Φάσης 2a 3
Απουσιάζει εκ σχεδιασμού
~144 ώρες (~6 ημέρες)
~120 ώρες (~5 ημέρες)
1 πρώτη ανακοίνωση (TRIUMPH-4)· εκκρεμούν TRIUMPH-1/2/3 4
12+ (SURPASS 1–6, CVOT, PEDS· SURMOUNT 1–5, OSA)
Καμία (δεν έχει ξεκινήσει CVOT)
SURPASS-CVOT (n=13.165· NEJM Δεκ 2025) 12
Καμία (καμία εγκεκριμένη ετικέτα)
MTC κύτταρα C θυρεοειδούς (τρωκτικά, ανθρώπινη συνάφεια μη τεκμηριωμένη) 28
Καμία δημοσιευμένη
Καμία δημοσιευμένη
Μία φορά εβδομαδιαίως, υποδορίως
Μία φορά εβδομαδιαίως, υποδορίως
ΗΠΑ: ενωρίτερα τέλη 2027 (NDA Q4 2026 το συντομότερο) 22
Ήδη εγκεκριμένο (ΗΠΑ: 2022/2023/2024· ΕΕ: 2022/2024)
Λυοφιλιωμένο· ανασύσταση με βακτηριοστατικό ύδωρ· 2–8 °C
Λυοφιλιωμένο· ανασύσταση με βακτηριοστατικό ύδωρ· 2–8 °C
Υψηλότερη οροφή + ευρύτητα υποδοχέα γλυκαγόνης
Χαμηλότερη οροφή· καλύτερα χαρακτηρισμένο φάκελο ασφαλείας
Το Tirzepatide (LY3298176) είναι διπλός αγωνιστής GLP-1R / GIPR — ένα ενιαίο πεπτίδιο 39 καταλοίπων ρυθμισμένο ώστε να αλληλεπιδρά και με τους δύο υποδοχείς ινκρετινών με συγκρίσιμη δραστικότητα. Το σκέλος GLP-1R συνεισφέρει τον ίδιο πυρηνικό μηχανισμό που μας είναι οικείος από την πρώτη γενιά αναλόγων GLP-1: εξαρτώμενη από τη γλυκόζη έκκριση ινσουλίνης, καταστολή της γλυκαγόνης από τα α-κύτταρα, υποθαλαμική ρύθμιση της όρεξης και επιβράδυνση της γαστρικής κένωσης 24.
Αυτό που διαφοροποιεί το tirzepatide από τους καθαρούς αγωνιστές GLP-1 είναι η πρόσθετη δραστηριότητα GIPR. Σε προκλινικό επίπεδο, η συγχορήγηση GIP με GLP-1 παράγει αθροιστικές και, σε ορισμένες παραμέτρους, συνεργιστικές μειώσεις στο σωματικό βάρος και τη γλυκόζη, μεγαλύτερες απ' ό,τι κάθε ένα μόνο του 25. Η κεντρική ενεργοποίηση του GIPR φαίνεται να ενισχύει την προκαλούμενη από το GLP-1 ανορεξία μέσω υποθαλαμικής σηματοδότησης POMC· η περιφερική ενεργοποίηση του GIPR στον λευκό λιπώδη ιστό ενισχύει τη ρυθμιστική ικανότητα της δεξαμενής και μειώνει την ανάγκη έκτοπης εναπόθεσης. Η παρατηρήσιμη συνέπεια είναι το πιο ισχυρό προφίλ μείωσης βάρους και γλυκόζης από οποιοδήποτε μόριο εγκεκριμένο πριν από το retatrutide: η SURMOUNT-1 ανέφερε περίπου 22,5% μείωση βάρους στη δόση των 15 mg σε διάστημα 72 εβδομάδων 13, και η SURMOUNT-5 έδειξε το tirzepatide ανώτερο του semaglutide 2,4 mg σε άμεση σύγκριση στις 72 εβδομάδες (−20,2% έναντι −13,7%) 18.
Το σκέλος του υποδοχέα γλυκαγόνης αποτελεί τον μηχανιστικό διαφοροποιητή του retatrutide. Τα προκλινικά δεδομένα και τα δεδομένα Φάσης 2 υποδηλώνουν ότι αυτό μεταφράζεται σε επιδράσεις μείωσης λιπιδίων, μείωσης ηπατικού λίπους και ενεργειακής δαπάνης τις οποίες, εκ σχεδιασμού, στερείται το tirzepatide. Το αν αυτό μεταφράζεται σε πλεονέκτημα άμεσης σύγκρισης που υπονοείται από τις μετα-αναλύσεις δικτύου θα παραμείνει ανοικτό μέχρι να ανακοινωθούν τα αποτελέσματα μιας RCT άμεσης σύγκρισης — η οποία, μέχρι τον Απρίλιο του 2026, δεν έχει ακόμα ανακοινωθεί.
Το βάθος τεκμηρίωσης του tirzepatide είναι ασύγκριτο σήμερα — δώδεκα μελέτες Φάσης 3 σε δύο προγράμματα νόσων, μια δημοσιευμένη μελέτη καρδιαγγειακών εκβάσεων σε περισσότερους από δεκατρείς χιλιάδες ασθενείς και τρεις εγκρίσεις FDA στην ετικέτα. Η διαθέσιμη ανακοίνωση του retatrutide, αν και μοναδική, ξεπερνά την καλύτερη οροφή Φάσης 3 του tirzepatide σε βραχύτερο παράθυρο παρατήρησης. Αυτό είναι σήμα που αξίζει σοβαρής προσοχής καθώς οι TRIUMPH-1, TRIUMPH-2 και TRIUMPH-3 ωριμάζουν κατά τη διάρκεια του 2026 και του 2027.
Ώριμος φάκελος ασφαλείας στις πληροφορίες συνταγογράφησης για Mounjaro και Zepbound. Οι κοινές ανεπιθύμητες ενέργειες αντικατοπτρίζουν την κατηγορία GLP-1 και συγκεντρώνονται στην τιτλοποίηση δόσης· οι σοβαροί κίνδυνοι αποτυπώνονται σε προειδοποίηση εντός πλαισίου και σε σύνολο προειδοποιήσεων και προφυλάξεων εξευγενισμένων μέσω της επαγρύπνησης μετά τη διάθεση στην αγορά (ανάλυση FAERS 2024 και φαρμακοεπαγρύπνηση EMA).
Αυτό το άρθρο είναι μια συντακτική σύγκριση που έχει ετοιμαστεί για αναγνώστες σε ερευνητικό πλαίσιο. Ούτε το retatrutide ούτε το tirzepatide προσφέρονται ή συνιστώνται για αυτοχορήγηση από ανθρώπους μέσω αυτού του ιστοτόπου. Όπου το tirzepatide συνταγογραφείται, διατίθεται μόνο υπό την επίβλεψη ιατρού σε δικαιοδοσίες όπου έχει εγκριθεί (Mounjaro για T2D· Zepbound για χρόνια διαχείριση βάρους και αποφρακτική υπνική άπνοια). Το retatrutide είναι ερευνητικό σε παγκόσμια κλίμακα τον Απρίλιο του 2026 και πρέπει να χρησιμοποιείται μόνο εντός κατάλληλων ερευνητικών πρωτοκόλλων.
Τα δεδομένα ασφάλειας που συνοψίζονται εδώ αντικατοπτρίζουν δημοσιευμένα σύνολα δεδομένων Φάσης 2 και Φάσης 3 και τις τρέχουσες πληροφορίες συνταγογράφησης. Νέα σήματα μπορούν να εμφανιστούν ανά πάσα στιγμή· η ημερομηνία lastUpdated σε αυτή τη σελίδα υποδεικνύει το χρονικό όριο της ανασκόπησής μας. Τίποτα σε αυτή τη σελίδα δεν συνιστά ιατρική συμβουλή ή υποκατάστατο διαβούλευσης με εξειδικευμένο κλινικό ιατρό.
Το tirzepatide είναι εγκεκριμένο υπό δύο εμπορικές ονομασίες: Mounjaro για διαβήτη τύπου 2 (FDA Μάιος 2022) και Zepbound για χρόνια διαχείριση βάρους (Νοέμβριος 2023) και μέτρια έως σοβαρή αποφρακτική υπνική άπνοια με παχυσαρκία (Δεκέμβριος 2024) 28. Το retatrutide είναι ερευνητικό παντού· κανένα NDA δεν έχει υποβληθεί έως τον Απρίλιο του 2026 22.
Το retatrutide, με βάση τα διαθέσιμα δεδομένα. Η TRIUMPH-4 ανέφερε ~−28,7% στα 12 mg σε 68 εβδομάδες 5· η καλύτερη ανακοίνωση Φάσης 3 του tirzepatide για παχυσαρκία, η SURMOUNT-1 στα 15 mg σε 72 εβδομάδες, ήταν ~−22,5% 13. Και οι δύο δημοσιευμένες μετα-αναλύσεις δικτύου κατατάσσουν το retatrutide υψηλότερα ως προς τη μείωση σωματικού βάρους 20 21.
Σε επίπεδο κατηγορίας, και τα δύο έχουν προφίλ κυριαρχούμενο από γαστρεντερικά συμπτώματα (ναυτία, έμετος, διάρροια) που συγκεντρώνεται στην τιτλοποίηση δόσης. Η μετα-ανάλυση δικτύου του Οκτωβρίου 2025 ανέφερε υψηλότερο σχετικό κίνδυνο ανεπιθύμητων ενεργειών για το retatrutide (RR 4,10) απ' ό,τι για το tirzepatide (RR 2,78), συμβατό με υψηλότερο γαστρεντερικό φορτίο στις ανώτερες δόσεις 20. Το tirzepatide φέρει προειδοποίηση εντός πλαισίου για MTC και χαρακτηρισμένο προφίλ παγκρεατίτιδας / χοληδόχου κύστης / υπερευαισθησίας 28 29· ο αντίστοιχος μακροπρόθεσμος φάκελος ασφαλείας του retatrutide δεν έχει τεκμηριωθεί.
Οι δημοσιευμένες μελέτες Φάσης 2 και Φάσης 3 και για τα δύο μόρια ενσωματώνουν συμμετέχοντες ως μονοθεραπεία (με ή χωρίς υποκείμενη θεραπεία T2D όπως μετφορμίνη ή ινσουλίνη). Δεν υπάρχουν δημοσιευμένα στοιχεία για τη σύνδεση κανενός από τα δύο με άλλα ερευνητικά πεπτίδια. Κάθε πρωτόκολλο συνδυασμού είναι αυστηρά ερευνητικό και εκτός της βάσης τεκμηρίωσης που συνοψίζεται σε αυτό το άρθρο.
Ο χρόνος ημίσειας ζωής του retatrutide ~144 ωρών και του tirzepatide ~120 ωρών υποστηρίζουν αμφότεροι μία εβδομαδιαία υποδόρια δόση, το σχήμα που χρησιμοποιήθηκε σε κάθε μελέτη για έγκριση. Ο ελαφρώς μεγαλύτερος χρόνος ημίσειας ζωής του retatrutide παρέχει μέτριο περιθώριο έναντι της μεταβλητότητας από παραλειπόμενη δόση αλλά δεν αλλάζει τον θεμελιώδη ρυθμό μίας φοράς εβδομαδιαίως.
Ναι. Τόσο το retatrutide όσο και το tirzepatide είναι καταχωρημένα για ερευνητική χρήση και στα δύο κανάλια ΕΕ και ΗΠΑ. Η διαθεσιμότητα, τα μεγέθη φιαλιδίων και η τιμολόγηση ανά κανάλι φαίνονται στη σελίδα λεπτομερειών κάθε προϊόντος.
Αναμένονται κατά τη διάρκεια του 2026 οι ανακοινώσεις των TRIUMPH-1 (παχυσαρκία χωρίς T2D), TRIUMPH-2 (παχυσαρκία με T2D) και TRIUMPH-3 (παχυσαρκία με τεκμηριωμένη καρδιαγγειακή νόσο) σύμφωνα με την καθοδήγηση της Lilly 4. Καθεμία θα διευρύνει ουσιαστικά τη βάση τεκμηρίωσης του retatrutide· συλλογικά θα καθορίσουν αν η οροφή της TRIUMPH-4 γενικεύεται σε όλους τους πληθυσμούς και αν μια κατάθεση NDA μετατοπιστεί από το τρέχον πλαίσιο νωρίτερα από το τέταρτο τρίμηνο του 2026.
Το tirzepatide. Έξι μελέτες SURPASS Φάσης 3 συν την SURPASS-CVOT του προσφέρουν τη βαθύτερη γλυκαιμική βάση τεκμηρίωσης από οποιοδήποτε μόριο της κατηγορίας ινκρετινών 7 12. Τα δεδομένα του retatrutide για T2D παραμένουν σε Φάση 2 (Rosenstock 2023)· η TRIUMPH-2 δεν έχει ακόμα ανακοινώσει αποτελέσματα 2.
Το retatrutide υπερτερεί στις διαστάσεις που έχουν τη μεγαλύτερη σημασία για έρευνα στο μέτωπο: υψηλότερη παρατηρούμενη οροφή στη TRIUMPH-4, ευρύτητα μηχανισμού τριπλού αγωνιστή και συνεπή κατεύθυνση και στις δύο δημοσιευμένες μετα-αναλύσεις δικτύου. Το tirzepatide παραμένει το μόριο αναφοράς για πρωτόκολλα που χρειάζονται τη βαθύτερη δημοσιευμένη βάση τεκμηρίωσης σήμερα.