

Il triplo agonista che ha fissato un nuovo tetto di efficacia contro il doppio agonista che ha definito la categoria. Un confronto pensato per i protocolli di ricerca che vogliono capire quale molecola rappresenti la frontiera, quale lo standard e perché questa distinzione conta.

Tirzepatide (Mounjaro/Zepbound di Eli Lilly) è un doppio agonista dei recettori GLP-1/GIP, con quattro anni di dati di Fase 3, tre approvazioni FDA e uno studio sugli outcome cardiovascolari pubblicato. Retatrutide, la molecola successiva di Lilly, è un triplo agonista che aggiunge il recettore del glucagone allo stesso scheletro doppio e, nella sua prima lettura di Fase 3, ha prodotto la riduzione ponderale più profonda mai riportata in uno studio registrativo sull’obesità: circa il 28,7% a 68 settimane 5 contro il picco di tirzepatide nello SURMOUNT-1, pari a circa il 22,5% a 72 settimane 13.
Le basi probatorie non sono simmetriche. Tirzepatide vanta un dossier maturo, sottoposto a peer review. Retatrutide presenta un tetto di efficacia osservato più alto, un profilo recettoriale meccanicamente più ampio e due meta-analisi di rete che puntano nella sua direzione 20 21. Per i protocolli di ricerca che privilegiano il massimo tetto terapeutico e l’ampiezza meccanicistica, la nostra scelta editoriale è retatrutide. Per i protocolli che valorizzano la profondità delle evidenze di livello regolatorio e un’etichetta di sicurezza consolidata, tirzepatide rimane la molecola di riferimento.
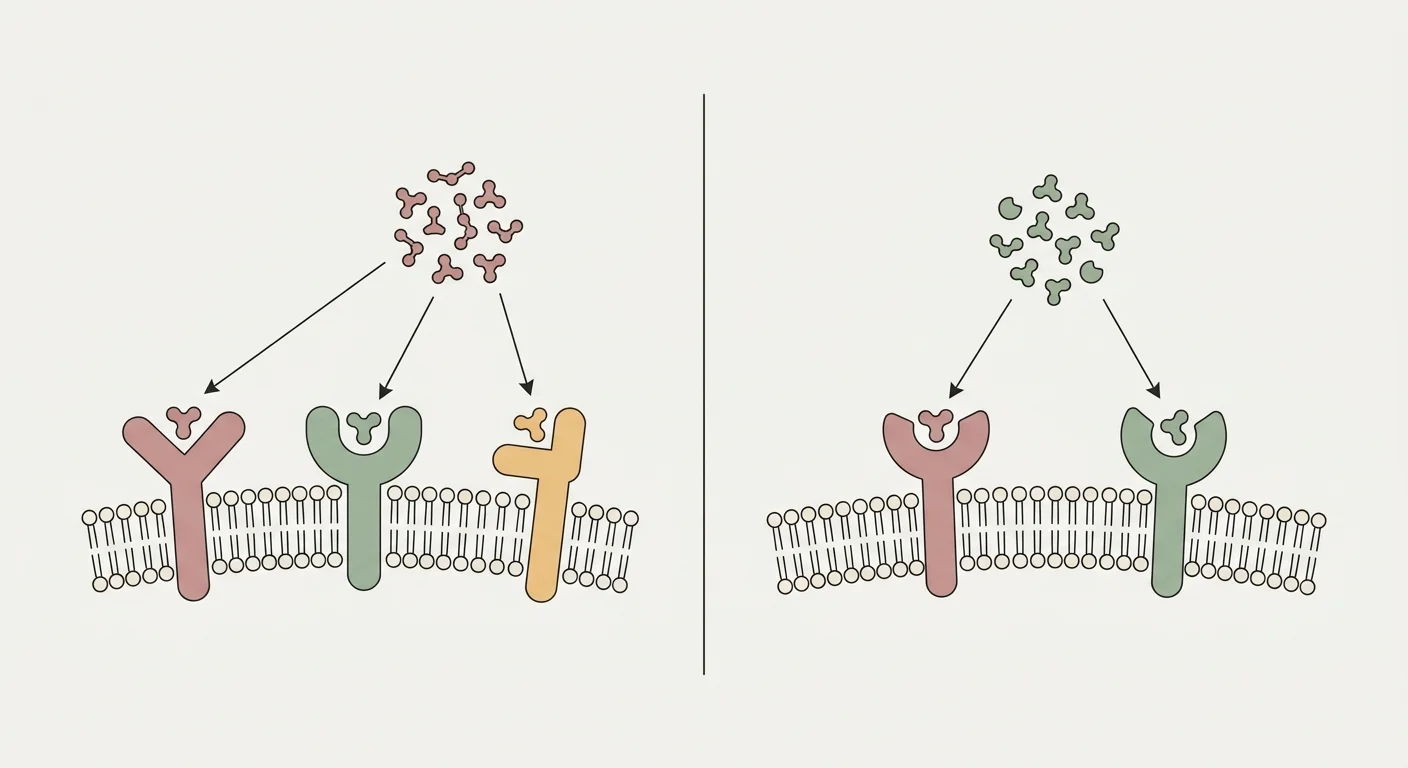
Retatrutide (LY3437943) è un singolo peptide progettato per attivare contemporaneamente tre recettori della famiglia delle incretine: il recettore del peptide-1 simile al glucagone (GLP-1R), il recettore del polipeptide insulinotropico glucosio-dipendente (GIPR) e il recettore del glucagone (GCGR) 26. La componente GLP-1R guida la soppressione centrale dell’appetito, il rallentamento dello svuotamento gastrico e la secrezione insulinica glucosio-dipendente, già nota da semaglutide e tirzepatide 24. La componente GIPR aggiunge un’attività insulinotropica sinergica e, nel tessuto adiposo, potenzia il buffering lipidico fisiologico, riducendo la deposizione di grasso ectopico nel fegato e nei muscoli 25.
La componente distintiva è il GCGR. Il glucagone è solitamente descritto come l’ormone controregolatorio che innalza la glicemia; nel contesto di un triplo agonista bilanciato, il suo effetto classico sulla produzione epatica di glucosio è compensato dall’azione insulinotropica simultanea su GLP-1R/GIPR, mentre vengono preservati gli effetti metabolici che i progettisti di peptidi cercano realmente nel GCGR: aumento del dispendio energetico tramite termogenesi nel tessuto adiposo bruno e ossidazione muscolare scheletrica, lipolisi adiposa con rilascio di acidi grassi liberi per la beta-ossidazione e ossidazione epatica degli acidi grassi che rimuove i trigliceridi dal fegato 27. Nei dati di Fase 2a sulla MASLD, retatrutide ha prodotto una riduzione del grasso epatico di circa l’85–90% alla dose massima; circa il 90% dei partecipanti a 12 mg ha raggiunto un grasso epatico inferiore al 5% a 48 settimane, una magnitudine che il doppio agonismo non ha dimostrato .
Ad aprile 2026 non è stato pubblicato né annunciato alcuno studio randomizzato controllato diretto tra retatrutide e tirzepatide. Uno studio registrativo testa a testa (NCT06662383) compare nel tracker di pipeline di Lilly, ma non sono stati riportati risultati. Ogni affermazione comparativa in questo articolo porta quindi una riserva: si tratta o di un confronto indiretto tra studi con popolazioni, schemi di dosaggio ed endpoint differenti, oppure di un’estrapolazione meccanicistica da dati preclinici e di Fase 2. Non è una ragione per ignorare il segnale, ma per qualificarlo.
Due meta-analisi di rete hanno tentato di collocare le molecole sulla stessa scala. L’analisi di ottobre 2025 pubblicata nel Journal of the Endocrine Society (abstract SUN-659, con articolo completo sottoposto a peer review su PMC12544991) ha riportato per retatrutide una riduzione assoluta media di −16,34 kg e −23,77% del peso corporeo, contro −11,82 kg e −16,79% per tirzepatide, un vantaggio indiretto a favore di retatrutide 20. La stessa analisi ha segnalato un rischio relativo più alto di eventi avversi per retatrutide (RR 4,10 vs 2,78), coerente con un carico gastrointestinale maggiore alle dosi superiori. Una meta-analisi di rete più ampia, su sette molecole, pubblicata su Metabolism (2024) ha classificato i farmaci per perdita di peso nell’ordine retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, con classifiche coerenti su circonferenza vita, HbA1c e glicemia plasmatica a digiuno 21.
Entrambe le meta-analisi di rete favoriscono retatrutide sia numericamente sia direzionalmente, ma l’assenza di evidenze RCT dirette impone una riserva su qualsiasi affermazione comparativa. Per finalità di ricerca, è una ragione per approfondire l’indagine, non per liquidare il segnale.
Il profilo di sicurezza di Fase 2 è coerente con la classe degli agonisti del recettore GLP-1, dominato da eventi avversi gastrointestinali dose-dipendenti che si concentrano nelle prime una o due settimane di ciascuno step di escalation. La sicurezza di Fase 3 (TRIUMPH-4) è disponibile ad aprile 2026 solo come top-line da comunicato stampa e non è ancora stata sottoposta a peer review con risoluzione completa del dataset.
La top-line di TRIUMPH-4 riporta una riduzione di circa il 28,7% a 68 settimane, superando il picco di tirzepatide nello SURMOUNT-1 a 72 settimane di circa sei punti percentuali. Entrambe le meta-analisi di rete pubblicate puntano nella stessa direzione.
La componente GCGR aggiunge vie che tirzepatide non possiede: ossidazione epatica degli acidi grassi (~85–90% di riduzione del grasso epatico nella MASLD di Fase 2a), lipolisi adiposa e dispendio energetico termogenico.
Più di dodici studi di Fase 3, tre approvazioni FDA, un CVOT pubblicato su 13.165 pazienti e un profilo di sicurezza maturo nelle informazioni di prescrizione. La molecola di riferimento per la ricerca su GLP-1/GIP oggi.
SURPASS-2 ha battuto semaglutide 1 mg testa a testa sull’HbA1c; SURPASS-CVOT è l’unico studio pubblicato sugli outcome cardiovascolari per entrambe le molecole. Le evidenze di retatrutide nel T2D restano in Fase 2 (Rosenstock 2023).
Tirzepatide è un doppio agonista di GLP-1R e GIPR; retatrutide aggiunge il recettore del glucagone (GCGR) come terzo bersaglio 26. La componente GCGR contribuisce con ossidazione epatica degli acidi grassi, lipolisi adiposa e dispendio energetico termogenico, vie che il doppio agonismo per progettazione non attiva 27.
Tirzepatide, senza ambiguità. Più di dodici studi di Fase 3, tre approvazioni FDA e uno studio pubblicato sugli outcome cardiovascolari su 13.165 pazienti 12. Retatrutide ha una top-line di Fase 3 (TRIUMPH-4) e un programma di Fase 2 di circa sei pubblicazioni sottoposte a peer review 1 5. Il divario si ridurrà nel corso del 2026 con le letture di TRIUMPH-1, TRIUMPH-2 e TRIUMPH-3.
No. Ad aprile 2026 non è stato pubblicato né riportato pubblicamente alcun RCT diretto retatrutide vs tirzepatide. Le evidenze comparative si limitano a due meta-analisi di rete indirette, che puntano entrambe nella direzione di retatrutide ma non possono sostituire uno studio testa a testa 20 .
La nostra scelta è retatrutide. Non perché disponga di più dati clinici, perché non li ha. Il programma di Fase 3 di tirzepatide è più profondo di quattro anni, le sue tre approvazioni FDA coprono il diabete di tipo 2, la gestione cronica del peso e l’apnea ostruttiva del sonno, e il suo studio pubblicato sugli outcome cardiovascolari su oltre tredicimila pazienti è un dato che non contestiamo 12 28. Per i protocolli di ricerca che richiedono la base probatoria più profonda e meglio scrutinata oggi disponibile nella classe delle incretine, tirzepatide è la molecola di riferimento e rimarrà tale fino al completamento del programma TRIUMPH.
Ma per i protocolli di ricerca che inseguono il tetto terapeutico più alto, i numeri favoriscono retatrutide. La sua prima lettura di Fase 3 ha riportato una riduzione ponderale di circa il 28,7% a 12 mg in 68 settimane 5— un significativo vantaggio di sei punti percentuali sul tetto rispetto al picco di tirzepatide nello SURMOUNT-1, pari al 22,5% in 72 settimane 13. La spiegazione meccanicistica non è speculativa: il recettore del glucagone aggiunge ossidazione epatica degli acidi grassi, lipolisi adiposa e dispendio energetico termogenico, vie che il doppio agonismo per progettazione non può attivare 27, e la riduzione del grasso epatico dell’85–90% nella lettura di Fase 2a sulla MASLD è una firma diretta di tale via 3. Entrambe le meta-analisi di rete pubblicate puntano nella direzione di retatrutide 20 21. La base probatoria maturerà; il tetto, per progettazione, non si abbasserà.
Per la frontiera della ricerca sulla terapia peptidica metabolica, retatrutide è il vincitore. Per i protocolli che valorizzano la profondità di livello regolatorio sopra ogni altra cosa, tirzepatide rimane lo standard. È una divisione di ruoli più chiara di quanto la maggior parte dei confronti «X vs Y» possa offrire, e la franchezza su questa divisione è più utile di un vincitore unico forzato.
Presente; ~85–90% di riduzione del grasso epatico nella MASLD di Fase 2a 3
Assente per progettazione
~144 h (~6 giorni)
~120 h (~5 giorni)
1 top-line (TRIUMPH-4); TRIUMPH-1/2/3 in attesa 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Nessuno (nessun CVOT avviato)
SURPASS-CVOT (n=13.165; NEJM dic 2025) 12
Nessuna (nessuna etichetta approvata)
Cellule C tiroidee MTC (roditore, rilevanza umana non stabilita) 28
Nessuno pubblicato
Nessuno pubblicato
Una volta a settimana, sottocutanea
Una volta a settimana, sottocutanea
USA: fine 2027 al più presto (NDA Q4 2026 nello scenario migliore) 22
Già approvata (USA: 2022/2023/2024; UE: 2022/2024)
Liofilizzato; ricostituzione con acqua BAC; 2–8 °C
Liofilizzato; ricostituzione con acqua BAC; 2–8 °C
Tetto più alto + ampiezza data dal recettore del glucagone
Tetto più basso; profilo di sicurezza meglio caratterizzato
Tirzepatide (LY3298176) è un doppio agonista GLP-1R / GIPR, un singolo peptide di 39 residui calibrato per impegnare entrambi i recettori delle incretine con potenza paragonabile. La componente GLP-1R contribuisce con lo stesso meccanismo centrale già noto dalla prima generazione di analoghi del GLP-1: secrezione insulinica glucosio-dipendente, soppressione del glucagone delle cellule alfa, regolazione ipotalamica dell’appetito e rallentamento dello svuotamento gastrico 24.
Ciò che distingue tirzepatide dai puri agonisti del GLP-1 è l’aggiunta dell’attività GIPR. In modelli preclinici, la co-somministrazione di GIP con GLP-1 produce riduzioni additive e, su alcuni parametri, sinergiche del peso corporeo e della glicemia, superiori a quelle ottenute con ciascun agonista da solo 25. L’attivazione centrale del GIPR sembra potenziare l’anoressia indotta dal GLP-1 tramite il segnale ipotalamico POMC; l’attivazione periferica del GIPR nel tessuto adiposo bianco amplia la capacità di buffering del deposito e riduce la necessità di deposizione ectopica. La conseguenza osservabile è il profilo più potente di riduzione del peso e della glicemia di qualsiasi molecola approvata prima di retatrutide: SURMOUNT-1 ha riportato una riduzione ponderale di circa il 22,5% alla dose di 15 mg in 72 settimane 13, e SURMOUNT-5 ha mostrato la superiorità di tirzepatide su semaglutide 2,4 mg in confronto diretto a 72 settimane (−20,2% vs −13,7%) 18.
La componente recettoriale del glucagone è il differenziatore meccanicistico di retatrutide. I dati preclinici e di Fase 2 suggeriscono che ciò si traduca in effetti di riduzione lipidica, di riduzione del grasso epatico e di aumento del dispendio energetico che tirzepatide, per progettazione, non possiede. Se questo si tradurrà nel vantaggio diretto suggerito dalle meta-analisi di rete resterà aperto fino alla lettura di un RCT testa a testa — che, ad aprile 2026, non risulta annunciato.
La profondità delle evidenze di tirzepatide è oggi ineguagliata: dodici studi di Fase 3 in due programmi terapeutici, uno studio pubblicato sugli outcome cardiovascolari su oltre tredicimila pazienti e tre approvazioni FDA in etichetta. La lettura disponibile per retatrutide, sebbene singola, supera il miglior tetto di Fase 3 di tirzepatide in una finestra di osservazione più breve. È un segnale che merita attenzione seria man mano che TRIUMPH-1, TRIUMPH-2 e TRIUMPH-3 maturano nel corso del 2026 e del 2027.
Profilo di sicurezza maturo nelle informazioni di prescrizione di Mounjaro e Zepbound. Gli eventi avversi comuni rispecchiano la classe GLP-1 e si concentrano in fase di escalation; i rischi gravi sono raccolti in un’avvertenza in cornice e in una serie di avvertenze e precauzioni affinate dalla sorveglianza post-marketing (analisi FAERS 2024 e farmacovigilanza EMA).
Questo articolo è un confronto editoriale rivolto a lettori in contesto di ricerca. Né retatrutide né tirzepatide sono offerti o raccomandati per l’auto-somministrazione umana attraverso questo sito. Dove tirzepatide è prescritto, è disponibile solo sotto la supervisione di un medico nelle giurisdizioni in cui è stato approvato (Mounjaro per il T2D; Zepbound per la gestione cronica del peso e per l’apnea ostruttiva del sonno). Retatrutide è sperimentale a livello globale ad aprile 2026 e dovrebbe essere maneggiato esclusivamente nell’ambito di protocolli di ricerca appropriati.
I dati di sicurezza qui sintetizzati riflettono i dataset di Fase 2 e Fase 3 pubblicati e le informazioni di prescrizione attuali. Nuovi segnali possono emergere in qualsiasi momento; la data di lastUpdated su questa pagina indica il limite della nostra revisione. Nulla in questa pagina costituisce consiglio medico né sostituisce la consulenza di un clinico qualificato.
Tirzepatide è approvato con due nomi commerciali: Mounjaro per il diabete di tipo 2 (FDA, maggio 2022) e Zepbound per la gestione cronica del peso (novembre 2023) e per l’apnea ostruttiva del sonno da moderata a grave con obesità (dicembre 2024) 28. Retatrutide è sperimentale ovunque; ad aprile 2026 nessuna NDA è stata depositata 22.
Retatrutide, sulla base dei dati disponibili. TRIUMPH-4 ha riportato ~−28,7% a 12 mg in 68 settimane 5; la migliore lettura di Fase 3 sull’obesità di tirzepatide, SURMOUNT-1 a 15 mg in 72 settimane, è stata di ~−22,5% 13. Entrambe le meta-analisi di rete pubblicate classificano retatrutide più in alto sulla riduzione del peso corporeo 20 21.
A livello di classe, entrambe presentano un profilo a dominanza gastrointestinale (nausea, vomito, diarrea) che si concentra in fase di escalation. La meta-analisi di rete di ottobre 2025 ha riportato un rischio relativo di eventi avversi più alto per retatrutide (RR 4,10) rispetto a tirzepatide (RR 2,78), coerente con un carico gastrointestinale maggiore alle dosi più elevate 20. Tirzepatide reca un’avvertenza in cornice per MTC e un profilo caratterizzato di pancreatite, malattia della colecisti e ipersensibilità 28 29; il profilo di sicurezza analogo a lungo termine di retatrutide non è stato stabilito.
Gli studi di Fase 2 e Fase 3 pubblicati per entrambe le molecole arruolano i partecipanti in monoterapia (con o senza terapia di base per il T2D, come metformina o insulina). Non esistono evidenze pubblicate sulla combinazione con altri peptidi di ricerca. Qualsiasi protocollo combinato è strettamente sperimentale e al di fuori della base probatoria sintetizzata in questo articolo.
L’emivita di circa 144 ore di retatrutide e quella di circa 120 ore di tirzepatide sostengono entrambe una singola dose sottocutanea settimanale, lo schema utilizzato in tutti gli studi registrativi. L’emivita leggermente più lunga di retatrutide offre un modesto margine di sicurezza contro la variabilità in caso di dose mancata, ma non modifica la cadenza settimanale di fondo.
Sì. Sia retatrutide sia tirzepatide sono elencati per uso di ricerca nei canali UE e USA. La disponibilità, le dimensioni dei flaconcini e i prezzi specifici per canale sono indicati nella pagina di dettaglio di ciascun prodotto.
Le letture di TRIUMPH-1 (obesità senza T2D), TRIUMPH-2 (obesità con T2D) e TRIUMPH-3 (obesità con malattia cardiovascolare conclamata) sono attese nel corso del 2026 secondo le indicazioni di Lilly 4. Ciascuna amplierà sostanzialmente la base probatoria di retatrutide; collettivamente determineranno se il tetto di TRIUMPH-4 si generalizzi tra le popolazioni e se il deposito di una NDA possa anticiparsi rispetto all’attuale finestra del Q4 2026, oggi la più precoce ipotizzata.
Retatrutide vince sulle dimensioni più rilevanti per la ricerca di frontiera: tetto osservato più alto in TRIUMPH-4, ampiezza meccanicistica del triplo agonismo e direzione coerente in entrambe le meta-analisi di rete pubblicate. Tirzepatide rimane la molecola di riferimento per i protocolli che oggi richiedono la base probatoria pubblicata più profonda.