

De triple-agonist die een nieuw plafond zette tegenover de dual-agonist die de categorie heeft opgebouwd. Een vergelijking voor onderzoeksprotocollen die willen begrijpen welk molecuul de grens vormt, welk de standaard is, en waarom dat onderscheid ertoe doet.

Tirzepatide (Eli Lilly’s Mounjaro/Zepbound) is een duale GLP-1/GIP-receptoragonist met vier jaar fase-3-data, drie FDA-goedkeuringen en een gepubliceerde cardiovasculaire-uitkomstentrial. Retatrutide, het opvolgmolecuul van Lilly, is een triple-agonist die de glucagonreceptor toevoegt aan dezelfde duale ruggengraat en in de eerste fase-3-uitlezing de diepste gewichtsreductie ooit gerapporteerd in een registratie-obesitastrial liet zien: ongeveer 28,7% na 68 weken 5 tegenover de SURMOUNT-1-piek van tirzepatide van ruwweg 22,5% na 72 weken 13.
De bewijsbases zijn niet symmetrisch. Tirzepatide heeft het volwassen, peer-reviewed dossier. Retatrutide heeft het hogere waargenomen plafond, een mechanistisch breder doelprofiel en twee netwerkmeta-analyses die dezelfde richting wijzen 20 21. Voor onderzoeksprotocollen die het maximale therapeutische plafond en een breed mechanisme prioriteren, is onze redactionele keuze retatrutide. Voor protocollen die diepte van regulatorisch bewijs en een uitgekristalliseerd veiligheidslabel waarderen, blijft tirzepatide het referentiemolecuul.
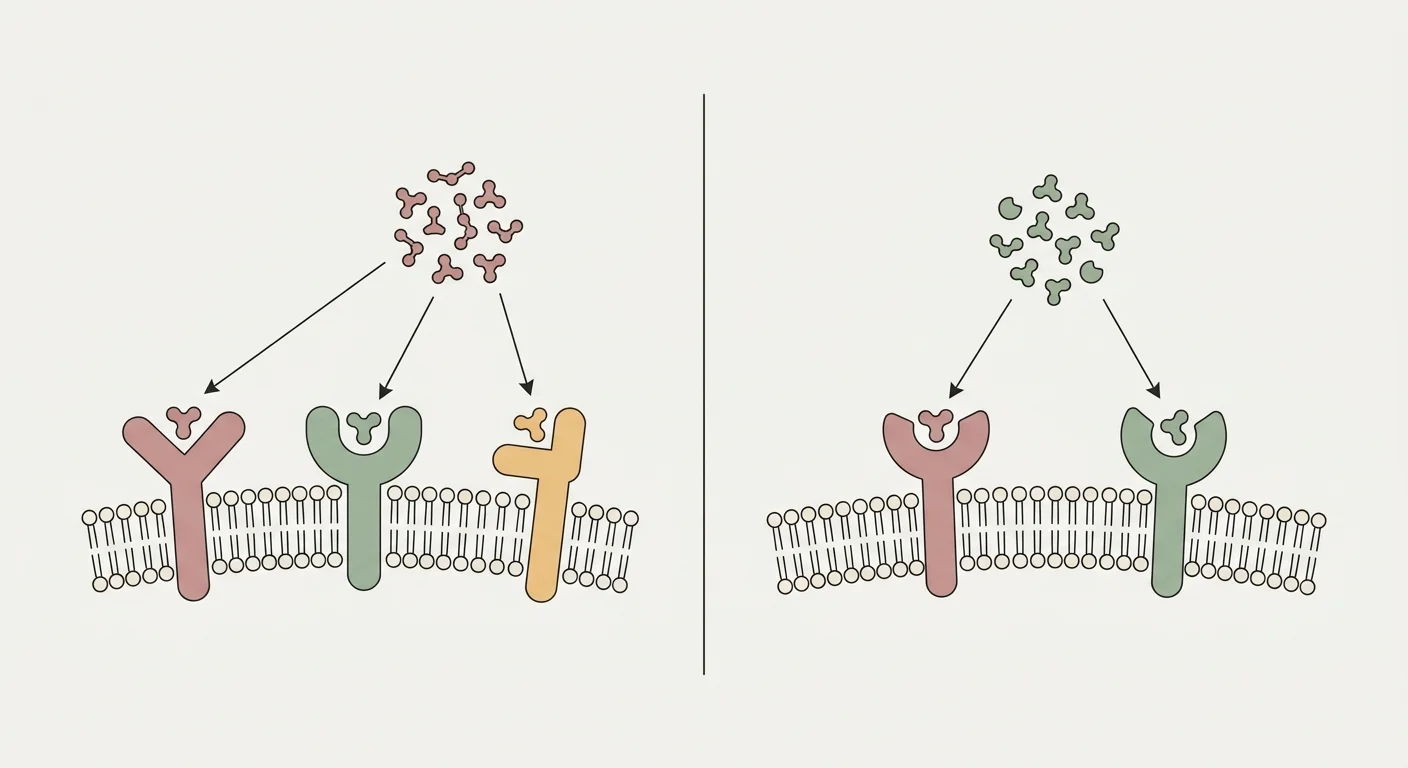
Retatrutide (LY3437943) is een enkel peptide dat is ontworpen om drie incretine-familie-receptoren tegelijk te activeren: de glucagon-like peptide-1-receptor (GLP-1R), de glucose-afhankelijke insulinotrope polypeptide-receptor (GIPR) en de glucagonreceptor (GCGR) 26. De GLP-1R-arm zorgt voor de centrale eetlustremming, vertraagde maaglediging en glucose-afhankelijke insulinesecretie die we kennen van semaglutide en tirzepatide 24. De GIPR-arm voegt synergetische insulinotrope activiteit toe en versterkt in vetweefsel een gezonde lipidenbuffering, waardoor ectopische vetafzetting in lever en spier afneemt 25.
De onderscheidende arm is GCGR. Glucagon wordt doorgaans omschreven als het contraregulerende hormoon dat het bloedsuiker doet stijgen; binnen een evenwichtige triple-agonist wordt het klassieke effect op hepatische glucoseproductie gecompenseerd door de gelijktijdige GLP-1R/GIPR-insulinotrope werking, terwijl de metabole effecten die peptide-ontwerpers daadwerkelijk willen behouden blijven: verhoogd energieverbruik via thermogenese in bruin vetweefsel en oxidatie in skeletspieren, lipolyse in wit vetweefsel met afgifte van vrije vetzuren voor bèta-oxidatie, en hepatische vetzuuroxidatie die triglyceriden uit de lever afvoert 27. In de fase-2a-MASLD-data leverde retatrutide bij de hoogste dosis ongeveer 85–90% reductie van leververvetting op; ongeveer 90% van de deelnemers met 12 mg bereikte na 48 weken een leververvetting onder 5%, een omvang die duaal agonisme niet heeft laten zien 3.
Per april 2026 is er geen directe gerandomiseerde gecontroleerde trial gepubliceerd of aangekondigd waarin retatrutide rechtstreeks tegen tirzepatide wordt vergeleken. Een registratie-head-to-head-trial (NCT06662383) is zichtbaar in de pijplijntracker van Lilly, maar er zijn nog geen resultaten gerapporteerd. Elke vergelijkende uitspraak in dit artikel draagt daarom een voorbehoud: het is ofwel een indirecte vergelijking tussen trials met verschillende populaties, doseerschema’s en eindpunten, ofwel een mechanistische extrapolatie vanuit preklinische en fase-2-data. Dat is geen reden om het signaal te negeren, maar wel om het te kwalificeren.
Twee netwerkmeta-analyses hebben geprobeerd de moleculen op dezelfde schaal te plaatsen. De analyse van oktober 2025, gepubliceerd in het Journal of the Endocrine Society (abstract SUN-659, met het volledige peer-reviewed artikel op PMC12544991), rapporteerde retatrutide met een gemiddelde absolute reductie van −16,34 kg en −23,77% lichaamsgewicht tegenover −11,82 kg en −16,79% voor tirzepatide, een indirect voordeel in het voordeel van retatrutide 20. Dezelfde analyse signaleerde een hoger relatief risico op bijwerkingen voor retatrutide (RR 4,10 vs 2,78), in lijn met een hogere gastro-intestinale belasting bij de hoogste doses. Een bredere zeven-agentennetwerkmeta-analyse, gepubliceerd in Metabolism (2024), rangschikte moleculen voor gewichtsverlies als retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, met consistente rangordes voor tailleomvang, HbA1c en nuchtere plasmaglucose 21.
Beide netwerkmeta-analyses zijn numeriek en richtinggevend in het voordeel van retatrutide, maar de afwezigheid van direct RCT-bewijs betekent dat elke vergelijkende uitspraak een voorbehoud moet dragen. Voor onderzoeksdoeleinden is dit een reden voor verder onderzoek, niet om het signaal terzijde te schuiven.
Het fase-2-veiligheidsprofiel is consistent met de klasse van GLP-1-receptoragonisten en wordt gedomineerd door dosisafhankelijke gastro-intestinale bijwerkingen die zich concentreren in de eerste één tot twee weken van elke titratiestap. De fase-3-veiligheid (TRIUMPH-4) is per april 2026 alleen beschikbaar als top-line uit een persbericht en is nog niet peer-reviewed op het niveau van de volledige dataset.
De top-line van TRIUMPH-4 rapporteert ~28,7% reductie na 68 weken, wat de SURMOUNT-1-piek van tirzepatide na 72 weken met circa zes procentpunten overtreft. Beide gepubliceerde netwerkmeta-analyses wijzen in dezelfde richting.
De GCGR-arm voegt routes toe die tirzepatide niet heeft: hepatische vetzuuroxidatie (~85–90% reductie van leververvetting in fase-2a MASLD), lipolyse in vetweefsel en thermogeen energieverbruik.
Twaalf+ fase-3-trials, drie FDA-goedkeuringen, een gepubliceerde CVOT bij 13.165 patiënten en een uitgekristalliseerde veiligheidsenveloppe in de productinformatie. Het referentiemolecuul voor GLP-1/GIP-onderzoek vandaag de dag.
SURPASS-2 versloeg semaglutide 1 mg head-to-head op HbA1c; SURPASS-CVOT is de enige gepubliceerde cardiovasculaire-uitkomstentrial voor beide moleculen. Het bewijs voor retatrutide bij T2D blijft fase 2 (Rosenstock 2023).
Tirzepatide, ondubbelzinnig. Twaalf+ fase-3-trials, drie FDA-goedkeuringen en een gepubliceerde cardiovasculaire-uitkomstentrial bij 13.165 patiënten 12. Retatrutide heeft één fase-3-top-line (TRIUMPH-4) en een fase-2-programma met ongeveer zes peer-reviewed publicaties 1 5. De kloof zal in 2026 kleiner worden naarmate TRIUMPH-1, TRIUMPH-2 en TRIUMPH-3 hun resultaten geven.
Nee. Per april 2026 is er geen directe RCT van retatrutide vs tirzepatide gepubliceerd of publiekelijk gerapporteerd. Het vergelijkende bewijs blijft beperkt tot twee indirecte netwerkmeta-analyses, die beide in de richting van retatrutide wijzen, maar geen vervanging kunnen zijn voor een head-to-head trial 20 .
Retatrutide is onze keuze. Niet omdat het meer trialdata heeft, dat is namelijk niet zo. Het fase-3-programma van tirzepatide is vier jaar dieper, de drie FDA-goedkeuringen omspannen type 2 diabetes, chronisch gewichtsbeheer en obstructief slaapapneu, en de gepubliceerde cardiovasculaire-uitkomstentrial bij meer dan dertienduizend patiënten is een feit dat we niet betwisten 12 28. Voor onderzoeksprotocollen die de diepste, meest doorgelichte bewijsbasis nodig hebben die de incretineklasse vandaag de dag biedt, is tirzepatide het referentiemolecuul en zal dat blijven totdat het TRIUMPH-programma is afgerond.
Maar voor onderzoeksprotocollen die het hoogste therapeutische plafond nastreven, vallen de cijfers in het voordeel van retatrutide uit. De eerste fase-3-uitlezing rapporteerde ongeveer 28,7% gewichtsreductie bij 12 mg over 68 weken 5, een betekenisvol plafondvoordeel van zes procentpunten ten opzichte van de SURMOUNT-1-piek van tirzepatide van 22,5% over 72 weken 13. De mechanistische verklaring is niet speculatief: de glucagonreceptor voegt hepatische vetzuuroxidatie, lipolyse in vetweefsel en thermogeen energieverbruik toe die duaal agonisme per ontwerp niet kan aanspreken 27, en de 85–90% reductie van leververvetting in de fase-2a-MASLD-uitlezing is een directe handtekening van die route 3. Beide gepubliceerde netwerkmeta-analyses wijzen in de richting van retatrutide 20 21. De bewijsbasis zal volwassen worden; het plafond zal, per ontwerp, niet naar beneden bewegen.
Voor de onderzoeksgrens van metabole peptidetherapie is retatrutide de winnaar. Voor protocollen die boven alles waarde hechten aan diepte van regulatorisch bewijs, blijft tirzepatide de standaard. Dat is een duidelijker rolverdeling dan de meeste “X vs Y”-vergelijkingen kunnen bieden, en eerlijkheid over die verdeling is nuttiger dan een gedwongen enkele winnaar.
Aanwezig; ~85–90% reductie van leververvetting in fase-2a MASLD 3
Per ontwerp afwezig
~144 u (~6 dagen)
~120 u (~5 dagen)
1 top-line (TRIUMPH-4); TRIUMPH-1/2/3 nog uitstaand 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Geen (geen CVOT gestart)
SURPASS-CVOT (n=13.165; NEJM dec 2025) 12
Geen (geen goedgekeurd label)
MTC schildklier-C-cel (knaagdier, humane relevantie niet vastgesteld) 28
Niet gepubliceerd
Niet gepubliceerd
Eenmaal per week, subcutaan
Eenmaal per week, subcutaan
VS: op zijn vroegst eind 2027 (NDA op zijn vroegst Q4 2026) 22
Reeds goedgekeurd (VS: 2022/2023/2024; EU: 2022/2024)
Gelyofiliseerd; reconstitutie met BAC-water; 2–8 °C
Gelyofiliseerd; reconstitutie met BAC-water; 2–8 °C
Hoger plafond + breedte van glucagonreceptor
Lager plafond; best gekarakteriseerde veiligheidsenveloppe
Tirzepatide (LY3298176) is een duale GLP-1R/GIPR-agonist, een enkel peptide van 39 residuen dat is afgestemd om beide incretinereceptoren met vergelijkbare potentie te activeren. De GLP-1R-arm draagt hetzelfde kernmechanisme bij dat we kennen van de eerste generatie GLP-1-analogen: glucose-afhankelijke insulinesecretie, onderdrukking van glucagon door alfacellen, hypothalame regulatie van de eetlust en vertraagde maaglediging 24.
Wat tirzepatide onderscheidt van pure GLP-1-agonisten, is de toegevoegde GIPR-activiteit. Preklinisch leidt co-toediening van GIP met GLP-1 tot additieve en in sommige metingen synergetische verlagingen van lichaamsgewicht en glucose, sterker dan elk afzonderlijk 25. Centrale GIPR-activatie lijkt de door GLP-1 geïnduceerde anorexie te versterken via hypothalame POMC-signalering; perifere GIPR-activatie in wit vetweefsel verhoogt de buffercapaciteit van het depot en vermindert de noodzaak voor ectopische afzetting. Het waarneembare gevolg is het meest potente gewichts- en glucoseverlagende profiel van elk vóór retatrutide goedgekeurd molecuul: SURMOUNT-1 rapporteerde ongeveer 22,5% gewichtsreductie bij de dosis van 15 mg over 72 weken 13, en SURMOUNT-5 toonde tirzepatide head-to-head superieur aan semaglutide 2,4 mg over 72 weken (−20,2% vs −13,7%) 18.
De glucagonreceptor-arm is de mechanistische onderscheider van retatrutide. Preklinische en fase-2-data wijzen erop dat dit zich vertaalt naar lipidenverlagende, leververvetting-reducerende en energieverbruik-verhogende effecten die tirzepatide per ontwerp niet heeft. Of dit zich vertaalt naar het in netwerkmeta-analyses gesuggereerde voordeel in directe vergelijking, blijft open totdat een head-to-head RCT resultaten geeft, waarvan er per april 2026 nog geen is aangekondigd.
De diepte van het bewijs van tirzepatide is op dit moment ongeëvenaard: twaalf fase-3-trials verspreid over twee ziekteprogramma’s, een gepubliceerde cardiovasculaire-uitkomstentrial bij meer dan dertienduizend patiënten en drie FDA-goedkeuringen op het label. De beschikbare uitlezing van retatrutide is weliswaar uniek, maar overtreft het beste fase-3-plafond van tirzepatide bij een kortere observatieperiode. Dat is een signaal dat serieuze aandacht verdient naarmate TRIUMPH-1, TRIUMPH-2 en TRIUMPH-3 in 2026 en 2027 tot wasdom komen.
Volwassen veiligheidsenveloppe in de productinformatie van Mounjaro en Zepbound. De veelvoorkomende bijwerkingen weerspiegelen de GLP-1-klasse en concentreren zich rond dosisescalatie; ernstige risico's zijn vastgelegd in een zwarte-kaderwaarschuwing en een reeks waarschuwingen en voorzorgsmaatregelen die zijn verfijnd via post-marketing-bewaking (FAERS-analyse 2024 en EMA-farmacovigilantie).
Dit artikel is een redactionele vergelijking opgesteld voor lezers in een onderzoekscontext. Noch retatrutide noch tirzepatide wordt via deze site aangeboden of aanbevolen voor humane zelftoediening. Waar tirzepatide wordt voorgeschreven, is het uitsluitend beschikbaar onder toezicht van een arts in jurisdicties waar het is goedgekeurd (Mounjaro voor T2D; Zepbound voor chronisch gewichtsbeheer en obstructief slaapapneu). Retatrutide is per april 2026 wereldwijd in onderzoek en mag uitsluitend worden gehanteerd binnen passende onderzoeksprotocollen.
De hier samengevatte veiligheidsdata weerspiegelen gepubliceerde fase-2- en fase-3-datasets en de actuele productinformatie. Nieuwe signalen kunnen op elk moment naar voren komen; de datum lastUpdated op deze pagina geeft de afsluitdatum van onze beoordeling aan. Niets op deze pagina vormt medisch advies of een vervanging voor consultatie van een gekwalificeerd arts.
Tirzepatide is goedgekeurd onder twee merknamen: Mounjaro voor type 2 diabetes (FDA mei 2022) en Zepbound voor chronisch gewichtsbeheer (november 2023) en matig tot ernstig obstructief slaapapneu met obesitas (december 2024) 28. Retatrutide is overal in onderzoek; per april 2026 is geen NDA ingediend 22.
Retatrutide, op basis van de beschikbare data. TRIUMPH-4 rapporteerde ~−28,7% bij 12 mg over 68 weken 5; de beste fase-3-uitlezing van tirzepatide voor obesitas, SURMOUNT-1 bij 15 mg over 72 weken, was ~−22,5% 13. Beide gepubliceerde netwerkmeta-analyses rangschikken retatrutide hoger op gewichtsreductie 20 21.
Op klasseniveau hebben beide een GI-gedomineerd profiel (misselijkheid, braken, diarree) dat zich concentreert rond dosisescalatie. De netwerkmeta-analyse van oktober 2025 rapporteerde een hoger relatief risico op bijwerkingen voor retatrutide (RR 4,10) dan voor tirzepatide (RR 2,78), in lijn met een hogere GI-belasting bij de hoogste doses 20. Tirzepatide draagt een zwarte-kaderwaarschuwing voor MTC en heeft een gekarakteriseerd profiel voor pancreatitis, galblaasaandoeningen en overgevoeligheid 28 29; het analoge langetermijnveiligheidsprofiel van retatrutide is nog niet vastgesteld.
Gepubliceerde fase-2- en fase-3-trials voor beide moleculen werven deelnemers in monotherapie (met of zonder achtergrondtherapie voor T2D zoals metformine of insuline). Er is geen gepubliceerd bewijs over het stapelen van een van beide met andere onderzoekspeptiden. Elk combinatieprotocol is strikt experimenteel en valt buiten de bewijsbasis die in dit artikel wordt samengevat.
De halfwaardetijd van retatrutide van ~144 uur en die van tirzepatide van ~120 uur ondersteunen beide een enkele wekelijkse subcutane dosis, het schema dat in elke registratietrial is gehanteerd. De iets langere halfwaardetijd van retatrutide biedt een bescheiden buffer tegen variabiliteit bij gemiste doses, maar verandert de fundamentele eenmaal-per-week-cadans niet.
Ja. Zowel retatrutide als tirzepatide is voor onderzoeksgebruik vermeld in zowel het EU- als het VS-kanaal. Beschikbaarheid, vialgroottes en kanaalspecifieke prijzen worden weergegeven op de detailpagina van elk product.
De uitlezingen van TRIUMPH-1 (obesitas zonder T2D), TRIUMPH-2 (obesitas met T2D) en TRIUMPH-3 (obesitas met vastgestelde cardiovasculaire ziekte) worden in de loop van 2026 verwacht volgens de richtlijnen van Lilly 4. Elk daarvan zal de bewijsbasis voor retatrutide wezenlijk uitbreiden; gezamenlijk zullen ze bepalen of het plafond van TRIUMPH-4 generaliseert over populaties heen, en of een NDA-indiening vervroegd kan worden ten opzichte van het huidige op zijn vroegst Q4 2026-venster.
Retatrutide wint op de dimensies die het meest van belang zijn voor onderzoek aan de grens: een hoger waargenomen plafond in TRIUMPH-4, breedte van het triple-agonist-mechanisme en een consistente richting in beide gepubliceerde netwerkmeta-analyses. Tirzepatide blijft het referentiemolecuul voor protocollen die de diepste op dit moment gepubliceerde bewijsbasis nodig hebben.