

El triple-agonista que ha fijado un nuevo techo frente al doble-agonista que construyó la categoría. Una comparación pensada para protocolos de investigación que quieren entender cuál es la molécula de la frontera, cuál es el estándar y por qué la distinción importa.

Tirzepatide (Mounjaro/Zepbound de Eli Lilly) es un doble agonista de los receptores GLP-1 y GIP con cuatro años de datos en fase 3, tres aprobaciones de la FDA y un ensayo publicado de resultados cardiovasculares. Retatrutide, la molécula sucesora de Lilly, es un triple agonista que añade el receptor de glucagón al mismo esqueleto dual y, en su primera lectura de fase 3, ha producido la reducción de peso más profunda jamás reportada en un ensayo registracional de obesidad: en torno al 28,7% a las 68 semanas 5 frente al pico de SURMOUNT-1 con tirzepatide, de aproximadamente 22,5% a las 72 semanas 13.
Las bases de evidencia no son simétricas. Tirzepatide cuenta con el dosier maduro y revisado por pares. Retatrutide presenta el techo observado más alto, un perfil de dianas mecanísticamente más amplio y dos meta-análisis en red que apuntan en su dirección 20 21. Para protocolos de investigación que prioricen el máximo techo terapéutico y la amplitud mecanística, nuestra elección editorial es retatrutide. Para protocolos que valoren la profundidad de evidencia de grado regulatorio y una ficha de seguridad consolidada, tirzepatide sigue siendo la molécula de referencia.
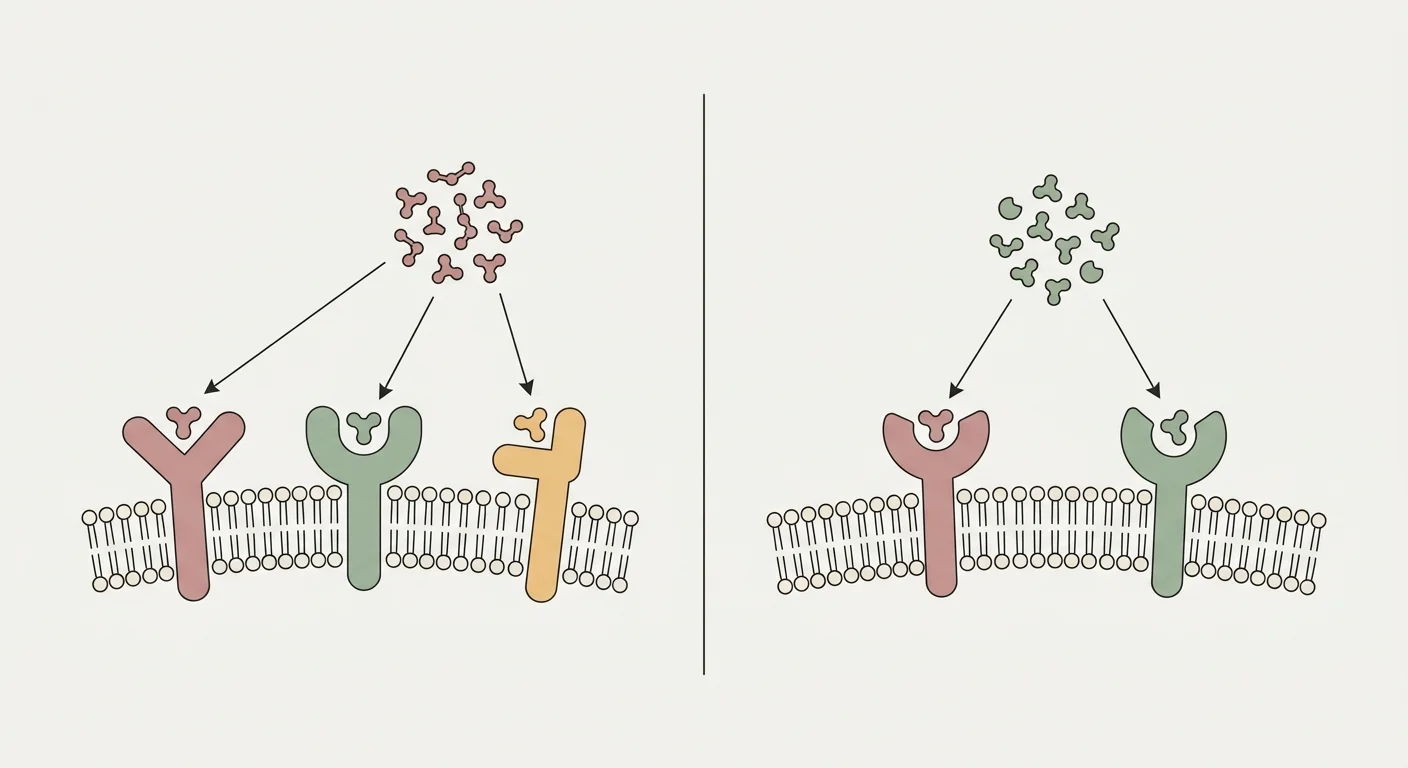
Retatrutide (LY3437943) es un péptido único diseñado para activar simultáneamente tres receptores de la familia incretina: el receptor del péptido similar al glucagón tipo 1 (GLP-1R), el receptor del polipéptido insulinotrópico dependiente de glucosa (GIPR) y el receptor de glucagón (GCGR) 26. El brazo GLP-1R impulsa la supresión central del apetito, el retraso del vaciado gástrico y la secreción de insulina dependiente de glucosa, ya familiares por semaglutide y tirzepatide 24. El brazo GIPR añade actividad insulinotrópica sinérgica y, en el tejido adiposo, mejora el tamponamiento lipídico saludable, reduciendo el depósito ectópico de grasa en hígado y músculo 25.
El brazo distintivo es GCGR. Habitualmente se presenta al glucagón como la hormona contrarreguladora que eleva la glucemia; sin embargo, en el contexto de un triple agonista equilibrado, su efecto clásico sobre la producción hepática de glucosa queda compensado por la acción insulinotrópica simultánea de GLP-1R/GIPR, mientras se conservan los efectos metabólicos que los diseñadores de péptidos sí desean obtener de GCGR: un aumento del gasto energético vía termogénesis del tejido adiposo pardo y oxidación en el músculo esquelético, lipólisis adiposa con liberación de ácidos grasos libres para la beta-oxidación, y oxidación hepática de ácidos grasos que aclara triglicéridos del hígado 27. En los datos de fase 2a en MASLD, retatrutide produjo en torno al 85–90% de reducción de grasa hepática a la dosis más alta; alrededor del 90% de los participantes con 12 mg alcanzó una grasa hepática inferior al 5% a las 48 semanas, una magnitud que el agonismo dual no ha demostrado 3.
No se ha publicado ni anunciado ningún ensayo aleatorizado controlado directo entre retatrutide y tirzepatide a fecha de abril de 2026. Un ensayo registracional cara a cara (NCT06662383) figura en el seguimiento de pipeline de Lilly, pero no ha reportado resultados. Cualquier afirmación comparativa recogida en este artículo lleva, por tanto, una salvedad: o bien procede de una comparación indirecta entre ensayos con poblaciones, esquemas de dosificación y variables de resultado distintos, o bien es una extrapolación mecanística a partir de datos preclínicos y de fase 2. Esto no es una razón para ignorar la señal — es una razón para matizarla.
Dos meta-análisis en red han intentado situar a las moléculas en una misma escala. El análisis de octubre de 2025, publicado en el Journal of the Endocrine Society (resumen SUN-659, con artículo completo revisado por pares en PMC12544991), reportó para retatrutide una reducción absoluta media de −16,34 kg y −23,77% del peso corporal, frente a −11,82 kg y −16,79% para tirzepatide, una ventaja indirecta a favor de retatrutide 20. El mismo análisis señaló un riesgo relativo de eventos adversos más alto para retatrutide (RR 4,10 vs 2,78), congruente con una mayor carga gastrointestinal en las dosis más altas. Un meta-análisis en red más amplio, con siete agentes, publicado en Metabolism (2024), ordenó las moléculas en pérdida de peso como retatrutide 12 mg > retatrutide 8 mg > tirzepatide 15 mg, con clasificaciones coherentes en circunferencia de cintura, HbA1c y glucemia plasmática en ayunas 21.
Ambos meta-análisis en red favorecen a retatrutide en términos numéricos y direccionales, pero la ausencia de evidencia directa de ECA implica que cualquier afirmación comparativa debe llevar una salvedad. A efectos de investigación, esta es una razón para profundizar el análisis, no para descartar la señal.
El perfil de seguridad de fase 2 es coherente con la clase de los agonistas del receptor de GLP-1, dominado por eventos adversos gastrointestinales dependientes de la dosis que se concentran en la primera o segunda semana de cada escalón de escalado. La seguridad en fase 3 (TRIUMPH-4) está disponible, a fecha de abril de 2026, únicamente como lectura preliminar en nota de prensa y todavía no se ha revisado por pares con el dataset completo.
La lectura preliminar de TRIUMPH-4 reporta una reducción del ~28,7% a las 68 semanas, superior al pico de SURMOUNT-1 con tirzepatide a las 72 semanas en aproximadamente seis puntos porcentuales. Ambos meta-análisis en red publicados apuntan en la misma dirección.
El brazo GCGR añade rutas que tirzepatide no aborda: oxidación hepática de ácidos grasos (~85–90% de reducción de grasa hepática en fase 2a en MASLD), lipólisis adiposa y gasto energético termogénico.
Más de doce ensayos de fase 3, tres aprobaciones de la FDA, un CVOT publicado en 13.165 pacientes y una ficha técnica con un perfil de seguridad maduro. Es la molécula de referencia para investigación con GLP-1/GIP hoy.
SURPASS-2 superó a semaglutide 1 mg en comparación directa en HbA1c; SURPASS-CVOT es el único ensayo de resultados cardiovasculares publicado entre ambas moléculas. La evidencia de retatrutide en T2D sigue siendo de fase 2 (Rosenstock 2023).
Tirzepatide, sin ambigüedades. Más de doce ensayos de fase 3, tres aprobaciones de la FDA y un ensayo de resultados cardiovasculares publicado en 13.165 pacientes 12. Retatrutide cuenta con una sola lectura preliminar de fase 3 (TRIUMPH-4) y un programa de fase 2 con alrededor de seis publicaciones revisadas por pares 1 5. La brecha se irá estrechando a lo largo de 2026 a medida que TRIUMPH-1, TRIUMPH-2 y TRIUMPH-3 vayan reportando.
No. No se ha publicado ni reportado públicamente ningún ECA directo de retatrutide frente a tirzepatide a fecha de abril de 2026. La evidencia comparativa se limita a dos meta-análisis en red indirectos, ambos en la dirección de retatrutide, que no pueden sustituir a un ensayo cara a cara 20 .
Retatrutide es nuestra elección. No porque cuente con más datos de ensayos — no es el caso. El programa de fase 3 de tirzepatide es cuatro años más profundo, sus tres aprobaciones de la FDA cubren la diabetes tipo 2, el control crónico de peso y la apnea obstructiva del sueño, y su ensayo publicado de resultados cardiovasculares en más de trece mil pacientes es un hecho que no discutimos 12 28. Para protocolos de investigación que necesiten la base de evidencia más profunda y escrutada disponible hoy en la clase incretínica, tirzepatide es la molécula de referencia y lo seguirá siendo hasta que el programa TRIUMPH se complete.
Pero para protocolos de investigación que persiguen el techo terapéutico más alto, los números favorecen a retatrutide. Su primera lectura de fase 3 reportó alrededor del 28,7% de reducción de peso a 12 mg a lo largo de 68 semanas 5— una ventaja relevante de seis puntos porcentuales en el techo respecto al pico de SURMOUNT-1 con tirzepatide, del 22,5% a las 72 semanas 13. La explicación mecanística no es especulativa: el receptor de glucagón añade oxidación hepática de ácidos grasos, lipólisis adiposa y gasto energético termogénico que el agonismo dual no puede involucrar por diseño 27, y la reducción del 85–90% de grasa hepática observada en la lectura de fase 2a en MASLD es una firma directa de esa ruta 3. Ambos meta-análisis en red publicados apuntan en la dirección de retatrutide 20 21. La base de evidencia madurará; el techo, por diseño, no bajará.
Para la frontera de investigación de la terapia metabólica peptídica, retatrutide es el ganador. Para protocolos que valoran por encima de todo la profundidad de grado regulatorio, tirzepatide sigue siendo el estándar. Esta es una división de papeles más nítida que la que ofrecen la mayoría de comparaciones del tipo «X vs Y», y la honestidad sobre esa división resulta más útil que un único ganador forzado.
Presente; reducción de grasa hepática del ~85–90% en fase 2a en MASLD 3
Ausente por diseño
~144 h (~6 días)
~120 h (~5 días)
1 lectura preliminar (TRIUMPH-4); TRIUMPH-1/2/3 pendientes 4
12+ (SURPASS 1–6, CVOT, PEDS; SURMOUNT 1–5, OSA)
Ninguno (no se ha iniciado un CVOT)
SURPASS-CVOT (n=13.165; NEJM dic. 2025) 12
Ninguno (sin ficha aprobada)
MTC, células C tiroideas (roedor; relevancia humana no establecida) 28
No publicado
No publicado
Una vez por semana, subcutánea
Una vez por semana, subcutánea
EE. UU.: finales de 2027 como muy pronto (NDA en el cuarto trimestre de 2026 en el mejor escenario) 22
Ya aprobado (EE. UU.: 2022/2023/2024; UE: 2022/2024)
Liofilizado; reconstitución con agua bacteriostática; 2–8 °C
Liofilizado; reconstitución con agua bacteriostática; 2–8 °C
Mayor techo + amplitud por receptor de glucagón
Techo más bajo; perfil de seguridad mejor caracterizado
Tirzepatide (LY3298176) es un agonista dual GLP-1R / GIPR — un único péptido de 39 residuos afinado para acoplarse a ambos receptores incretínicos con potencia comparable. El brazo GLP-1R aporta el mismo mecanismo central conocido por la primera generación de análogos del GLP-1: secreción de insulina dependiente de glucosa, supresión del glucagón en la célula alfa, regulación hipotalámica del apetito y enlentecimiento del vaciado gástrico 24.
Lo que distingue a tirzepatide de los agonistas puros del GLP-1 es la actividad GIPR añadida. En el ámbito preclínico, la coadministración de GIP con GLP-1 produce reducciones aditivas y, en algunos parámetros, sinérgicas del peso corporal y la glucemia, superiores a las de cada hormona por separado 25. La activación central del GIPR parece potenciar la anorexia inducida por GLP-1 a través de la señalización hipotalámica POMC; la activación periférica del GIPR en el tejido adiposo blanco mejora la capacidad de tamponamiento del depósito y reduce la necesidad de depósito ectópico. La consecuencia observable es el perfil de reducción de peso y glucemia más potente de cualquier molécula aprobada antes de retatrutide: SURMOUNT-1 reportó alrededor del 22,5% de reducción de peso a la dosis de 15 mg a lo largo de 72 semanas 13, y SURMOUNT-5 mostró tirzepatide superior a semaglutide 2,4 mg en comparación directa a las 72 semanas (−20,2% vs −13,7%) 18.
El brazo del receptor de glucagón es el diferenciador mecanístico de retatrutide. Los datos preclínicos y de fase 2 sugieren que esto se traduce en efectos hipolipemiantes, reductores de la grasa hepática y de incremento del gasto energético que tirzepatide, por diseño, no engloba. Si esto se traducirá en la ventaja en comparación directa que sugieren los meta-análisis en red quedará abierto hasta que un ECA cara a cara reporte resultados — algo que, a fecha de abril de 2026, todavía no se ha anunciado.
La profundidad de evidencia de tirzepatide es hoy inigualable — doce ensayos de fase 3 en dos programas de enfermedad, un ensayo de resultados cardiovasculares publicado en más de trece mil pacientes y tres aprobaciones de la FDA en ficha técnica. La lectura disponible de retatrutide, aunque única, supera el mejor techo de fase 3 de tirzepatide en una ventana de observación más corta. Esa es una señal que merece atención seria a medida que TRIUMPH-1, TRIUMPH-2 y TRIUMPH-3 vayan madurando a lo largo de 2026 y 2027.
Ficha técnica madura, con perfil de seguridad consolidado para Mounjaro y Zepbound. Los eventos adversos comunes reflejan los de la clase GLP-1 y se concentran en el escalado de dosis; los riesgos graves quedan recogidos en un recuadro de advertencia y en un conjunto de advertencias y precauciones refinadas mediante farmacovigilancia poscomercialización (análisis FAERS de 2024 y farmacovigilancia de la EMA).
Este artículo es una comparación editorial elaborada para lectores en contexto de investigación. Ni retatrutide ni tirzepatide se ofrecen ni se recomiendan para autoadministración humana a través de este sitio. Cuando tirzepatide se prescribe, está disponible únicamente bajo supervisión médica en las jurisdicciones en las que ha sido aprobado (Mounjaro para T2D; Zepbound para el control crónico de peso y la apnea obstructiva del sueño). Retatrutide es, a fecha de abril de 2026, una molécula en investigación a nivel global y solo debe manejarse en el marco de protocolos de investigación adecuados.
Los datos de seguridad aquí resumidos reflejan los conjuntos de datos publicados de fase 2 y fase 3, así como la ficha técnica vigente. Pueden surgir nuevas señales en cualquier momento; la fecha indicada como lastUpdated en esta página marca el corte de nuestra revisión. Nada de lo expuesto en esta página constituye consejo médico ni sustituye la consulta con un profesional sanitario cualificado.
Tirzepatide está aprobado bajo dos marcas comerciales: Mounjaro para diabetes tipo 2 (FDA, mayo de 2022) y Zepbound para el control crónico de peso (noviembre de 2023) y para la apnea obstructiva del sueño moderada a grave con obesidad (diciembre de 2024) 28. Retatrutide es una molécula en investigación en todo el mundo; a fecha de abril de 2026 no se ha presentado ninguna NDA 22.
Retatrutide, en función de los datos disponibles. TRIUMPH-4 reportó ~−28,7% a 12 mg a lo largo de 68 semanas 5; la mejor lectura de fase 3 en obesidad de tirzepatide, SURMOUNT-1 a 15 mg durante 72 semanas, fue de ~−22,5% 13. Ambos meta-análisis en red publicados sitúan a retatrutide por delante en reducción de peso corporal 20 21.
A nivel de clase, ambas presentan un perfil dominado por eventos gastrointestinales (náuseas, vómitos, diarrea) que se concentran durante el escalado de dosis. El meta-análisis en red de octubre de 2025 reportó un riesgo relativo de eventos adversos más alto para retatrutide (RR 4,10) que para tirzepatide (RR 2,78), congruente con una mayor carga gastrointestinal a las dosis más altas 20. Tirzepatide cuenta con un recuadro de advertencia por MTC y un perfil caracterizado de pancreatitis, vesícula e hipersensibilidad 28 29; el perfil análogo de seguridad a largo plazo de retatrutide aún no se ha establecido.
Los ensayos publicados de fase 2 y fase 3 de ambas moléculas reclutan en monoterapia (con o sin tratamiento de fondo para T2D, como metformina o insulina). No existe evidencia publicada sobre la combinación de cualquiera de las dos con otros péptidos de investigación. Cualquier protocolo de combinación es estrictamente de investigación y queda fuera de la base de evidencia resumida en este artículo.
La vida media de aproximadamente 144 horas de retatrutide y la de aproximadamente 120 horas de tirzepatide son ambas compatibles con una única dosis subcutánea semanal, esquema utilizado en todos los ensayos registracionales. La vida media ligeramente más larga de retatrutide ofrece un margen modesto frente a la variabilidad por dosis omitidas, pero no modifica la cadencia fundamental de una administración semanal.
Sí. Tanto retatrutide como tirzepatide figuran para uso en investigación en los canales de la UE y de EE. UU. La disponibilidad, los tamaños de vial y los precios específicos de cada canal se muestran en la página de detalle de cada producto.
Se esperan, según las indicaciones de Lilly, las lecturas de TRIUMPH-1 (obesidad sin T2D), TRIUMPH-2 (obesidad con T2D) y TRIUMPH-3 (obesidad con enfermedad cardiovascular establecida) a lo largo de 2026 4. Cada una ampliará materialmente la base de evidencia de retatrutide; en su conjunto, determinarán si el techo observado en TRIUMPH-4 se generaliza entre poblaciones y si la presentación de la NDA se adelanta respecto al horizonte actual del cuarto trimestre de 2026 como caso más temprano.
Retatrutide gana en las dimensiones que más importan para la investigación de frontera: mayor techo observado en TRIUMPH-4, amplitud mecanística como triple agonista y dirección consistente en ambos meta-análisis en red publicados. Tirzepatide sigue siendo la molécula de referencia para protocolos que necesitan hoy la base de evidencia publicada más profunda.